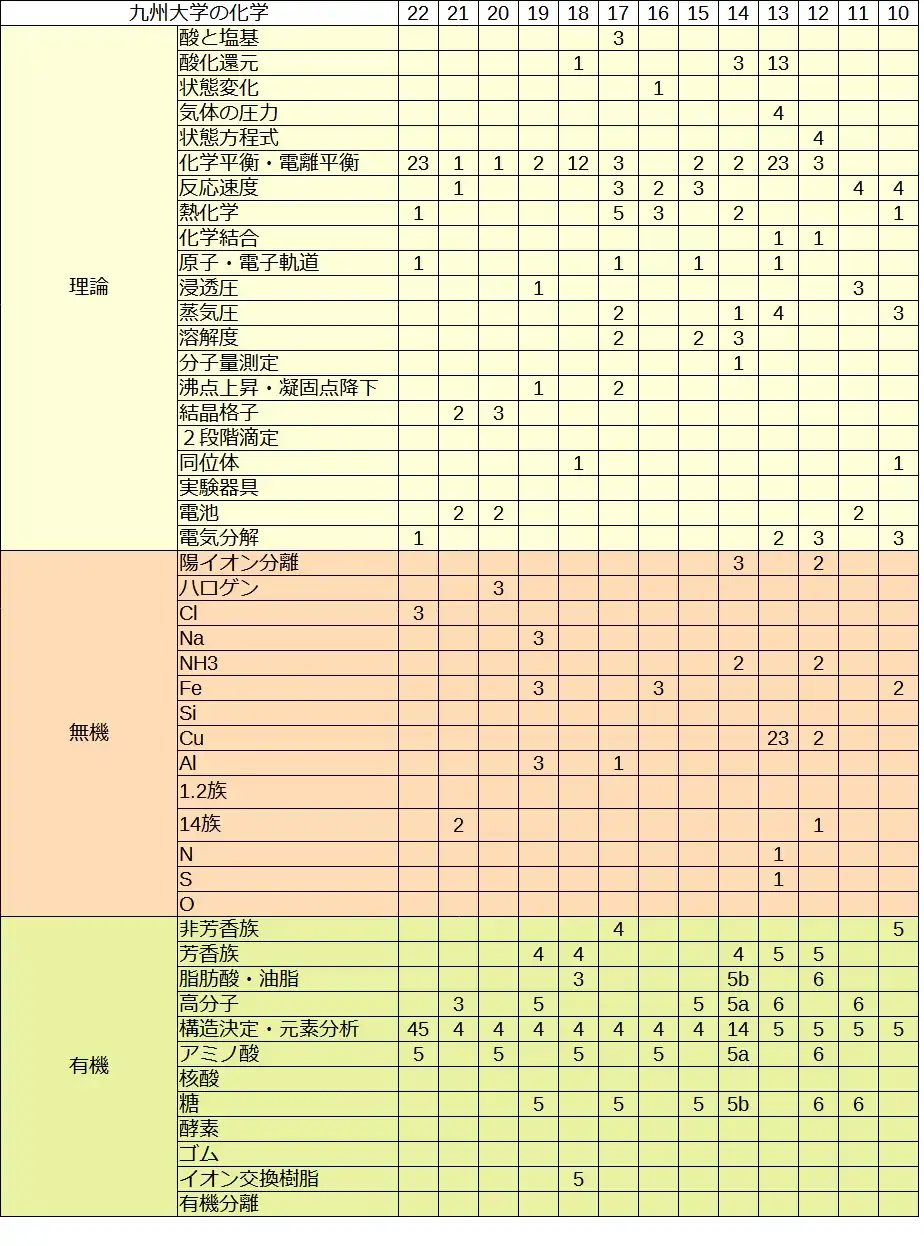
九州大学の化学過去問を1980~2023年まで43年分研究しました。
その一部を公開します。
各小問ごとの解説に加え、高校偏差値60前後の高校で落ちこぼれて
- 1番簡単な国立大学を目指せない
- 九州工業大学・熊本大学など想像もできない
などの学生さんが九大合格できる所まで簡略化した「点数の取り方」を公開します。
偏差値60前後の高校
| 高校 偏差値 | 6学区 | 5学区 | 4学区 | 3学区 | 2学区 |
|---|---|---|---|---|---|
| 63 | 春日 | 香住丘 | |||
| 62 | 福岡中央 | ||||
| 61 | 筑紫 | 宗像 | |||
| 60 | 筑前 | 新宮 | 八幡 | 戸畑 | |
| 59 | 筑紫中央 | ||||
| 58 | |||||
| 57 | 北筑 | 小倉西 | |||
| 56 | 香椎 |


- 九州大学の化学2023年・令和5年度
- 九州大学の化学2022年・令和4年度
- 九州大学の化学2021年・令和3年度
- 九州大学の化学2020年・令和2年度
- 九州大学の化学2019年・平成31年度
- 九州大学の化学2018年・平成30年度
- 九州大学の化学2017年・平成29年度
- 九州大学の化学2016年・平成28年度
- 九州大学の化学2015年・平成27年度
- 九州大学の化学2014年・平成26年度
- 九州大学の化学2013年・平成25年度
- 九州大学の化学2012年・平成24年度
- 九州大学の化学2011年・平成23年度
- 九州大学の化学2010年・平成22年度
- 九州大学の化学2009年・平成21年度
- 九州大学の化学2008年・平成20年度
- 九州大学の化学2007年・平成19年度
- 九州大学の化学2006年・平成18年度
- 九州大学の化学2005年・平成17年度
- 九州大学の化学2004年・平成16年度
- おわりに
九州大学の化学2023年・令和5年度
大問1

「気体全般」からの出題です。
知識の必要性に関して、普通程度です。理論上の気体と実際の気体で計算結果にズレが出る理由を問われています。思考力の必要性に関して、やや難しいです。問題集による練習機会が少ない「実在気体の状態方程式」を問題文で与えられ、その場で理解しながら応用していく問題です。また、最後に付け足された「化学平衡」1問も少し歯ごたえがあります。
問1に関して、知識問題です。気体の性質に関する語句問題を3つ答えます。
- 理想気体に比べ、実際のNH₃の体積は「ア:小さく」なります。分子間に水素結合があるからです。
- 理想気体に比べ、実際のH₂の体積は「イ:大きく」なります。分子自身に体積があるからです。
- 実在気体においても「ウ:高温・低圧」であれば、理想気体としてふるまいます。高温であれば分子間力を無視でき、低圧であれば分子自身の体積を無視できるからです。
理想気体と実在気体の違いに関するやや細かい知識を問われています。不合格者さんには難しく、合格者さんは正解してくるので、合否を分ける1問です。
問2に関して、知識問題です。問1(ウ)の「圧力条件の根拠」を20字以内で答えます。
ポイントは「少ない文字数なので難しく考えないこと」です。
- 密度が下がり分子間の距離が広がるから(18文字)
(これが正解です)
問1の理由を答えるので、難易度は問1と同じく、合否を分ける1問です。
問3に関して、思考問題です。実在気体における「理想気体からのズレ」をグラフから読み取ります。
ポイントは「3つの気体が全て無極性分子」である事です。分子間に水素結合がはたらかないため、分子間力は分子量に依存します。
- 3種の気体(H2、CH4、CO2)はいずれも無極性分子
- ゆえに、分子量が大きくなるほど分子間力が強くなり、理論値からずれていく
- よって、正解は以下のとおり
| 気体 | 分子量 | |
|---|---|---|
| 気体A | H₂ | 2 |
| 気体B | CH₄ | 16 |
| 気体C | CO₂ | 44 |
分子量の小さい順に並べるだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、思考問題です。3つの気体(CH₄、H₂O、NH₃)を「ファンデルワールス定数aが大きい順」に並べます。
ポイントは、ファンデルワールス定数が「分子間力の強さ」を反映した数値であることです。
- 分子間力とは主に「水素結合・静電気力・ファンデルワールス力」なので
- 分子間力の強い順に並べればよい
H₂O>NH₃>CH₄(これが正解です)
分子間力が強い順に並べるだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問5に関して、思考問題です。CH₄分子1個あたりの「分子が自由に動ける体積の減少量」を答えます。
ポイントは「1モルあたりの体積減少量が与えられている」ことです。
- 状態方程式の「V-b」の部分より
分子が自由に動ける体積に影響を与えるのは
bの値とわかる - 今、問題文の表より
1モルあたりのCH₄の体積減少分は
0.0428L/mol - よって、分子1個あたりは
0.0428÷(6.02×10²³)
≒7.11×10⁻²⁶(リットル)
(これが正解です)
「bが体積減少量を表している」と読み取る事は、合格者さんでもやや難しいレベルです。よって、正解できれば他者に差をつける1問です。
問6に関して、思考問題です。問1~問5までの流れから一転、最後に九大の頻出分野「化学平衡」が1問出題されています。
ポイントは「増減表を描くこと」です。平衡と言えば増減表です。
| H₂ | +1/2O₂ | →H₂O | |
| 前 | 0.100mol | x | 0 |
| 中 | -0.100 | -0.050 | +0.100 |
| 後 | 0 | x-0.050 | 0.100 |
- H₂Oが全て気体になったと仮定すると圧力は
P水=nRT/V
=0.100×8.31×10³×300×1/8.31
=3.0×10⁴(Pa) - これは水の飽和蒸気圧を超えているため
P水=3.60×10³(Pa)
となる - よって、PV=nRTより
(38.4-3.6)×10³×8.31=(x-0.050)×8.31×10³×300
∴ x=1.66×10⁻¹(mol)
(これが正解です)
「水の飽和蒸気圧」を含めた化学平衡なので、不合格者さんには難しいレベルです。合格者さんは正解してくるので、合否を分ける1問です。
- 知識:★★★(普通)
- 思考:★★★★(やや難しい)
- 総合:★★★(普通)
- 短評:小問6「化学平衡」を正解したい
大問2

「熱化学」からの出題です。
知識の必要性に関して、やや簡単です。エネルギー図を描く知識、生成熱・燃焼熱などが「何を主役とした熱」なのか知っておけば十分です。思考力の必要性に関して、普通程度です。小問3つともエネルギー図を描ければ正解できます。
問1に関して、知識問題です。(ア)~(キ)に化学式・数値を入れ、エネルギー図を完成させます。
ポイントは「解離エネルギーの定義」です。1molの気体分子をバラバラの原子に戻すのが解離エネルギーなので、それをエネルギー図に描き込んでいけば正解できます。
- (イ)→(ア)が蒸発と書いてあるので
イ:H₂O(液)
ア:H₂O(気)
とわかる - (ウ)+1/2(エ)という表示より
ウ:H₂(気)
エ:O₂(気)
とわかる - 解離エネルギーの表より
オ:926kJ
カ:683kJ(436+494×1/2)
とわかる - よって、残った(キ)は
キ:287kJ
とわかる
以上が正解です。
エネルギー図を完成させるだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、思考問題です。黒鉛の完全燃焼を表す式と、その燃焼熱を答えます。
ポイントは「黒鉛の昇華熱(黒→気)が与えられていないこと」です。COの生成を経由することになります。
- 問題文の「一酸化炭素の生成熱」より
C(黒)+1/2O₂(気)=CO(気)+111kJ - 反応熱=(右辺の結合エネルギー) - (左辺の結合エネルギー)より
111=1073-(x+494×1/2)(xは黒鉛の昇華熱)
∴ x=715 - ここで
C(黒)+O₂(気)=CO₂(気)+QkJ
より
Q=(右辺の結合エネルギ-)-(左辺結合エネルギー)
=1602-(715+494)
=393kJ/mol
(これが正解です)
「黒鉛の昇華熱」に自分で気付く必要があり、不合格者さんには難しいレベルです。合格者さんの一定数が不正解になるレベルなので、正解できれば他者に差をつけられる1問です。
問3に関して、思考問題です。固体グルコースの生成熱と、完全燃焼の式を答えます。
- まず完全燃焼の式は
C₆H₁₂O₆+6O₂→6CO₂+6H₂O
(これが正解です) - エネルギー図より
C₆H₁₂O₆(固)の生成熱
=(黒鉛の燃焼熱+H₂Oの生成熱)-(C₆H₁₂O₆の燃焼熱)
=(393×6+287×6)-2803
=1277 kJ/mol
(これが正解です)
反応熱と生成熱の基本的な関係なので、不合格者さんでも正解してくるレベルです。しかし、本問に参加するには「問2の正解」が必要なので、問2とセットで、正解できれば他者に差をつける1問です。
- 知識:★★(やや簡単)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:完答したい1問
大問3

講師としての解説
「遷移元素」と「酸化還元」からの出題です。
知識の必要性に関して、やや簡単です。知識問題主体の大問ですが、遷移元素・酸化還元ともに基本的なものばかりです。思考力の必要性に関して、やや簡単です。問4の酸化還元反応の濃度問題が思考タイプですが、計算は簡単な部類です。
問1に関して、知識問題です。遷移元素に関する語句問題を5つ答えます。
- 周期表で3~11族に属する元素を「ア:遷移元素」といいます
- 錯イオンにおいて、金属イオンに結合した分子やイオンは「イ:配位子」です
- 錯イオンの立体構造に関して
ジアンミン銀(Ⅰ)イオンは「ウ:直線」形です
ヘキサシアニド鉄(Ⅲ)酸イオンは「エ:正八面体」形です - 鉄(Ⅱ)イオンFe²⁺を含む水溶液にヘキサシアニド鉄(Ⅲ)酸カリウム水溶液を加えると「オ:濃青」色沈殿を生じます
(ア)(イ)は基礎知識です。
(ウ)(エ)に関して、錯イオンの配位子は「金属イオンの価数の2倍」になる事が多いです。そして、錯イオンの形状は「配位子の数」によって想像できるため、丸暗記する必要はありません。
(オ)に関して、ヘキサシアニド鉄(Ⅲ)酸カリウム水溶液による濃青色沈殿は定番問題です。
(ア)(イ)(ウ)(オ)は不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
(エ)は合格者さんでも一定数が不正解になるレベルなので、正解できれば他者に差をつける1問です。
問2に関して、知識問題です。原子番号26・鉄の電子殻に含まれる電子の数を、K~N殻まで階層ごとに答えます。
ポイントは「電子の入り方のルール」です。
- まず、原子番号20番・カルシウムまでは「ルール通りに」内側から電子が入ります。よって、カルシウム原子の電子配置は以下のとおりです。
K殻:2個
L殻:8個
M殻:8個
N殻:2個 - ここから先(Sc、Ti、V、Cr、Mn、Fe、Co・・・)が遷移元素で、ルールを無視して「基本的にM殻」に電子が入ります
- そして、CuとCr(ゴロ合わせ:ドクロ)は更に例外があって「N殻の電子をM殻に」引っ張り込みます(そして次の元素でN殻の電子は2個に回復します)
- 以上より、正解の「鉄の電子殻に含まれる電子配置」は以下のとおりです
K殻:2個
L殻:8個
M殻:14個
N殻:2個
合格者さんでも一定数の不正解者が出るレベルです。よって、正解できれば他者に差をつける1問です。
問3に関して、知識問題です。「過剰アンモニア」による沈殿・錯イオンを答えます。
ポイントは「ゴロ合わせ:安藤銀さん」です。
- アンモニアは水に解けてOH⁻を放出するため、概ねの金属(アルカリ金属・アルカリ土類金属以外)は水酸化物となって沈殿します
- しかし、アンモニアが「過剰」になるとZn、Cu、Ag(ゴロ合わせ:安藤銀さん)は沈殿がもう1度溶け、錯イオンとなります
- よって、正解は
沈殿に含まれる金属イオン:Fe³⁺とAl³⁺
錯イオン:[Cu(NH3)4]²⁺
読み:テトラアンミン銅イオン
不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、思考問題です。酸化還元反応に用いた過マンガン酸カリウム水溶液の濃度を答えます。
ポイントは「半反応式の作り方」です。
【半反応式の作り方】
- 酸化還元反応の前後の物質を憶える(ここは暗記してください)
- H₂Oを使って酸化還元反応式の両辺の「O原子の数」を合わせる
- H⁺を使って両辺の「水素原子の数」を合わせる
- 最後に電子eを使って両辺の「電気的バランス」をとる
上記の手順で本問は
- MnO₄⁻ + 8H⁺ + 5e⁻ → Mn²⁺ + 4H₂O
Fe²⁺ → Fe³⁺ + e⁻ - 求める濃度をxmol/Lとして
「受け取ったe⁻=放出したe⁻」より
x× 100/1000 × 5=0.100 × 50.0/1000 × 1
∴ x=1.00×10⁻²(mol/L)
(これが正解です)
半反応式からの濃度計算なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★★(やや簡単)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:問2以外は完答したい
大問4

講師としての解説
「構造決定」からの出題です。
知識の必要性に関して、普通程度です。本問は全体的に思考問題ですが、思考を支える基礎知識が必要です。また、小問4のフェノール樹脂の種類がやや細かい知識です。思考力の必要性に関して、強く必要です。九大で頻出の「構造決定問題」の中でも、出発点となる化合物(本問ではE)を見つけにくいです。
問1に関して、思考問題です。化合物A・B・C・D・F・Gの中から
- ⅰ:臭素を脱色したものを選べ
- ⅱ:臭素と反応して白色沈殿を生じたものを選べ
という問題なので、構造決定を進めてA~Gを確定させましょう。
- 元素分析より
C:308×12/44=84(mg)
H:108×2/18=12(mg)
O:96.0-(84+12)=0(mg) - C:H
=84/12:12/1
=7:12
よって、化合物Eの組成式が「C₇H₁₂」と解ります。分子式も「C₇H₁₂」だろうと思いながら、化合物Eを探します。
- 「Lの重合体は天然ゴムの主成分」より
Lは「イソプレン」で確定 - 「化合物L+エチレン=E」より
Eは「メチルヘキセン」で確定
Eを基点に、芋づる式で情報を引き出します。
- 「化合物Bの水素をメチル基で置換したものがE」より
Bは「シクロヘキセン」で確定 - よって、問1(ⅰ)「臭素を脱色した」の正解はB
続いて
- 「AおよびBに水素を付加するとC」より
Cは「ヘキサン」で確定 - よって、Aは「ベンゼン」か「ヘキサジエン」
- Aがヘキサジエンと仮定すると
臭素を脱色できてしまうので
問1(ⅰ)の正解が2つになり矛盾 - よって
Aは「ベンゼン」で確定
さらに続けます。
- 「Aの水素をメチル基で置換するとD」より
Dは「トルエン」で確定 - 「D・Eに水素を付加させると、いずれもF」より
Fは「メチルシクロヘキサン」で確定
さらに問題文を読むと
- 「Aの水素原子を-OHで置換したものがG」より
Gは「フェノール」で確定
これでA・B・C・D・F・Gがそろいました。
問1(ⅱ)「臭素と反応して白色沈殿を生じた」に関して。G「フェノール」は臭素と反応してトリブロモフェノール(白色沈殿)を生じます。よって、これが正解です。
ポイントとなる「化合物E」が見つけにくい問題でした。
合格者さんでも、一定数の不正解者が出るレベルです。
よって、正解できれば他者に差をつける1問です。
問2に関して、思考問題です。化合物Iの3つの異性体の内「最も融点が高い化合物」の構造式を答えます。
- 「Gの水素原子をメチル基で置換すると化合物I」より
Iは「クレゾール」で確定
クレゾールには「オルト、メタ、パラ」3種の異性体があるので、問2の問題文とも合致します。最も融点が高いのは、-OHと-CH3が離れているおかげで水素結合がジャマされにくい「パラクレゾール」で、これが問2の正解です。
「オルト、メタ、パラ」による融点の違いは、不合格者さんには難しく、合格者さんは正解してきます。
よって、本問自体は「合否を分ける1問」ですが、本問に参加するには問1の正解が必要です。
よって、問1とセットで、正解できれば他者に差をつける1問です。
問3に関して、思考問題です。化合物N・P・Qの構造式を答えます。
ポイントは「正解のアルファベットN・P・Q」です。正解するためにはA~Mをハッキリさせる必要がありそうです。
- 「D(トルエン)を過マンガン酸カリウムと反応させると化合物K」より
Kは「安息香酸」で確定
さらに読み進めると
- 「エチレンに水を付加させると化合物M」より
Mは「エタノール」で確定 - 「MとKの縮合反応で化合物N」より
Nは「安息香酸エチル」で確定 - 「Mを酸化すると化合物O」より
Oは「酢酸」で確定 - 「Oを脱水加熱で化合物P」より
Pは「無水酢酸」で確定 - 「PをG(フェノール)と反応させると化合物Q」より
Qは「酢酸フェニル」で確定
本問自体は不合格者さんでも正解してくるレベルですが、参加するには問1の正解が必要です。
よって、問1とセットで、正解できれば他者に差をつける1問です。
問4に関して、知識問題です。化合物Rの名称と分子量を答えます。
- 「G(フェノール)とホルムアルデヒドを反応させると柔らかい固体R」より
Rは「フェノール樹脂」で確定
フェノール樹脂には
- 常温固体の「ノボラック」
- 常温液体の「レゾール」
があり、問題文「固体R」より正解は「ノボラック」となります。
最後に分子量に関して
- ファントホッフの式(πV=nRT)より
求める分子量Mとして
2.50×10⁴×0.10=1/M ×8.31×10³×300
∴ M≒997(これが正解です)
本問自体は不合格者さんでも正解してくるレベルですが、参加するには問1の正解が必要です。
よって、問1とセットで、正解できれば他者に差をつける1問です。
受験生としての解説
出発点となる化合物Eが見つけにくいため
- 問1が解けず
- 大問丸ごと0点
という事が起きやすいです。
一方、化合物Eさえ見つけてしまえば比較的容易に完答できます。
- 知識:★★★(普通)
- 思考:★★★★(やや難しい)
- 総合:★★★★(やや難しい)
- 短評:才能で劣る学生さんにチャンス
大問5
講師としての解説
「糖類」と「合成高分子」からの出題です。
知識の必要性に関して、やや難しいです。高分子に関する基礎を中心に難しい部分まで、幅広く問われています。思考力の必要性に関して、普通程度です。知識問題が正解できない場合に、思考と勘をはたらかせて正解を導き出せる部分があります。また、問7に割合計算があります。
問1に関して、思考問題です。化合物Aの不斉炭素原子に結合するものを4つ答えます。問題文にAの分子式C3(H2O)3が書いてあるので、これから構造式を組みます。解りにくい場合はカッコを展開し「分子式C3H6O3の構造式を描け」と読み直せば解きやすくなります。不斉炭素に結合する4要素は
- -CHO
- -OH
- -H
- -CH2-OH
となります。
C原子が3個の構造式を描くだけなので、不合格者さんでも正解してきます。
よって、全ての受験生さんが正解したい問題です。
問2に関して、知識問題です。鎖状構造フルクトースの「末端の構造」を答えます。フルクトースの構造式は、九大受験生なら白紙から描ける必要があります。もし描けない場合は、問題文にフルクトースの分子式(C6H12O6)が与えられているので、ここから図1で示される構造を引き算すれば、末端構造だけが残って正解できます。
鎖状フルクトースの図が無ければ「合否を分ける1問」です。
しかし、本問は図が与えられているので、不合格者さんでも正解してきます。
よって、全ての受験生さんが正解したい問題です。
問3に関して、知識問題です。化合物F・G・H・Iの構造式を見て、マルトース。セロビオース、トレハロースを当てる問題です。
ポイントは、グルコースの「表裏」と「結合部位」です。正解は以下の通りです。
| 物質名 | 結合形態 | 正解 |
|---|---|---|
| マルトース | αグルコース・表 αグルコース・表 1-4結合 | H |
| セロビオース | βグルコース・表 βグルコース・裏 1-4結合 | G |
| トレハロース | αグルコース・表 αグルコース・表 1-1結合 | I |
- 「マルトース」は、不合格者さんでも正解してきます。
- 「セロビオース」は、不合格者さんの一定数が不正解になるレベルです。
- 「トレハロース」は、不合格者さんには難しく、合格者さんは正解してきます。
総合して、合否を分ける1問より少し簡単な問題です。
問4に関して、知識問題です。多糖に関する◯✕問題を7つ答えます。
| 問題 | 正解 | 根拠 |
|---|---|---|
| A | ✕ | デンプンはアミラーゼで加水分解されて「マルトース」になる |
| B | ✕ | アミロペクチンはらせん構造を「とる」 |
| C | ✕ | セルロースはC1原子がグリコシド結合に使われているため、還元性を「示さない」 |
| D | ◯ | デキストリンはデンプンより水に「溶けやすい」 |
| E | ✕ | グリコーゲンはヨウ素デンプン反応を「示す」 |
| F | ◯ | アミロースは「鎖状構造」 |
| G | ✕ | 溶媒のアセトンは水よりも極性が強い。よって、極性を持つ「-OH基」を3つ失ったトリアセチルセルロースは、2つしか失ってないジアセチルセルロースより極性が弱いため、アセトンに「溶けにくい」 |
問A~Fまでは不合格者さんでも正解してきます。問Gは合格者さんでも少し難しいレベルです。
よって総合的には、全ての受験生さんが正解したい問題です。
問5に関して、知識問題です。「合成高分子」に関する語句問題を3つ答えます。
- 酢酸ビニルは、ビニル基の二重結合が開いて「A:付加」重合します
- ポリ酢酸ビニルに水酸化ナトリウムを加えて「イ:けん化」するとポリビニルアルコールになります
- ポリビニルアルコールの-OH基がエーテル結合する事を「ウ:アセタール化」といいます
不合格者さんにとってはやや難しい知識、合格者さんは正解するレベルです。
よって、合否を分ける1問となります。
問6に関して、知識問題です。化合物B・D・合成繊維Eの名称、および化合物B・Cの構造式を答えます。
- 問5で既に判明しているもの
B:酢酸ビニル
D:ポリ酢酸ビニル - 「硫酸ナトリウムに流し込んでホルムアルデヒドで処理」より
E:ビニロン - 「ビニルアルコールは不安定で化合物Cに変化」より
C:アセトアルデヒド
基本知識なので、不合格者さんでも正解してきます。
よって、全ての受験生さんが正解したい問題です。
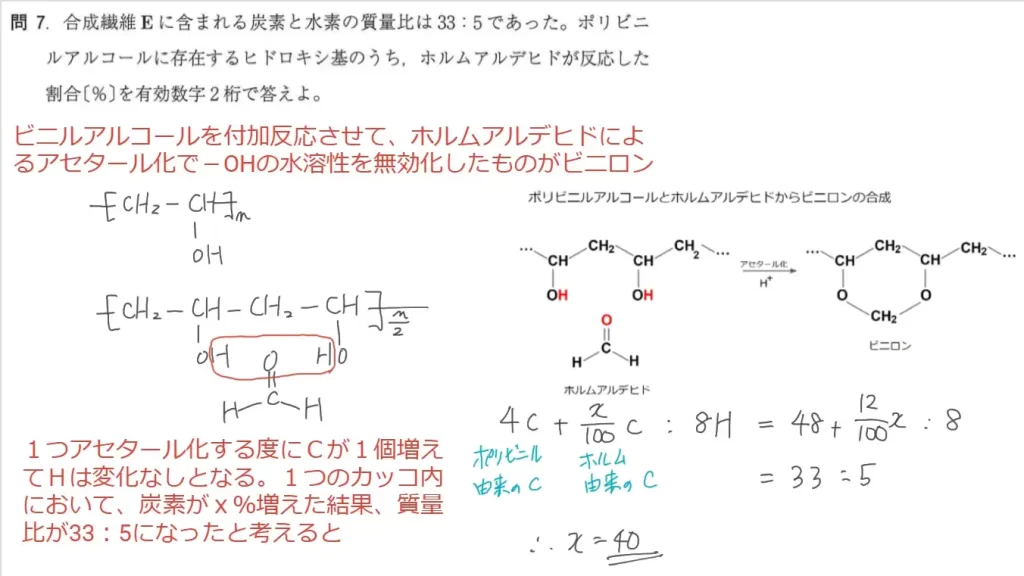
問7に関して、思考問題です。ビニロンに含まれる炭素と酸素の質量比が「33:5」である時、ポリビニルアルコールに含まれる-OH基の何%がアセタール化されたかを答えます。
アセタール化による「繰り返し単位」の変化は以下のとおりです。
- ポリビニルアルコール本体から「Hが2つ」失われる
- ホルムアルデヒドから「Hが2つ、Cが1つ」補給される
| アセタール化前 | (C₂H₄O) n個 |
| アセタール化後 | (C₄H₈O₂) n/2個 |
よって、アセタール化が1つ起きると「C1つ分」の質量が増えます。これを踏まえ「C:H=33:5」の質量比計算に持ち込みましょう。
a%がアセタール化したと仮定して
| 内容 | 数式化 | 割合 | |
|---|---|---|---|
| Cの質量 | 4C + a%C | 12×4 + 12×(a/100) | 33 |
| Hの質量 | 8H | 1×8 | 5 |
- 48+12a/100:8=33:5
- a=40
つまり「40%」が正解
難関の定番「高分子の割合計算」です。
不合格者さんには厳しく、合格者さんは正解してきます。
よって、合否を分ける1問です。
受験生としての解説
- 知識:★★★★(やや難しい)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:才能で劣る学生さんにとって逆転チャンス
九州大学の化学2022年・令和4年度
大問1
講師としての解説
「原子の構造」と「電気分解」からの出題です。
知識の必要性に関して、やや簡単です。使われている知識は基礎的なものばかりで、量も多くありません。思考力の必要性に関して、普通程度です。問4までは共通テストより簡単です。しかし、問5で陽極泥の「質量比と質量」を前面に出した結果、定番の解き方が使えず難易度が上がっています。
問1に関して、知識問題です。原子に関する語句問題を5つ答えます。
- 原子番号が同じで質量数がことなる原子を「ア:同位体」といいます
- ³Hは2個の「イ:中性子」を持ち、その原子核は放射線を出して「ウ:陽子」を2個、中性子を1個含む「エ:ヘリウム」原子の原子核に変わります。
- 解答オに関して、分子量(分子間力)の差でAの方が蒸発しやすいため「蒸気を冷却した水」に含まれるBの両は「オ:少なくなった」が正解です。
(ア)~(エ)は基本レベルなので、不合格者さんでも正解してきます。
(オ)は不合格者さんの一定数が不正解になるレベルです。
総合して、全ての受験生さんが正解したい問題です。
問2に関して、思考問題です。³Hの半減期12年を使い、48年後に原子数が「何分の1になるか」を求めます。また、水分子Cの構造を答えます。
まず、³Hの減少から
- ³Hの半減期が12年なので、48年で4回半減する
- よって
(1/2)⁴=1/16(これが正解です)
次は、水分子Cの構造です。
- 問題文「水分子Aや水分子Bとは異なる水分子C」より
¹H-¹⁶O-³H(これが正解です)
不合格者さんでも正解してきます。
よって、全ての受験生さんが正解したい問題です。
問3に関して、思考問題です。25℃の水18gを100℃の水蒸気にする「熱量」を計算します。
ポイントは「水温を上げる熱量」と「水を蒸発させる熱量」に分けることです。
- 水温を上げる熱量
=比熱×水の質量×温度上昇×10⁻³
=4.2×18×(100-25)×10⁻³…① - 水を蒸発させる熱量
=蒸発熱×水のモル数
=41×18/18…② - ①+②
≒46.6(kJ)(これが正解です)
不合格者さんでも正解してきます。
よって、全ての受験生さんが正解したい問題です。
問4に関して、思考問題です。銅の電解精錬において、粗銅板から溶出したニッケルの質量を求めます。
ポイントは「ニッケルと金の質量比、100:1」です。
- イオン化傾向より、粗銅板のAuは溶液中に溶けることなく沈殿する
- 沈殿したAu:5.87×10⁻⁴g
- 質量比
Au:Ni=100:1 - よって
溶け出したNi=5.87×10⁻²(g)
(これが正解です)
計算は簡単ですが、装置のしくみが少し複雑です。
不合格者さんには難しく、合格者さんは正解してくるレベル。
よって、合否を分ける1問です。
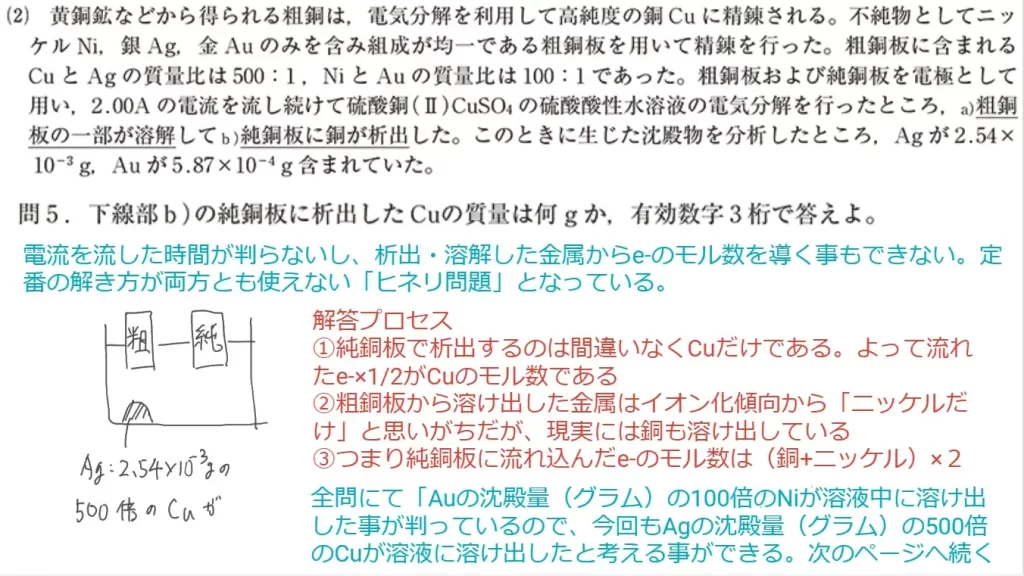
問5に関して、思考問題です。放電によって純銅板に析出したCuの質量を求めます。
ポイントは「電気分解の基本プロセス」に沿うことです。
- 極板の反応式を確認する
- 溶出した極板の質量(モル数)を確認する
- 流れたe⁻のモル数を確認する
- 析出したCuの質量(モル数)を確認する
以下、この基本プロセスで解答します。
- イオン化傾向より
純銅板で析出するのはCuである - また、イオン化傾向より
粗銅板から溶出するのはNiとCuである - 「Cu:Ag」と「Ni:Au」の質量比より
溶出したCu:2.54×10⁻³×500(g)…①
溶出したNi:5.87×10⁻⁴×100(g)…② - ゆえに溶出したモル数は
Cu:①×1/63.5…③
Ni:②×1/58.7…④ - ③④より、流れたe⁻のモル数は
③×2+④×2
=0.042(mol)…⑤ - よって、析出したCuの質量は
⑤×1/2×63.5
=1.3335
≒1.33(g)(これが正解です)
合格者さんでも一定数が不正解になるレベルです。
よって、正解できれば他者に差をつける1問です。
問6に関して、思考問題です。問5の「電気分解に要した時間」を答えます。
ポイントは「求める時間をtとおく」ことです。時間tを設定することで、方程式を立てられます。
- 流れたe⁻のモル数は問5⑤なので
(2.00×t)/96500=0.042
∴ t=2026.5≒2.03×10³(秒)
(これが正解です)
「電流×時間=電気量」を計算するだけなので、不合格者さんでも正解してきます。
しかし、本問に参加するには「問5のe⁻のモル数」が必要です。
よって、問5とセットで、正解できれば他者に差をつける1問です。
受験生としての解説
問1に関して、(ア)~(エ)は共通テストレベルなので、全ての受験生さんが正解したい問題です。(オ)はやや複雑ですが、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、半減期の計算は不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
問3に関して、水の比熱・蒸発熱は不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、一見すると難しそうですが、よく読むとニッケルと金の質量比の問題なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問5に関して、電流を流した時間が解らず、粗銅板の溶解量も応用が利かせてあるため、定番の解き方が使えません。合格者さんでも難しいレベルなので、正解できれば他者に差をつける1問となります。
問6に関して、不合格者さんでも正解してくるレベルですが、本問に参加するためには問5の正解が必要となります。よって、問5とセットで、正解できれば他者に差をつける1問となります。
- 知識:★★(やや簡単)
- 思考:★★★(普通)
- 総合:★★(やや簡単)
- 短評:問5の不正解は仕方ないが問6もセットなので痛い
大問2

講師としての解説
「化学平衡」からの出題です。
知識の必要性に関して、やや簡単です。化学平衡の基礎知識、ルシャトリエの原理、圧平衡定数など、頻出の知識で正解できます。思考力の必要性に関して、やや簡単です。問3・問4がややパズル的ですが、仕組みは簡単です。
問1に関して、思考問題です。圧力P₁とP₃の大小関係を求めます。
ポイントは「同じ温度で比較する」ことです。PV=nRTにおいて
- V:一定(問題文より)
- R:一定(気体定数)
- T:一定(同じ温度で比較)
とできれば、「Pとn」の比例関係に持ち込めます。
- グラフの1100Kの縦ラインで比較すると
気体Cの割合は
P₁>P₃
となっている - 与式①とルシャトリエの原理より
圧力が高いほど、平衡が右に移ってCの割合が増えるので
圧力の関係は
P₁>P₃(これが正解です)
不合格者さんでも正解してきます。
よって、全ての受験生さんが正解したい問題です。
問2に関して、思考問題です。与式の右向き反応が発熱か吸熱かを答えます。
ポイントは「温度を上げるほど、Cの割合が増えたか減ったか」を見ることです。
- グラフより
温度を上げるほどCの割合は減る - つまり
温度をあげるほど、平衡は左に移る - よって
式①は発熱反応(これが正解です)
不合格者さんでも正解してきます。
よって、全ての受験生さんが正解したい問題です。
問3に関して、思考問題です。温度を上げると与式①の「圧平衡定数が増えるか減るか」を答えます。
ポイントは「問2の正解が『発熱反応』である」ことです。
- 問2の結果より
式①は「発熱反応」なので
温度を上げるほど式①は左に移る - 圧平衡定数Kp=右辺/左辺より
左辺が増えて、右辺が減れば
Kpの値は「小さくなる」
(これが正解です)
不合格者さんでも正解してきます。
よって、全ての受験生さんが正解したい問題です。
問4に関して、思考問題です。問題文の条件から圧平衡定数を計算します。
ポイントは「A・B・Cの物質量はすべて同じ」という文言です。つまり「A・B・Cの分圧が全て等しい」と言い換えることができます。
- PV=nRTにおいて
本問はV・T・Rが一定なので
Pとnが比例関係である - 問題文「A・B・Cの物質量はすべて同じ」より
A・B・Cの分圧も等しいことがわかる - よって
圧平衡定数Kp=右辺/左辺
=(1.0×10⁵)/(1.0×10⁵)²
=1.0×10⁻⁵(Pa⁻¹)
(これが正解です)
やや応用を利かせていますが、不合格者さんでも正解してくるレベルです。
よって、全ての受験生さんが正解したい問題です。
ため各分圧が判り「圧平衡定数=右辺/左辺」で正解となります。
問5に関して、思考問題です。気体Cのモル分率が0.20という条件を利用し「気体の全圧」を答える問題です。
ポイントは「増減表を書くこと」です。
| A | +B | ↔C | |
| 前 | 4.0モル | 2.0 | 0 |
| 中 | -x | -x | +x |
| 後 | 4.0-x | 2.0-x | x |
増減表を描けば全貌が見え、次に打つ手が自然と解ります。
- Cのモル分率が0.20より
x/(6.0-x)=0.20
∴ x=1.0 - ゆえに、平衡状態における各モル数は
A:3.0モル
B:1.0
C:1.0 - 求める全圧をPとおくと各気体の分圧は
A:3/5・P
B:1/5・P
C:1/5・P - Kp=1.0×10⁻⁵より
Kp=右辺/左辺
=(P/5)/(3P/5・P/5)
=1.0×10⁻⁵
∴ P≒1.7×10⁵(Pa)
(これが正解です)
増減表を書けば正解できる問題ですが、不合格者さんには難しいです。
合格者さんは乗り越えてくるので、合否を分ける1問です。
- 知識:★★(やや簡単)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:完答したい1問
大問3

講師としての解説
「塩素化合物」と「電離平衡」からの出題です。
知識の必要性に関して、やや簡単です。「枝葉の分野」である塩素化合物まで勉強を行き届かせる事は難しいですが、知識を使わず思考で正解できる出題でした。思考力の必要性に関して、普通程度です。小問4・小問5ともに少し仕掛けが施してありますが、化学平衡の基礎が身についていれば試験現場で気がつけるレベルです。
問1に関して、知識問題です。NaClOにおける「Clの酸化数」を答えます。
| NaClO | 酸化数 |
|---|---|
| O | -2 |
| Na | +1 |
| NaClO全体 | ±0 |
| ゆえにClは | +1 (これが正解です) |
不合格者さんでも正解してきます。
よって、全ての受験生さんが正解したい問題です。
問2に関して、思考問題です。以下に示す反応式の「係数a・b・cと生成物X」を答えます。
- Ca(ClO)₂・2H₂O+aHCl → X+bH₂O+cCl₂↑
さらし粉に塩酸を加えて塩素が発生する有名式です。
| 正解 | |
|---|---|
| a | 4 |
| b | 4 |
| c | 2 |
| X | CaCl₂ |
「さらし粉+塩酸」の式は必須知識ですが、不合格者さんの多くは書けません。
合格者さんは書けるので、本来は「合否を分ける1問」です。
しかし、本問は「穴埋め形式」なので、逆算でツジツマを合わせれば不合格者さんでも正解できます。
よって、全ての受験生さんが正解したい問題です。
問3に関して、思考問題です。塩素系洗浄剤と塩酸系洗浄剤を混ぜた時に発生する「塩素の体積」を答えます。
- 問2を応用すると、反応式は以下の様になる
NaClO + 2HCl → NaCl + H2O + Cl2 - ゆえに反応比率は
NaClO : HCl =1:2 - 今、両者の物質量は
NaClO:100×7.45/100×1/74.5=0.100モル
HCl:100×10.0/100×1/36.5≒0.273モル - よって、先に原料が尽きて
化学反応を終了させてしまうのは
NaClOとわかる - 反応式より
NaClO:Cl₂=1:1
なので
NaClOのモル数(0.100モル)が
発生するCl₂のモル数となる - よって「PV=nRT」より
V=nRT/P
=(0.100×8.3×10³×300)/1.0×10⁵
≒2.5リットル
(これが正解です)
やや複雑になってきたので、不合格者さんには難しいレベルです。
合格者さんは正解してくるので、合否を分ける1問です。
問4に関して、思考問題です。リン酸二水素ナトリウムを水に溶かした際の「pH」を答えます。
ポイントは「増減表」です。
- 初期濃度c(mol/L)
電離度α
とすると
| H₂PO₄⁻ | ↔ H⁺ | + HPO₄²⁻ | |
| 前 | c(mol/L) | 0 | 0 |
| 中 | -cα | +cα | +cα |
| 後 | c(1-α) | cα | cα |
- 電離定数をKとして
K=右辺/左辺
=cα²/(1-α)…①
=6.3×10⁻⁸ - c=0.10(mol/L)なので
α²/(1-α)=6.3×10⁻⁷
∴ α²+6.3×10⁻⁷α-6.3×10⁻⁷=0 - 解の公式より
α={-6.3×10⁻⁷±√(省略)}/2<0.05 - よって、1-α≒1と近似できるため
①より
cα²=K
∴[H⁺]=√(cK)
=10⁻⁵√63 - よって
pH=-log₁₀[H⁺]
=4.1(これが正解です)
九大化学の「定番の流れ」ですが、不合格者さんには厳しいレベルです。
合格者さんは正解してくるので、合否を分ける1問です。
問5に関して、思考問題です。リン酸二水素ナトリウム水溶液に水酸化ナトリウム水溶液を加えた際の「pH」を答えます。
ポイントは以下3点です。
- 増減表を描く
- リン酸二水素の平衡を考えればよいため、水酸化ナトリウムは無視できる
- 「温度一定」より、平衡定数は6.3×10^-8のまま
| H₂PO₄⁻ | ↔ H⁺ | + HPO₄²⁻ | |
| 後 | x(mol/L) | a | x |
- 平衡状態における
H₂PO₄⁻の濃度をx
H⁺の濃度をa
とおくと、増減表は上の様になる - 温度は25℃のままなので
平衡定数も変化しないため
K=右辺/左辺
=ax/x
=a
=6.3×10⁻⁸ - よって
pH=-log₁₀[H⁺]
=7.2(これが正解です)
NaOHと0.10mol/Lが引っかけになっています。
これを回避できるのは、正確な基礎を身に着けた学生さんです。
よって、合否を分ける1問です。
受験生としての解説
問1に関して、酸化数のルール確認問題なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、生成物XにCaが入る事は明らかなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、塩素系の応用問題なので不合格者さんには厳しいレベル、合格者さんでも不正解の人は少なくないでしょう。よって、非医歯薬系の合格ラインより1段上の問題です。
問4に関して、九大化学の「定番の流れ」ですが、定番とはいえ1度身につけるまでが難しいので、不合格者さんには厳しいレベルです。逆に、合格者さんはキチンと身につけてくる流れです。よって、合否を分ける1問です。
問5に関して、NaOHの存在と0.10モル/Lという数値が引っ掛け問題になっています。これを回避できるのは、正確な基礎を身に着けた学生さんだけです。よって、合否を分ける1問となります。
- 知識:★★(やや簡単)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:小問3の不正解は仕方ない
大問4
講師としての解説
「構造決定」からの出題です。
知識の必要性に関して、やや難しいです。全体的に「脂肪族」と「芳香族」の基礎知識で解答できます。しかし、基本とはいえ「クメン法」を思い出せずに行き詰まる九大受験生さんは多く、ここが少し難しいです。思考力の必要性に関して、やや難しいです。九大の頻出分野なので、サラリと解けないように作られています。
問1に関して、思考問題です。化合物Aの分子式を答えます。
まずは「元素分析」です。
- C:74.8×12/44=20.4…①
H:18.0×2/18=2.0…②
O:28.8-(①+②)=6.4…③ - C:H:O
=①/12:②/1:③/16
=17:20:4 - よって、組成式は
C₁₇H₂₀O₄
であり、問題文の「分子量288」より
分子式も
C₁₇H₂₀O₄(これが正解です)
となる
元素分析なので、不合格者さんでも正解してきます。
よって、全ての受験生さんが正解したい問題です。
問2に関して、思考問題です。化合物C・D・G・H・Iの名称を答えます。
- まず、問題文のヒント(2)「水酸化ナトリウムを加えて加水分解」より「化合物Aはエステル」と予想できます
- 続いてヒント(3)「塩化鉄Ⅲ水溶液を加えたところ、Cのみ呈色」より、Cだけがフェノール類(B・Dはフェノール類ではない)と判ります
- 続いてヒント(4)「Bに水素を付加するとシス体である化合物E」より「Bは三重結合を持つ、Eはシス体」と判ります
- さらに「Eに水素を付加させると化合物F」より「Fは一重結合」と判ります。
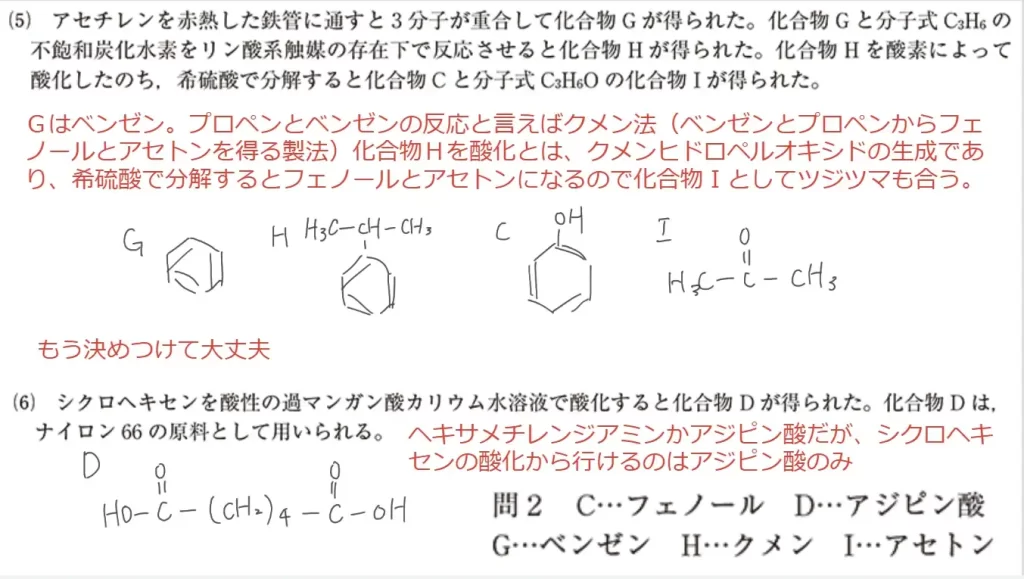
- ヒント(5)「アセチレンが3重結合して化合物G」より「Gがベンゼン」で確定します。
- 「GとC₃H₆を反応させると化合物H」より「Hは高確率でクメン」と想像できます。
なかなか正解に繋がりませんが、頑張って読み進めて行きましょう。
- 同じくヒント(5)より「Hを酸化した後、分解すると、化合物Cと化合物I(C3H6O)が得られた」より、Hは「クメン」、Iは「アセトン」
- よって、残った化合物Cは「フェノール」
と、一気につながります。ヒント(3)「Cだけがフェノール類」にも合致します。残りは「化合物D」です、読み進めていきましょう。
- ヒント(6)「化合物Dはナイロン66の原料」「Dはシクロヘキセンの酸化で得られる」よりDは「アジピン酸」で確定です。
構造決定問題のメイン部分なので不合格者さんには厳しく、合格者さんは正解してきます。
よって、合否を分ける1問です。
問4に関して、思考問題です。問3の前に問4の正解が出るので、先に解きます。化合物Fの構造異性体の中で「ヒドロキシ基を持つものの個数」を答えます。
ヒント(4)より
- 化合物Bに水素を2mol付加したものがF
と判っています。よって「Bの形」が判れば「Fの形」が判るので、Bを求めにいきます。
- ヒント(2)より
B+C+D-水2分子=A - A・C・Dの分子式は判明しているので
B=A-C-D+水2分子
=C5H8O - 上記から解る化合物Bの特徴は
1.三重結合を持つ
2.分子式がC₅H₈O
3.水素を1分子付加するとシス型になる - 上記3点を満たす物質は1つなので
Bは「CH₃C≡CH(CH₃)OH」で確定 - よって
水素を2分子付加したFの示性式は
「C₅H₁₁OH」で確定 - よって、構造異性体は「8種類」
(これが正解です)
合格者さんでもやや難しいレベルです。
よって、正解できれば他者に差をつける1問です。
問3に関して、思考問題です。化合物AとEの構造式を答えます。問4を先に解きBを確定させたので、Aの材料(B・C・D)は既にそろっています。
- D「アジピン酸」を中央に置く
- BとDをエステル結合させる
- CとDをエステル結合させる
- 以上で正解です
化合物Eに関して、ヒント(4)「Bに水素1分子を付加したものがE」より、「Bの3重結合にH₂を1つ付加したもの」が正解です。
本問自体は簡単です。
しかし、参加するには問4の正解が必要です。
よって、問4とセットで、正解できれば他者に差をつける1問です。
問5に関して、知識問題です。化合物B・C・Dを酸性の強い順に並べます。
ポイントは「酸としての強さ」です。強い順に以下の様になります。
- 硝酸・硫酸・塩酸・スルホン酸
- カルボン酸
- 過酸化水素
- フェノール(最弱)
- (アルコールは酸ではない)
| 種類 | 酸の強さ | |
|---|---|---|
| B | アルコール | 無力 |
| C | フェノール | 最弱 |
| D | カルボン酸 | 中程度 |
よって「D > C > B」が正解となります。
本問自体は簡単です。
しかし、参加するには問2・問3の正解が必要です。
よって、問2・問3とセットで、正解できれば他者に差をつける1問です。
受験生としての解説
- 知識:★★★★(やや難しい)
- 思考:★★★★(やや難しい)
- 総合:★★★★(やや難しい)
- 短評:小問2が合否の分かれ目
大問5

講師としての解説
「アミノ酸」からの出題です。
知識の必要性に関して、普通程度です。アミノ酸に関する基本知識が必要です。思考力の必要性に関して、やや難しいです。問題文で与えられた定義を理解し、その場で応用するタイプの出題です。
問1に関して、思考問題です。化合物Cの構造式を答えます。実験2「アミノ酸Bとメタノールと濃硫酸を加えて加熱したところ分子量が28増えた」より、「-COOHとCH3OHの間で脱水縮合が起き、結果として分子量が+14される事が2回起きている」と予測が立ちます。この予測に合致する物質(-COOHを2つ持つ物質)は問題中では「アスパラギン酸」だけなので、Bは「アスパラギン酸」と判ります。よって、化合物Cはアスパラギン酸の「-COOH」2つを「-COOCH3」に変えたものとなります。
問2に関して、実験5で生じたアミノ酸Gの名称を答えます。いきなり実験5に飛ぶのは危険なので、実験3から追っていきます。実験3「芳香族アミノ酸のペプチド結合を特異的に切る」「切るとD・E・Fが出る」という内容より、D・E・Fの内、いずれか2つのC末端が「フェニルアラニン」と判ります。なぜなら、問題中の芳香族アミノ酸はフェニルアラニンだけだからです。続いて実験4に関して、文章そのままで「D・Fはアミノ酸3つで構成、Eはアミノ酸2つで構成」されている事が判ります。続いて実験5に関して、「ペプチドEの組成式はC10H20N2O3」「Eを加水分解するとGのみが得られた」という内容より
- E=G×2-水(Eはジペプチドなので)
- G=(E+水)÷2=(C10H20N2O3+H2O)÷2=C5H11NO2
- よってGは「バリン」で確定
- また、EのC末端がフェニルアラニンではないため、D・FのC末端がフェニルアラニンで確定
と判り、問2の正解は「バリン」となります。
問3に関して、思考問題です。ペプチドDを構成するアミノ酸3つを答えます。問2の結果より、C末端がフェニルアラニンと判明しています。実験6の文章そのままから「Dの構成要素の1つはB(アスパラギン酸)である」と判ります。実験7「Dの構成要素Hが電気泳動で陰極側に移動した」という内容より「Dの構成要素の1つはリシン(塩基性アミノ酸)である」と確定します。これでDの構成要素3つ(アスパラギン酸 → リシン → フェニルアラニン、並び順は実験1より)が出揃い、問3の正解となります。
問4に関して、思考問題です。実験3でペプチドAが切断される際の「ペプチド結合の切断場所」を答えます。ペプチドD・E・Fの姿をハッキリさせる必要がありそうです(Dは既に判明)実験8「Fを部分的に切ると2種類のジペプチドが得られ、いずれも不斉炭素を持たないアミノ酸が含まれていた」という内容より、「Fを構成する3つのアミノ酸の、真ん中はグリシン」で確定です。これで残るは「Fの左側」だけとなり、ここまで登場しなかった「システイン」で確定します。よって
- D:アスパラギン酸 → リシン → フェニルアラニン
- E:バリン → バリン
- F:システイン → グリシン → フェニルアラニン
- ペプチドA:D → F → E
となるため、切断場所は「3番と6番」が正解となります。
問5に関して、思考問題です。ペプチドAを構成する「アミノ酸8個の並び順」を答えます。総まとめの1問となります。実は上記・問4で正解が出ています。正解は「アスパラギン酸→リシン→フェニルアラニン→システイン→グリシン→フェニルアラニン→バリン→バリン」です(解答用紙には、アリフシグフババと記入)
受験生としての解説
問1に関して、「分子量が28増えた」という情報だけで「HとCH3の入れ替えが2回起きた」と見抜く事は、合格者さんでも簡単ではありません。よって、合否を分ける1問です。
問2に関して、決して難しい問題ではありませんが、短い試験時間を考えると不合格者さんには厳しいです。よって、合否を分ける1問です。
問3に関して、合格者さんでもそろそろ厳しくなってくる頃です。よって、非医歯薬系の合格ラインより1段上の問題です。
問4に関して、合格者さんでもそろそろ厳しいです。よって、非医歯薬系の合格ラインより1段上の問題です。
問5に関して、総まとめ付け足しの1問なので、問4まで正解できた人へのボーナス点となります。
- 知識:★★★(普通)
- 思考:★★★★(やや難しい)
- 総合:★★★★(やや難しい)
- 短評:パズル問題
九州大学の化学2021年・令和3年度
大問1

講師としての解説
「化学平衡」からの出題です。
知識の必要性に関して、普通程度です。化学平衡に関する知識が必要です。特に「平衡定数は温度によってのみ変化する」という部分が重要です。思考力の必要性に関して、やや難しいです。四酸化二窒素と二酸化窒素の定番シチュエーション、アルゴンを加えた応用シチュエーションと、平衡に関するバラエティに富んだ出題となっています。
問1に関して、知識問題です。ルシャトリエの原理に関する基本知識を問う出題です。
問2に関して、思考問題です。ルシャトリエの原理をベースに、グラフの動きを予測します。条件ⅰに関して、温度を上げれば反応速度が上がるためグラフは急カーブを描きます。しかし、与式よりこの反応は「発熱反応」なので、温度を上げると平衡は逆向きに傾いてしまい、結果としてアンモニアの生成量は減ります。それを表したグラフはAで、これが正解となります。条件ⅱも同じ考え方で、グラフCが正解となります。条件ⅲに関して、触媒は反応速度を早めますが反応の結果には影響しないので、それを表したグラフEが正解となります。
問3に関して、思考問題です。窒素ガスと水素ガスの平衡状態における割合を考え、変化した窒素ガスの割合を答えます。投入された窒素と水素の物質量が1:3なので、xモル・3xモルと置いて増減表を作ります。平衡移動によって窒素がyモル減ったと考えると増減表が完成してx/yが求まり、正解となります。
問4に関して、思考問題です。四酸化二窒素と二酸化窒素の混合気体と空気を封入・加熱し、平衡になった時の状態を正しく記述したものを5択から選びます。まず、気体を加熱しているため、窒素側・空気側とも体積が増加します。その後、ルシャトリエの原理より、窒素混合気体は平衡が与式右向きに移動するため(与式は吸熱反応)体積が更に増えます。これを記述した選択肢Cが正解となります。
問5に関して、思考問題です。二酸化窒素と四酸化二窒素の平衡状態における「圧平衡定数」を答えます。解離度が与えられているため平衡時の両気体のモル数がわかり、モル数によって分圧がわかるため、両気体の圧力がわかります。よって、圧平衡定数の式に代入して正解となります。
問6に関して、思考問題です。二酸化窒素と四酸化二窒素の混合気体が平衡であるところにアルゴンを投入し、アルゴンを含む新たな平衡状態になった時の「四酸化二窒素の解離度」を答えます。まず、アルゴンを投入されてない状態における平衡定数Kを求めます。次に、アルゴンを投入した状態における平衡定数K’を求めます。ここで問題文を読むと「温度は常に一定」と書いてあるので、実はK=K’である事がわかります(平衡定数は温度によってのみ変わる)よって、この式を解いていくと、xをαとβで表すことができ、これが正解となります。
受験生としての解説
問1に関して、ルシャトリエの原理は不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
問2に関して、ルシャトリエの原理の応用なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、合格者さんは正解でき不合格者さんには厳しいレベルなので、合否を分ける1問です。
問4に関して、やや難しいシチュエーションですが、本質はルシャトリエの原理を使っているだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい1問です。
問5に関して、解離度→モル数→分圧→圧平衡定数と素直な流れなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問6に関して、複雑なシチュエーションで難しいです。正解できれば他者に差をつけられる1問です。「医学科の合否を分ける問題」とみなして見切ってもよいです。
- 知識:★★★(普通)
- 思考:★★★★(やや難しい)
- 総合:★★★(普通)
- 短評:問6は不正解でもよい
大問2

講師としての解説
「14族元素」からの出題です。
知識の必要性に関して、普通程度です。あまりメジャーではない分野から、正確な基礎知識を問われています。思考力の必要性に関して、普通程度です。簡単な計算ですが、試験時間の短さを考慮すると普通程度の難しさになります。
問1に関して、知識問題です。14族元素に関する語句問題です。(イ)の正解「グラフェン」がやや難しいです。(ウ)「水ガラス」(エ)「シリカゲル」は問題集を解いていれば自然と憶えてしまう物質です。
問2に関して、思考問題です。リチウムイオン電池・負極の重量変化から「流れた電子の物質量」を答える問題です。問題文の与式より、リチウムと電子の物質量の比が「1:1」と解ります。よって「6.94g:1モル=3.82g:xモル」の式が立ち、これを解くと正解となります。
問3に関して、思考問題です。二酸化ケイ素の還元式を書き、その過程で発生した有毒気体の体積を答えます。「二酸化ケイ素の還元」という事で、受験生さんにとって馴染みの薄い式ですが、問題文に言われた通りすれば暗記は不要です。
- 二酸化ケイ素を炉中で融解し:溶かすだけなので化学式は無い
- 炭素を用いて還元する:還元する(酸素を奪う)式を立てる
(SiO2 + 2C → Si + 2CO) - 無色無臭の有毒な気体が発生する:↑COは無色無臭で有毒
後はモル数を計算して22.4リットル/molをかければ正解です。
問4に関して、思考問題です。ケイ素単体の単位格子の図を参考に、二酸化ケイ素の単位格子に含まれる「全ての原子数」を答えます。まず、注意が必要な点は「図に示されたボールは全てケイ素である」ことです。普通、この様な(二種類の色で)表示をされた場合、一方が酸素でもう一方がケイ素ですが、本問は全てのボールがケイ素です。よって、酸素原子は自分で書き込むか、想像で補います。酸素原子の位置に関して、問題文に「ケイ素原子の間に酸素原子が入り込んだ構造」と書いてあるので、図の灰色で書かれた線上に酸素原子が存在していると解ります。これらを踏まえ「全ての原子数=1/8×8個+1/2×6個+4個+4本×4個=24個」が正解となります。
問5に関して、知識問題です。ガラスに関する◯✕問題を4つ答えます。問題Aに関して、教会のステンドグラスなどから明らかな様に「全てのガラスは無色」ではないため✕が正解です。問題Bに関して、非晶質の構成要素は「粒子が規則的に配列している」わけではないため✕が正解です。問題Cに関して、全てのガラスは一定の融点を示さず、ある温度の幅で軟化するため正しいです。正解は◯です。問題Dに関して、金属の非晶質は電流を流すため「全ての非晶質が電気を流さない」ことはありません。正解は✕です。
問6に関して、知識問題です。石英ガラスがフッ化水素酸に溶ける時の化学反応式を答えます。本問は「SiO2 + 6HF → H2SiF6 + 2H2O」という難関大で暗記必須の式です。しかし、生成物の「ヘキサフルオロケイ酸」という名前さえ憶えておけば、名前から式を導き出す事ができます。
【丸暗記回避】
- 石英ガラス「SiO2」とフッ化水素酸「HF」の化学式は判っている
- 生成物の「ヘキサフルオロケイ酸」という名前を憶えておく(変な名前だし、重要な式なので憶えやすい)
- ヘキサは「6」フルオロは「F」という意味なので、ヘキサフルオロケイ酸という名前から「SiF6」を導き出せる
- 電気量はSiが「+4」F6が「-6」なので、バランスを取るためにH「+1」を2個加えて「H2SiF6」がヘキサフルオロケイ酸であると導ける
- 式全体の辻つまを合わせると、右辺に2H2Oが自然と出てくるので正解となる
問7に関して、知識問題です。スズと鉛に関する◯✕問題を4つ答えます。問Aに関して、スズはいつも還元剤として登場するので「強い酸化剤である」は✕となります(半反応式から導いても良いです:Sn4+ → Sn2+)問Bに関して、ブリキの表面は「スズで覆われいる」ので◯が正解です。
【丸暗記回避】
Zn Fe Ni Sn
鉄(Fe)を挟んだ両側の「ZnとSn」が主役です(Niは高価なので鉄メッキに使わない)
鉄に「亜鉛メッキがトタン」なので、ゴロ合わせ「会えた途端」と憶えてください。
「トタンじゃない方」がブリキなので、Snはブリキです。こちらは憶えずに導き出せばよいです。
問Cに関して、鉛は硫化物イオンと反応して「白色沈殿を生成」せず黒色沈殿を生成するので✕が正解です。
【丸暗記回避】
硫化物イオンによる沈殿は「Znだけ白で、残りは全部黒」と憶えておいてください。
必ずしもそうではありませんが、ハズレて痛い目に合う事はメッタにありません。
これで個別の丸暗記を避けられるため、コスパが良いです。
問Dに関して、ゴロ合わせ「ああすんなり溶ける」より、スズも鉛も両性金属なので◯が正解です。
受験生としての解説
問1に関して、14族の語句問題は不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、電池の計算としては最も簡単な部類なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、本問の化学式は不合格者さんでも立式できます。よって、全ての受験生さんが正解したい問題です。
問4に関して、合格者さんでも難しいレベルなので、正解できれば他者に差をつけられる1問となります。
問5に関して、「ガラスの性質」に関する知識問題は、不合格者さんだと勉強が行き届きにくい部分です。合格者さんは仕組みから理解している場合が多いので、合否を分ける1問です。
問6に関して、ガラスを溶かす化学式は不合格者さんには厳しく、合格者さんは憶えているレベルです。よって、合否を分ける1問となります。
問7に関して、スズと鉛は勉強が行き届きにくい分野なので、不合格者さんには厳しく、合格者さんでも4問全て正解はやや難しいです。よって、正解できれば他者に差をつける1問となります。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:問4は不正解でもよい
大問3

講師としての解説
「高分子化合物」からの出題です。
知識の必要性に関して、普通程度です。やや込み入った知識、少し知識に応用を利かせた問題などありますが「やや難しい」という程ではありません。思考力の必要性に関して、普通程度です。普通レベルの事を素早く・幅広く求められています。
問1に関して、知識問題です。重合に関する語句問題を8つ答えます。全て基礎知識ですが(ウ)「アラミド繊維」(ク)「共重合」は少し難しいです。
問2に関して、思考問題です。問題文をヒントに、乳酸とグリコール酸のジエステルの構造式を答えます。ポイントは「脱水縮合による環状」という部分です。乳酸2分子を180°ずらして向かい合わせ、双方の-COOHと-OHからH2Oを脱水し縮合すれば環状となり正解です。グリコール酸も同様です。
問3に関して、知識問題です。Cはポリエチレンテレフタラートの主原料となる2価アルコールなので、エチレングリコールです。それを酸化したDはシュウ酸となります。シュウ酸は中和滴定の標準試薬となるため(B)が正解ですが、消去法ならもっと楽に正解できます。例えば(A)の「アセテート繊維の原料」は無水酢酸、(C)の「自動車の不凍液」はエチレングリコール(酸を使ったら危ない、でも良いです)(D)の「ナイロン66」の原料はアジピン酸です。
問4に関して、思考問題です。「2,6-ナフタレンジカルボン酸」は名前から構造式を導き出せます。それとエチレングリコールを2ヶ所で脱水縮合したものがポリエステルEなので、繰り返し単位は構造式を描くか分子式を引き算すれば求まります。繰り返し単位が求まれば、後は「平均分子量 ÷ 繰り返し単位」で繰り返し回数が求まります。正解のエステル結合の個数は「繰り返し単位×2」で求まります(内側のエステル結合、外側のエステル結合の2ヶ所)
問5に関して、知識問題です。ポリエチレンテレフタラート、ポリエチレン、ポリ塩化ビニルに関する特徴を5択から答えます。選択肢Aに関して、「非結晶部分が多く、比較的柔らかくて透明度が高い」より(低密度)ポリエチレンの記述です。選択肢Bに関して、「銅線の先につけて加熱すると、炎の色が青緑色」より「CuCl2」が存在しており、銅に「塩化物イオン」を供給できる「ポリ塩化ビニル」の記述と解ります。選択肢Cに関して、「濃塩酸と反応させると白煙」より「塩化アンモニウム」の記述と解ります。選択肢Dに関して、文章全体より「デンプン」の記述と解ります。選択肢Eに関して、「空気中で燃やすと多量のすす」より、炭素を中心にした物質と解ります。よって「ポリエチレンテレフタラート」の記述と解ります。
受験生としての解説
問1に関して、語句問題なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、180°回転させて脱水縮合するだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、4択とはいえシュウ酸の特徴を答える事は不合格者さんには難しいです。合格者さんでもやや難しいので、正解できれば他者に差をつける1問となります。
問4に関して、繰り返し単位の計算は不合格者さんでも正解してきますが、少し応用が利いているので不合格者さんには厳しいでしょう。一方、合格者さんなら応用について来るレベルです。よって、合否を分ける1問となります。
問5に関して、ただの暗記ではなく仕組みを理解しておく必要があるため、不合格者さんには厳しいです。一方、合格者さんはこの辺りがシッカリしています。よって、合否を分ける1問となります。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:小問3~小問5で1つ不正解なら十分
大問4

講師としての解説
「構造決定」からの出題です。
知識の必要性に関して、普通程度です。特に難しい知識は必要ありませんが、思考問題に参加するための幅広い基礎を求められています。思考力の必要性に関して、やや難しいです。構造決定、鏡像異性体の判定、複雑なシチュエーションでのモル計算(計算自体は簡単ですが)など複数の思考問題を解きます。
問1に関して、思考問題です。化合物A・B・Cの構造式を答えます。まず、問題文のヒント(2)より「化合物Dの組成式はC3H7」と解ります。よって、分子式は「C6H14」と解ります。これにより、化合物A・B・Cは「C6H12」と解ります。続いてヒント(3)「化合物Aをオゾン分解するとEだけが得られた」より「AはEを2個つなげた物質」と解ります。そうなると「Eは炭素原子3つ」と解ります。続いてヒント(4)「AにHClを付加させると鏡像異性体を持つ」より、Aの形は「C-C-C=C-C-C」で確定します。続いてヒント(5)より
- Bの形はF=G
- GはCH3CO-を持つ
- Gだけがヨードホルム反応を示すなら(Fがヨードホルム反応を示さないなら)Fは「CH3CHO」
- よってGは「CH3CH2CH2CHO」
と解ります。続いてヒント(6)「Cをオゾン分解すると化合物Hだけが得られた」という内容より
- Cの形は「化合物H=化合物H」
- その上でHがヨードホルム反応陽性なら、Hはアセトンだろう
解ります。
問2に関して、思考問題です。化合物D・F・Hの名称を答えます。Dに関して、ヒント(2)より
- AとBに水素を付加するとDになる
- Dの組成式はC3H7である
より、Dは「ヘキサン」と解ります。F「アセトアルデヒド」G「アセトン」に関して、問1で既に正解しています。
問3に関して、思考問題です。2つの物質が鏡像異性体の関係になるようにRa~Rcに適切な官能基を答えます。ポイントは「左側の図のRa」を真上から指でつまんで120°回す事です。そうすると右側の図とソックリ(HとClが一致、RbとRdが同じ位置)になります。この状態でRaと同じ官能基をRcに入れてしまうと、左右の物質は全く同じになってしまう(鏡像異性体ではなくなる)ため、RaとRcには異なる官能基が入ります(必然、残ったRbとRdも異なる官能基となります)この時点で正解となります。
問4に関して、思考問題です。化合物Eと化合物Eが還元反応を起こした後の物質Xについて、構造式を答えます。まず、化合物Eについて。問1の段階で「化合物Aの二重結合をオゾン分解するとEが2つ発生する」と判明しています。よって、化合物Eは「CH3CH2CHO、プロピオンアルデヒド」となります。このアルデヒド基が還元反応を起こす(自身は酸化される)ので、反応性生物Xは「CH3CH2COO-」となり正解できます。
問5に関して、思考問題です。同じ質量のE・F・G・Hを完全燃焼させた時に排出されるCO2が最も少ないものを答えます。ここまで問題を解いた流れで
- E:C2H5CHO
- F:CH3CHO
- G:C3H7CHO
- H:CH3COCH3
である事は既に判っています。よって、CO2排出量が最も少なくなるのは、C原子の数が最も少ないFとなります。F1モル(44g)を完全燃焼させるとCO2が2モル(88g)排出されるので、F10mgではCO2が20mg排出され、これが正解となります。
問6に関して、思考問題です。化合物C21.0mgをオゾン分解してアセトンにし、アセトンでヨードホルム反応を起こした時の「ヨードホルムの生成量」を答えます。まず、反応物質量の比ですが「化合物C:アセントン:ヨードホルム=1:2:2」となります。よって化合物Cの2倍の物質量のヨードホルムが得られるので「(21.0mg/84)×2×394g=1.97×10^2mg」が正解となります。
受験生としての解説
問1に関して、不合格者さんには厳しいレベルです。合格者さんは正解してくるので、合否を分ける1問です。
問2に関して、不合格者さんには厳しいレベルですが、合格者さんなら正解してきます。よって、合否を分ける1問です。
問3に関して、立体をクルクル回して鏡像異性体の位置関係を探すだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、不合格者さんでも正解してくるレベルですが、問1を解く必要がある問題です。よって、問1とセットで合否を分ける1問となります。
問5に関して、不合格さんでも正解してくるレベルですが、本問に参加するためには問1・問2の正解が必要です。よって、問1・問2とセットで、合否を分ける1問となります。
問6に関して、不合格者さんでも正解してくるレベルですが、本問に参加するためには問1の正解が必要です。よって、問1とセットで合否を分ける1問となります。
- 知識:★★★(普通)
- 思考:★★★★(やや難しい)
- 総合:★★★★(やや難しい)
- 短評:問1・問2が重要
九州大学の化学2020年・令和2年度
大問1

講師としての解説
「反応速度」と「化学平衡」からの出題です。
知識の必要性に関して、やや簡単です。各分野の最初で習う様な基本知識ばかり問われているので、確実に正解を拾いたいところです。思考力の必要性に関して、やや難しいです。九大数学で難問になる事が多い「問題文で定義を与え、その場で応用させる問題」があります。その代わり、化学平衡の問題は最も簡単な部類です。
問1に関して、知識問題です。ルシャトリエの原理に関する基礎問題です。
問2に関して、思考問題です。与式Ⅰの反応における平衡定数を求めます。「平衡」と言えば「増減表」なので増減表を書き、「平衡定数=右辺のモル濃度/左辺のモル濃度」に値を入れれば正解となります。
問3に関して、知識問題です。活性化エネルギーに関する語句問題と4択問題です。基本知識ではありますが(カ)の「活性錯体」は少し難しいです。(キ)に関して、問題文中で与えられた記号だけで考える事は難しいので、活性化エネルギーの簡略図を描いて考えると安全確実に正解できます。
問4(1)に関して、思考問題です。問題文で与えられた定義をその場で理解し、応用して答えるタイプです。対数の式変形を問題文の指示通りに行っていけば正解できます。(2)に関して、知識問題です。反応速度に関する基本知識で、温度を上げるほど分子の運動エネルギーが増えて活性化エネルギーを超えるため、化学反応が促進されます。
受験生としての解説
2020年の九大化学5問で、1番目に簡単な問題です。
問1に関して、ルシャトリエの原理を説明するだけなので、全ての受験生さんが正解したい問題です。
問2に関して、増減表を書いて平衡定数を求めるタイプでは最も簡単な部類なので、不正解の受験生さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、(キ)がやや難しいですが全体的に基本レベルなので、不合格者さんでも正解してきます。よって全ての受験生さんが正解したいレベルです。
問4に関して、(1)の式変形は難しいです。数学の式変形ほど難しくありませんが、化学で急に出されると「医学科の合否を分ける問題」と言える難度になります。よって、非医歯薬系の受験生さんは不正解でも構いません。(2)の知識問題に関して、不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
- 知識:★★(やや簡単)
- 思考:★★★★(やや難しい)
- 総合:★★★(普通)
- 短評:簡単な問題だけ確実に正解したい
大問2

講師としての解説
「電池」からの出題です。
知識の必要性に関して、やや簡単です。電池の基本知識です。思考力の必要性に関して、普通程度です。電池に関する計算問題が続きます。
問1に関して、思考問題です。与式の係数を計算し、与式を完成させます。まず、右辺のO原子数を左辺と合わせるためにy=1を代入します。すると、左辺が「w=1、x=1」で辻褄が合うため正解となります。zは左辺・右辺の電気的バランスを考えると、すぐにz=2と解り正解です。
問2に関して、知識問題です。(ア)(イ)はアルカリマンガン乾電池の負極なので[Zn(OH)4]2-で、極板はZnです。その際に発生する気体は水素で、これが(ウ)の正解です。
問3に関して、出題ミスにより全員正解となりました。
問4に関して、思考問題です。アルカリマンガン乾電池を放電した時のpHの変化を答えます。負極のZnと水溶液のOH-が反応して電流が流れるため、放電するほどOH-が減り酸性に近づきます。よって、pHは減っていきます。
問5に関して、思考問題です。アルカリマンガン乾電池を一定時間放電した時の「正極の重量変化」を答えます。与式①より、電子が1モル流れる度に「陽極が1グラム増える」ことが解ります。よって、「20mA × 16分5秒 ÷ 96500」で流れた電子量を割り出せば正解です。
問6に関して、思考問題です。268mAの電流を1時間流すために必要な材料(正極・負極)の重量を答えます。コツは「電子1モルの場合」を考える事です。与式①②より電子1モルを流すのに必要な重量はすぐ解ります。後は「268mA × 1時間 ÷ 96500」で実際に流れる電子のモル数を出せば正解できます。
受験生としての解説
2020年の九大化学5問で、3番目に簡単な問題です。
問1に関して、不合格者さんでも正解してくるレベルなので、全ての受験生さんが正解したい問題です。
問2に関して、選択問題で[Zn(OH)4]2-を記述しなくて済むため、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、出題ミスにより全員正解となりました。
問4に関して、不合格者さんだとアルカリマンガン乾電池の「負極の反応」は難しいいので、合否を分ける1問です。
問5に関して、不合格者さんでも正解できるレベルなので、全ての受験生さんが正解したい問題です。
問6に関して、合格者さんでも少し難しいかもしれないレベルなので、正解できれば他者に差をつけられる1問です。仕組みは簡単ですが、短い試験時間なので難易度は上がって、合否を分ける1問となります。
- 知識:★★(やや簡単)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:高得点を目指したい1問
大問3

講師としての解説
「ハロゲン元素」からの出題です。
知識の必要性に関して、普通程度です。ハロゲン元素に関するやや理解しにくい基礎、分子結晶に関する知識を問われています。思考力の必要性に関して、やや簡単です。後半の小問4・小問5が計算問題ですが、共通テストでおなじみの問題なので難しくありません。
問1に関して、知識問題です。ハロゲン元素に関する語句問題です。ハロゲン元素の「酸化力」とハロゲン化水素の「酸の性質」は似て非なる紛らわしい部分なので、正確な基礎知識を問われています。
問2に関して、知識問題です。ハロゲン化物の融点を決める要因を答える問題です。融点は構成要素の「結合力の強さ」で決まり、本問のハロゲン化物は「金属+非金属」の関係になっているため、イオン結合による静電気力が正解となります。
問3に関して、知識問題です。分子結晶を作る物質を7つの中からあるだけ答えます。分子結晶は「ファンデルワールス力による結晶」だけでなく「水素結合による結晶」も含まれるため、必ずしも無極性である必要はない(つまり水も分子結晶である)事がポイントです。
問4に関して、思考問題です。ヨウ素結晶の密度を答えます。ポイントは、2原子1対で書かれているヨウ素分子を難しく考えず「1つのボール」とみなす事です。そうすれば、共通テストでおなじみの問題となり、簡単な問題である事が解ります。
問5に関して、面心立方格子の原子間距離を求める問題です。面心立方格子なので、各原子は斜めのラインで接触します。立方格子1辺の√2倍の長さで「2組」の原子が並ぶので、1組辺りの原子間距離は「√2/2倍」となり、これが正解です。
受験生としての解説
2020年の九大化学5問で、2番目に簡単な問題です。
問1に関して、合格者さんはハロゲンに関する基礎知識がシッカリしており、不合格者さんは曖昧な場合が多いです。よって、合否を分ける1問です。
問2に関して、問題はやや難しめですが、不正解の選択肢A・C・Dが明らかに不正解なので、不合格者さんでも正解できるでしょう。よって、全ての受験生さんが正解したい問題です。
問3に関して、不合格者さんには全て正解する事が難しいです。よって、合否を分ける1問です。
問4に関して、不合格者さんで正解してくるレベルなので、全ての受験生さんが正解したい問題です。
問5に関して、共通テストでおなじみのやや簡単な部類の問題なので、全ての受験生さんが正解したい問題です。
- 知識:★★★(普通)
- 思考:★★(やや簡単)
- 総合:★★★(普通)
- 短評:小問4・小問5は確実に拾いたい
大問4
講師としての解説
「脂肪族」からの出題です。
知識の必要性に関して、普通程度です。本問は「構造決定」なので思考問題ですが、思考を支えるだけの基礎知識が必要です。思考力の必要性に関して、やや強く必要です。
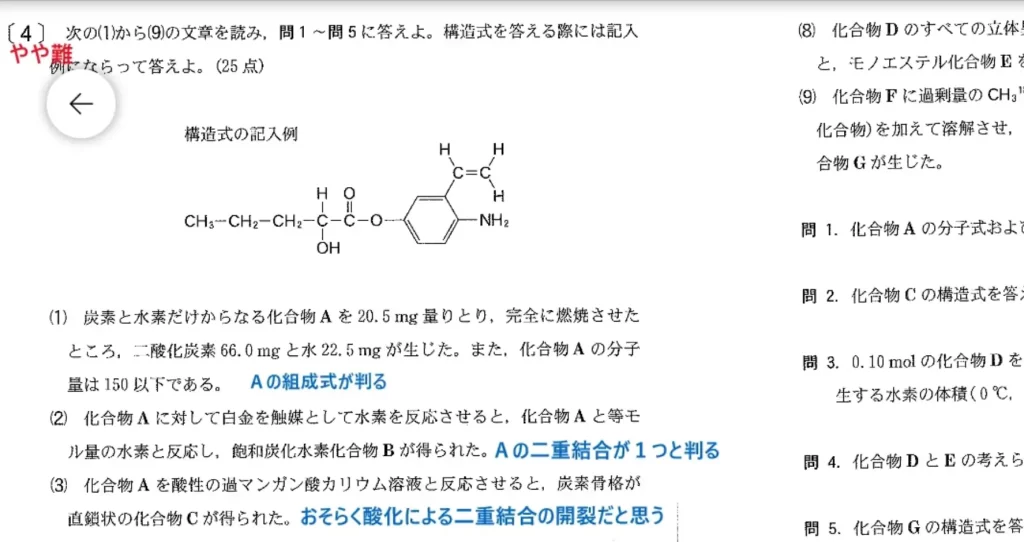
問1に関して、思考問題です。化合物Aの分子式・構造式を答えます。構造決定問題の定番「元素分析」を行うと、Aの組成式が「C3H5」と解ります。問題文に「Aの分子量は150以下」と書いてあるのでAの分子式は「C6H10」と定まります。更に問題文のヒント(2)により、Aは二重結合を1つ持っていると解るので、Aの構造式はシクロヘキセンとなり正解です。
問2に関して、思考問題です。化合物Cの構造式を答えます。化合物Aを過マンガン酸カリウムで酸化させると「直鎖状のC」が得られた、という事なので、Aの二重結合が開裂したと解ります。さらに問題文のヒント(4)の滴定により、化合物Cが「二価の酸」と解るため、Cの両脇をカルボキシ基に変えて「アジピン酸」で正解となります。
問3に関して、思考問題です。化合物Dに単体のナトリウムを加えた時のH2の発生量を答えます。まず化合物Dを確定させましょう。化合物Aを「塩基性条件下」で過マンガン酸カリウムと反応させる、と書いてあるのでAの開裂は起きず環状構造のままと解ります。その状態で、問題文のヒント(6)に「Dはジオール」と書いてあるので、単体のナトリウムとDを反応させると等モル数のH2が発生すると解り、後は計算で正解です。
問4に関して、思考問題です。化合物DとEの考えうる立体異性体(幾何異性体+光学異性体)の数を答えます。Dは既に「シクロヘキセンからのジオール」と判ってるため、不斉炭素原子の数は2であり、分子内対称性(メソ体)を考えて3個が正解となります。続いて化合物Eを確定させましょう。問題文のヒント(8)より「EはDを無水酢酸と反応させたモノエステル」と書いてあるので、Dの2つのOHの内1つがアセチル基になったものと解ります。よって、Dが分子内対称性を失ったものがEなので、光学異性体の数は4で正解となります。
問5に関して、思考問題です。化合物Gの構造式を答えます。問題文のヒント(8)(9)を読むと、D→Eの反応を更に進めOHを2つともアセチル基にしたものがFであり、Fとメタノールを反応させるとGが発生すると書いてあります。Gは「低沸点」と書いてあるので、Gは「酢酸メチル」と確定し質量数18のOもGに含まれます。
受験生としての解説
2020年の九大化学5問で、5番目に簡単な問題です。
問1に関して、シクロヘキセンを描く事は不合格者さんには少し難しいですが、正解してくるレベルではあります。よって、全ての受験生さんが正解したい問題です。
問2に関して、不合格者さんには難しく合格者さんは正解してくるレベルなので、合否を分ける1問です。
問3に関して、不合格者さんには難しく合格者さんは正解してくるレベルなので、合否を分ける1問です。
問4に関して、合格者さんでもやや難しいレベルなので、正解できれば他者に差をつけられる1問です。
問5に関して、短い試験時間の中では合格者さんでも厳しい1問です。よって、医学科の合否を分ける難問となります。
- 知識:★★★(普通)
- 思考:★★★★(やや難しい)
- 総合:★★★★(やや難しい)
- 短評:小問4まで正解したい
大問5
講師としての解説
「アミノ酸」からの出題です。
知識の必要性に関して、普通程度です。小問6以外は思考問題なので、思考のベースとなる基礎知識が必要です。問1の「フィッシャー図」を入れると「やや難しい」に難易度アップします。思考力の必要性に関して、普通程度です。問1~問5まで思考問題が続きますが、問1を除けば簡単なものばかりです。
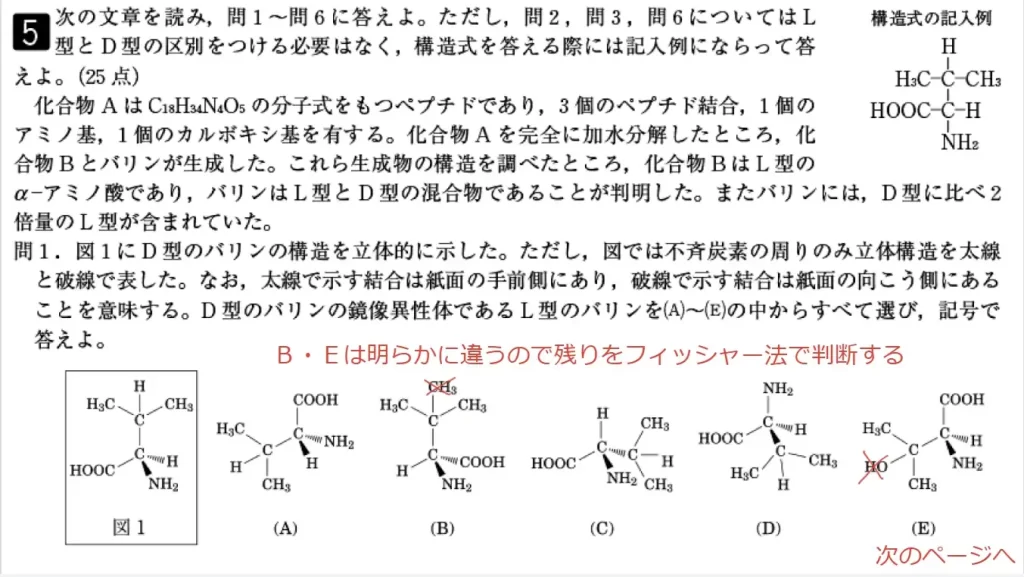
問1に関して、思考問題です。図1で示されたD型バリンと鏡像異性体の関係にあるものを、A~Eから全て選びます。まず、BとEですが、図1とは官能基の種類が違うため明らかに別の物質です。残りのA・C・Dは図1と同じ官能基を持つため、フィッシャー投影法を使って判定していきます。まずAですが、フィッシャー図を180°回転させると図1になるので、全く同じものです。次にCですが、官能基1ヶ所を固定して残り3つを順送りしても図1と一致する事はありません。よって、鏡像異性体となり正解です。最後にDですが、官能基1ヶ所を固定して残り3つを順送りするとCと一致します。よって、DとCは同じ物質であり、Dも正解となります。
問2に関して、思考問題です。アミノ酸Bの種類を答えます。問題文より化合物Aの構成要素は
- 化合物B
- D型バリン
- L型バリン2個
と、読み取れます。よって「化合物B=化合物A+3H2O-バリン×3=C3H7NO2」となり、正解はアラニンと判ります。
問3に関して、思考問題です。問2で求めた化合物Bと同じ分子式で、不斉炭素原子を持つ物質の構造式を答えます。化合物Bがアラニンなので「-NH2」の位置をずらして不斉炭素原子を発生させた「βアラニン」が正解となります。
問4に関して、思考問題です。化合物A772mgから生成できるL型バリンのmg数を答えます。よって「化合物A:L型バリン=386:117×2=772:x」という比の式が立ち、これを解くと「x=468mg」で正解となります。
問5に関して、思考問題です。化合物Aのアミノ酸配列の種類を答えます。化合物Aは「アラニン、D型バリン、L型バリン2個」で構成されている事が問2より判っています。今、D型・L型バリンの並べ方3通りに対し(DLL、LDL、LLD)それらの両脇およびスキマにアラニンを入れる方法は4通りあるため、3×4=12通りが正解となります。
問6に関して、知識問題です。問2で示されたアミノ酸の中で、不斉炭素原子を持たないものを答えます。アミノ酸の中で不斉炭素原子を持たない唯一の物質はグリシンなので、即答で正解となります。
受験生としての解説
2020年の九大化学5問で、4番目に簡単な問題です。
問1に関して、フィッシャー図は合格者さんでも使えない人は多いので、正解できれば他者に差をつける1問です。
問2に関して、簡単な引き算なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、問2の正解をほんの1か所動かすだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、難しい計算ではありませんが、短い試験時間を考えると不合格者さんには正解しにくい問題です。よって、合否を分ける1問です。
問5に関して、数学の「場合の数・確率」の共通テストレベルなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問6に関して、「不斉炭素を持たないアミノ酸=グリシン」で何度も見かけるため、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:問1が無ければ「★★やや簡単」な大問
九州大学の化学2019年・平成31年度
大問1
講師としての解説
「浸透圧」からの出題です。
知識の必要性に関して、やや難しいです。「浸透圧」と「凝固点降下」という受験化学の主流ではない分野からの出題です。思考の必要性に関して、やや難しいです。公式に数値を当てはめるだけの問題ではなく、水柱の高さ・重りの圧力など交えた応用問題です。
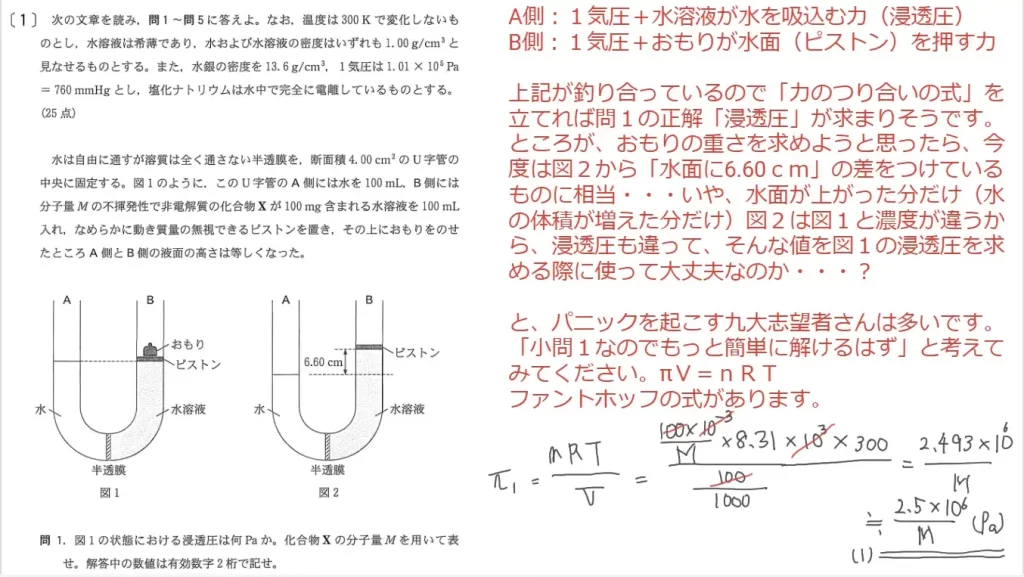
問1に関して、思考問題です。図1の状態における浸透圧を答えます。ポイントは「ファントホッフの式」です。図を見ると「重りが水面を押す圧力=浸透圧」という式を立てたくなりますが、それは問2以降で使います。ここはファントホッフの式(πV=nRT)を思い出せば、数値を当てはめて正解できます。
問2に関して、思考問題です。図1の浸透圧が「図2の液面差による圧力の何倍か」を答えます。ポイントは「図2の浸透圧」です。図2の状態は「液面差による圧力」と「浸透圧」が釣り合っています。よって、図2もファントホッフの式を使って浸透圧を求めれば、それが題意の「液面差による圧力」となります。液面差による「水量の増加、100ml→113ml」に気をつけて計算すれば、問1と同じ要領で正解できます。
問3に関して、思考問題です。重りの質量と溶質の分子量を答えます。問2でファントホッフの式を使い「図2の浸透圧」を求めましたが、これを「図2の液面差から算出した圧力」とイコールでつなぐと「未知数1つ、式1本」でMの値が求まります。Mの値が求まれば「図1の浸透圧」の値が判り、これが「重りによる圧力」と釣り合っているため、重りの質量が判明して正解となります。
問4に関して、思考問題です。図2の液面差が無くなるまでA側に投入した「塩化ナトリウムの質量」を答えます。ポイントは「液面差が無くなった=AB両側の浸透圧が等しい」という事です。ABの浸透圧が等しいという事は、ABのモル濃度(ここではモル数でよい)が等しいという事です。よって、塩化ナトリウムの質量をxミリグラムと置くと「未知数1つ、式1本」で正解できます。
問5に関して、思考問題です。化合物Xと塩化ナトリウムに関する「凝固点降下の値」を答えます。凝固点降下の式に値を入れれば正解できます。
受験生としての解説
小問1に関して、ファントホッフの式に値を代入するだけなので、全ての受験生さんが正解したい問題です。
小問2に関して
- ファントホッフの式に持ち込めばよいと気づくこと
- その際に、液面差の分だけ水量が増えた事に気づくこと
などがやや難しいため、合否を分ける1問です。小問2が不正解だと、以降の小問も全て不正解となってしまうため、厄介な1問となっています。
小問3に関して、5つの小問で1番難しい小問であり、比較的簡単に解ける小問4・小問5とセットになっているため、正解できれば他者に差をつけられる1問となっています。
小問4・小問5に関して、本問自体は「不正解の受験生さんでも正解してくるレベル」ですが、小問3を正解しておく必要があるため「小問3を正解できた人へのボーナス点」の意味合いを持ちます。
- 知識:★★★★(やや難しい)
- 思考:★★★★(やや難しい)
- 総合:★★★★(やや難しい)
- 短評:小問2が大量得点のカギ
大問2

講師としての解説
「化学平衡」からの出題です。
知識の必要性に関して、普通程度です。平衡定数と状態方程式をつなげて考えること、圧平衡定数などの知識を問われます。思考力の必要性に関して、やや強めに必要です。問2(3)で式変形による導出が続き、数学の様になります。
問1に関して、語句問題です。熱化学方程式における吸熱・発熱、ルシャトリエの原理に関する知識を問われています。式(1)の右向きの反応によって気体の分子量が増加するため、圧力を下げて(体積を増やして)分子の衝突回数を減らしてあげれば、右向きの反応が促進します。
問2(1)に関して、平衡定数を表す問題です。通常、平衡定数は「モル濃度」を使って表しますが、本問はp(圧力)R(気体定数)T(温度)を使って表すよう指示されています。そこで、気体の状態方程式「PV=nRT」を変形させ「モル濃度=n/V=P/RT」として気体定数の式を作れば正解となります。
(2)に関して、圧平衡定数を答える問題です。こちらは「圧平衡定数の式」をそのまま書けば正解となります。
(3)に関して、問題文の「pH2の算出式」に空けられた空所に、適切な計算式を代入していきます。問題文に言われた通りにするだけの問題ですが、強めに思考力を要求されています。
(オ)に関して、式①と式②で発生する(つまり右辺に書かれている)COとCO2に含まれる「酸素原子の物質量」(の比)を求められています。つまり「PV=nRT」を「n=PV/RT」と変形したものを書けば正解です。
(カ)に関して、(オ)が含まれる比の式を「内×内=外×外」で計算し、左辺をpH2でまとめた結果です。
(キ)に関して、(3)の問題文に「Kp1/Kp2も一定の値αとなる」と書いてあるので「α=Kp1/Kp2=・・・・」と式を立て、問2(2)で求めた平衡定数(Kp1とKp2)を代入して約分すると正解できます。
(ク)に関して、言われた通りにするだけです。式④を式③に代入すれば正解です。(4)に関して、先程の(ク)の式に問題文の数値を代入して計算するだけです。
受験生としての解説
2019年の九大化学5問で、4番目に簡単な問題です。
問1に関して、簡単な語句問題なので、全ての受験生さんが正解したい問題です。
問2に関して、(1)(2)は不合格者さんでも正解してくるので、落とすと痛い問題です。(3)は非医歯薬系の合格者さんでも正解がやや難しい、他者に差をつける1問です。(4)は簡単ですが、(3)の正解が必要なので、(3)まで解けた人へのボーナス点です。
- 知識:★★★(普通)
- 思考:★★★★(やや難しい)
- 総合:★★★(普通)
- 短評:
大問3

講師としての解説
「融解塩電解」からの出題です。
知識の必要性に関して、やや簡単です。問1~問7まで、各分野の簡単な基本知識の集合体と鳴っています。思考力の必要性に関して、やや簡単です。考えて解く問題はありますが、いずれも共通テストレベルかそれより簡単なレベルです。
問1に関して、融解塩電解に関する語句問題です。(ア)に関して、NaClの融解塩電解において電子を放出できるのは「Cl-」だけなのでCl2が発生します。(ウ)(エ)に関して、アルミニウム単体を融解塩電解で得る際は電極に黒鉛を用いるため「CO」と「CO2」が発生します。問題文に「炭素電極」と書いてあり、材料は「酸化アルミニウム」なので、仮に知識が無かったとしても想像で正解できます。
問2に関して、ナトリウムの融解塩電解を邪魔しない「物質とその理由」を3択から答えます。イオン化傾向がナトリウムより低い金属イオンだと、その金属イオンが電子を受け取ってしまいますが、イオン化傾向が大きいカルシウムイオンなら(K、Ca、Na、Mg、Al・・・・)ナトリウムイオンが優先して電子を受け取れるためジャマになりません。
問3に関して、製鉄に関する語句問題です。酸化鉄から酸素を取り除いただけの鉄を「銑鉄」といいます。この状態では炭素含有量が多くもろいため、酸素を吹き込んで炭素を追い出し強度を上げたものを「鋼」といいます。
問4に関して、塩化ナトリウムの単位格子に含まれるナトリウムイオン・塩化物イオンの数を答えます。
- 塩化物イオン:1/8が8個+1/2が6個=4個
- ナトリウムイオン:1/4が12個+1/1が1個=4個
となります。
問5に関して、単位格子中のナトリウムイオンの半径を答える問題です。「陰イオン同士が接している」という条件が与えられているため「ナトリウムイオンの半径=√2-塩化物イオンの半径=0.414」と計算できます。問4の図において
- 単位格子の中央にあるナトリウムイオン
- 中段の塩化物イオン4個
で考えると、解りやすいです。
問6に関して、ナトリウムに関する正誤判定問題です。(1)に関して、ナトリウムを石油中に保存する部分は正しいですが、ナトリウムは石油に浮かないため✕となります(浮いたら保存できない)(2)に関して、アルコールと反応して水素を出す事はナトリウムの性質なので◯です。(3)に関して、ナトリウムと水を反応させると水酸化ナトリウムが発生するため、液性は塩基性になります。よって、BTB溶液は青色になるため✕となります。
問7に関して、計算問題です。アルミニウム単体が5.4g生成する間に放出されたCO2の体積を求めます。アルミナが酸素を放出し、炭素棒が酸素を受け取る反応式を書くとAl:CO2=4:3になっている事がわかります。後は比の計算でCO2のモル数を出し、22.4l/molをかければ正解です。
受験生としての解説
2019年の九大化学5問で、2番目に簡単な問題です。
問1に関して、簡単な語句問題なので、全ての受験生さんが正解したい問題です。
問2に関して、不合格者さんでも正解してくるレベルなので、全ての受験生さんが正解したい問題です。
問3に関して、簡単な語句問題なので、全ての受験生さんが正解したい問題です。
問4に関して、共通テスト・センター試験で同様の問題が何度も出題されているため、全ての受験生さんが正解したい問題です。
問5に関して、問4に続き本問も共通テストレベルなので、全ての受験生さんが正解したい問題です。
問6に関して、◯✕問題3つとも基本知識レベルなので、全ての受験生さんが正解したい問題です。
問7に関して、簡単な比の計算で共通テストレベルなので、全ての受験生さんが正解したい問題です。
- 知識:★★(やや簡単)
- 思考:★★(やや簡単)
- 総合:★★★(普通、量が多い)
- 短評:才能が無い人ほど大事にしたい1問
大問4
講師としての解説
「構造決定」からの出題です。
知識の必要性に関して、普通程度です。還元性のフェーリング液、ベンゼン環を酸化した安息香酸など、使われる物質はベーシックなものが並び、量も多くありません。思考力の必要性に関して、やや強く必要です。旧帝大の構造決定問題としてはやや簡単な部類です。
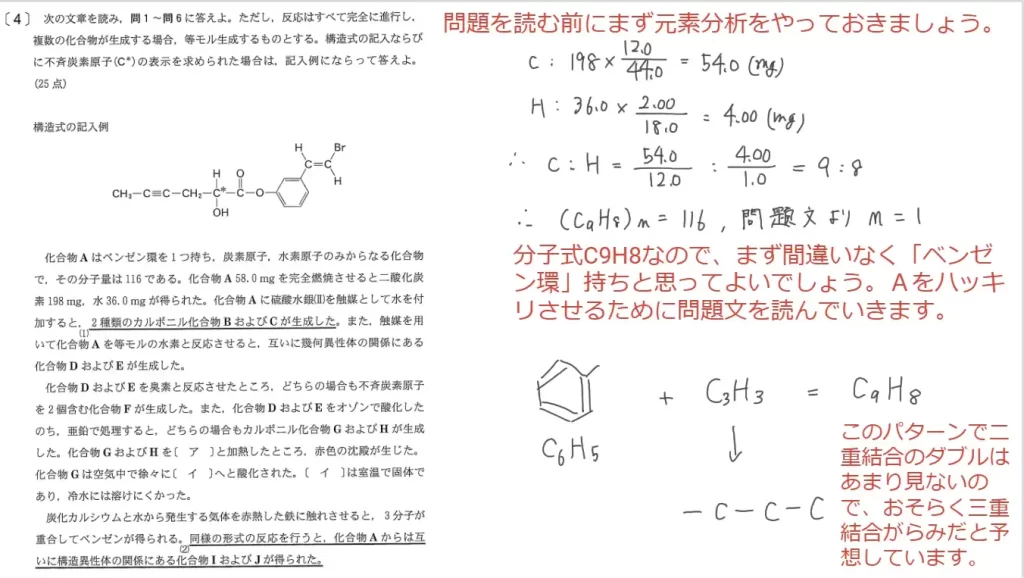
問1に関して、化合物Aの分子式と構造式を答えます。構造決定とセットになる事が多い「元素分析」の計算をするとAの組成式が解ります。問題文に「Aの分子量は116」と書いてあるので、組成式がそのまま分子式となり正解できます。構造式に関して、問題文に「H2を付加すると幾何異性体のD・Eが生じる」と書いてあるので、Aは三重結合持ちと解り、構造式が確定します。
問2に関して、化合物BとCを区別するのに最適な方法を3択から答えます。化合物Aの三重結合に水を付加させるとBとCが発生しますが、片方だけヨードホルム反応を示す「CH3CHOH」の形をとります。よって選択肢bが正解です。
問3に関して、化合物D・Eの構造式を描く問題です。Aの三重結合を1つはずし、H2を付加したものが正解です。どちらがDかEかは、解らずとも正解となります。
問4に関して、化合物Fの構造式を描く問題です。問題文に従い、化合物D・Eに臭素を付加した図を描けば正解です。
問5に関して、空所ア・イに入る物質を答えます。空所アに関して、「赤色沈殿」という文言からフェーリング液と解ります。赤色沈殿はCu2Oです。空所イに関して、「空気中で徐々に酸化」という文言から「安息香酸か酢酸」のどちらかだと解ります。その後、「水に溶けにくかった」という文言から「無極性」とわかり、安息香酸で確定となります。
問6に関して、化合物I・Jの構造式を答えます。問題文に「アセチレンがベンゼンになる時と似た反応でAがI・Jになる」という内容が書いてあるので、指示通りに実行すれば正解です。
受験生としての解説
2019年の九大化学5問で、3番目に簡単な問題です。
問1に関して、分子量は元素分析の計算をするだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。Aの構造式に関して、「H2を付加すると幾何異性体になる」というのは構造決定でも簡単な部類なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、共通テストレベルの知識問題である事に加え3択解答なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、化合物Aが「三重結合持ち」と思いつかねば、この辺りから難しくなります。合否を分ける1問です。
問4に関して、問3とのセット問題です。問3が正解できれば本問も必ず正解できる作りなので、合否を分ける1問です。
問5に関して、空所アは共通テストレベルなので、全ての受験生さんが正解したい問題です。空所イは「水に溶けにくい」という直撃のヒントがありますが、問4までを正解しておく必要があるため、問3・問4とセットで合否を分ける1問です。
問6に関して、問題文から「アセチレンによるベンゼンの生成」と読み取り、それを化合物Aに応用する事は簡単ではありません。よって、正解できれば他者に差をつけられる1問となります。
- 知識:★★★(普通)
- 思考:★★★★(やや難しい)
- 総合:★★★(普通)
- 短評:構造決定としては簡単
大問5

講師としての解説
「糖類」からの出題です。
知識の必要性に関して、やや難しいです。糖類・繊維の基本知識を幅広く問われています。思考力の必要性に関して、普通程度です。小問6でアセチルセルロースの割合計算があります。
問1に関して、知識問題です。グルコースの分子式を答える問題で「C6H12O6」が正解です。
問2に関して、知識問題です。鎖状グルコースと鎖状フルクトースに含まれる不斉炭素原子の数を答えます。この二者は糖類の柱となる物質なので、構造式まで描けるようにしておきましょう。
問3に関して、知識と思考の問題です。βガラクトースの構造式を描く問題です。問題文中に「グルコースと4位のOH配置が違うだけ」という内容が書いてあります。グルコースの構造式は基本レベルなので、ここから「4位のOHとH」を入れ替えれば正解となります。
問4に関して、知識問題です。8種類の二糖類の中から「グルコース以外」の単糖を含むものを答えます。完全に知識問題ですが、8種類の内「ラクトースを除く7種類」は必須レベルです。試験中にラクトースが思い出せない事は仕方ないですが「九大に入りたいならラクトースまで憶えておこう」ぐらいの知識なので、非医歯薬系の受験生さんもできるだけ正解したいところです。
問5に関して、知識問題です。繊維に関する語句を答えます。ア~オまで全5問ですが、全て問題集に必ず載っている必須知識です。コツは丸暗記せず理屈を知る事です。例えば
- 天然繊維・・・動植物そのまま(羊毛・綿花)
- 再生繊維・・・動植物を溶かして糸状に固めただけ(木材のクズ、綿花のクズ)
- 合成繊維・・・小さい粒粒を人間が化学の力でムリヤリつなぎ合わせた糸(ナイロン、ポリエステル)
- 半合成繊維・・・概ね再生繊維だが、一部だけ合成繊維の様に人間が手を加えた糸
丸暗記したらメチャクチャ難しいですが、丸暗記しなかったら簡単な上に応用も利きます。
問6に関して、思考問題です。アセチル化された割合を求める定番問題です。もし100%全部アセチル化されたら126g増えます。しかし、問題文によると、実際は97gしか増えなかったので、正解は76.9%となります。
受験生としての解説
2019年の九大化学5問で、1番目に簡単な問題です。
問1に関して、糖類の基礎知識なので、全ての受験生さんが正解したい問題です。
問2に関して、鎖状グルコースは不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。鎖状フルクトースは、合否を分けるレベルです。
問3に関して、グルコースが描ければ正解できる問題なので、全ての受験生さんが正解したい問題です。
問4に関して、8種類の物質を完璧に答える事は不合格者さんには難しいので、合否を分ける1問です。
問5・問6に関して、こちらも合格者さんは答えられるが不合格者さんは答えられないレベルなので、合否を分ける1問です。
1つ1つの小問は簡単ですが、短い試験時間で「即答」を求められるため、基礎力が必要です。逆に言えば、基礎さえやっておけば、才能が無くても高得点を取れます。才能で劣る学生さんにとって逆転チャンスの1問です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:高得点を狙いたい1問
九州大学の化学2018年・平成30年度
大問1

講師としての解説
「原子」と「化学平衡」と「酸化還元」からの出題です。
知識の必要性に関して、やや簡単です。複数の分野をまたぐためか、どの問題もベーシックな知識で解けます。思考力の必要性に関して、やや簡単です。計算はかなりシンプルです。
問1に関して、知識問題です。H2Oに関する◯✕問題を5つ答えます。問Aに関して、H2Oの沸点がHFより高い理由は「水素結合の本数が多いから」なので、正解は✕です。問Bに関して、H2OはH+放出して酸としてはたらきますし、H+を受け取って塩基としてもはたらきます。よって正解は◯です。問Cに関して、H2Oの分子は「折れ線形」なので、正解は◯です。問Dに関して、三重点のグラフを見てもらえば解るように、水も「昇華する」ので正解は✕です。問Eに関して、H2とO2を混ぜても反応が起きない理由は「活性化エネルギーに達してないから」なので、正解は✕です。
問2に関して、思考問題です。質量数が異なる水素原子・酸素原子から成るH2Oについて答えます。(1)に関して
- 水素原子の選び方:(1H,1H)(1H,2H)(2H,2H)の3通り
- 酸素原子の選び方:16Oと18Oの2通り
- H2Oの種類:3×2=6通りが正解となります
(2)に関して、6通りの水分子の中から2番めに分子量が大きいものは「1H2H18O」です。各原子の中性子(質量数-陽子数)は左から順に「0個+1個+10個=11個」が正解となります。
問3に関して、知識問題です。過酸化水素の電子式を描くだけです。
問4に関して、思考問題です。過酸化水素の電離による「H3O+の濃度」を答えます。濃度c、電離度αとおいて増減表を描くと、電離定数K=(cα)^2/1-α≒cα^2(α<0.05は明らかより近似)となります。よって[H3O+]=√cKに問題文の数値を代入して正解となります。
問5に関して、思考問題です。過酸化水素を過マンガン酸カリウムで消費するための体積を答えます。
- 酸化剤としてはたらく過マンガン酸カリウムの半反応式
- 還元剤としてはたらく過酸化水素の半反応式
この2式から「放出した電子のモル数=受け取った電子のモル数」の式を立てて解けば正解となります。
問6に関して、知識問題です。問5から計算を省いたような出題で、上記と同様に
- ヨウ化物イオンが還元剤としてはたらく半反応式
- 過酸化水素が酸化剤としてはたらく半反応式
を立てて2式を合体すれば正解です。
受験生としての解説
問1に関して、5問とも基本的な内容なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、同位体・質量数・中性子に関する基本問題なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、電子式を描くだけなので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、電離平衡の最も基本的なタイプの計算問題です。合格者さんは確実に正解でき、不合格者さんの一定数が不正解となるレベルなので、合否を分ける1問~落とすと痛い1問です。
問5に関して、酸化還元反応の計算としては最も基本的なタイプです。不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
問6に関して、問5とほぼ同様の出題なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★★(やや簡単)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:完答したい1問
大問2

講師としての解説
「平衡」からの出題です。
知識の必要性に関して、普通程度です。化学平衡に関する基本知識で正解できます。思考力の必要性に関して、普通程度です。問3の「平衡時の全圧」がやや難しいですが、そこも含めて定番です。
問1に関して、知識問題です。与式の反応熱を答えます。問題文でCO2とCOの生成熱が与えられているので、それに関する熱化学方程式を2本立ててください。「COの式×2-CO2の式」で正解できます。
問2に関して、思考問題です。容器の中に黒鉛と二酸化炭素を投入し、30分後のCO2の分圧と反応速度を答えます。モル数をn、二酸化炭素から一酸化炭素になった割合をxと置いて増減表を作ると「モル数の比」が判ります。今、問題文より「温度一定・体積一定」なので圧力とモル数は比例しているため(PV=nRT)、ここからxが求まります。また、初期状態における状態方程式からnの値が求まる(n=PV/RT)ため、「モル数の変化量」も判ります。よって「モル数の変化量/30分=平均反応速度」で正解となります。
問3に関して、思考問題です。問2の反応をさらに進め、平衡状態になった時の「CO2とCOの分圧」および「消費されて残った黒鉛の質量」を答えます。基本的に問2と同じ要領で解けます。CO2からCOになった割合をyと新しく置き、増減表を新しく書いて計算を進めます。1点異なるのは「圧平衡定数」を使うために「平衡時の全圧」を求める事です。温度一定・体積一定なので「平衡時の全圧=初期全圧×モル数の変化割合=1.0×10^5×n(1+y)/n=(1+y)10^5」となります。ここに平衡時の「モル数の割合」を使ってCOとCO2の分圧を求め、分圧から圧平衡定数の式に持ち込めば「y=0.62」となって正解まで直行です。
問4に関して、知識問題です。気体を圧縮した際、ルシャトリエの原理に沿って、系全体で起きる事を7択から1つ答えます。圧縮によって起きる事は以下の2点です
- CO2とCOの圧力が上がる
- その後、ルシャトリエの原理に沿い、平衡が左に移る
よって、正解は選択肢(e)となります。
問5に関して、知識問題です。気体を加熱した際、ルシャトリエの原理に沿って、系全体に起きる事を確認する語句問題を5つ答えます。系全体の温度を上昇させることで、平衡が右に動くことが問1の結果(吸熱反応)から判っています。よって、反応式・左辺の値は減少し、右辺のの値は増加するため、圧平衡定数は増加します。また、左辺が1モル減るごとに右辺が2モル増えるため、全圧は増加します。
受験生としての解説
問1に関して、生成熱の式を立てるだけなので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、不合格者さんは不正解になり合格者さんは正解してくるレベルです。よって、合否を分ける1問です。
問3に関して、「平衡時の全圧」を求める部分が気づきにくいため、不合格者さんには厳しいレベルです。合格者さんでも一定割合は不正解になるレベルなので、正解できれば他者に差をつける1問となります。
問4に関して、問3の続き問題とはいえ、ルシャトリエの原理さえ知っていれば正解できます。よって、不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
問5に関して、問1~問4の内容を指しているとはいえ、問題に参加するために必要なのは「問1の正解」だけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:完答したい1問
大問3

講師としての解説
「高級脂肪酸・油脂」からの出題です。
知識の必要性に関して、普通程度です。高級脂肪酸、けん化、化学平衡に関して幅広い基礎知識を問われています。思考力の必要性に関して、普通程度です。問5のシチュエーションがやや複雑ですが、以降問6~8まで使い続けるため理解する必要があります。
問1に関して、知識問題です。高級脂肪酸に関する語句問題を2つ答えます。(ア)に関して、不飽和脂肪酸は「二重結合」を持つため、分子が空間的に折れ曲がっています。よって、直線形より空間的に自由な体積を持てるため、流動性が増し、液体となります。(イ)に関して、せっけん水における疎水基を内側に、親水基を外側にして球状となったものを「ミセル」と言います。
問2に関して、知識問題です。せっけん水溶液が弱塩基性を示す理由を、化学反応式で説明します。ポイントは「せっけんとは、高級脂肪酸のアルカリ塩」である事を知っていることです。この知識があれば「RCOONa+H2O ↔ RCOOH+NaOH」と立式できて正解となります。
問3に関して、知識問題です。せっけん水にカルシウムやマグネシウムを入れると洗浄力が低下する理由を、化学反応式で答えます。高級脂肪酸のナトリウム塩とカルシウムイオンが材料なので左辺に書き、右辺で辻つまを合わせれば正解となります。「2C11H23COONa + Ca2+ → (C11H23COO)2Ca + 2Na+」
問4に関して、知識問題です。計算問題ですが、けん化に関する最もベーシックな計算問題なので「知識問題」とみなしました。ポイントは「けん化価の336が何なのかをハッキリさせる事」です。油脂のけん化には、油脂の3倍のモル数のKOHが必要となります。油脂が1gの時の、この3倍のモル数のKOHの重さ(mg)がけん化価336です。この言葉をそのまま数式にすれば「1/M×3×56×1000=336」となり「M=5.0×10^2」で正解となります。
問5に関して、思考問題です。与式の平衡定数を答える問題です。問題のシチュエーションが複雑で色々と書いてありますが、与えられた式をそのまま「増減表」に持ち込んで平衡定数を求めるだけで正解できます。
問6に関して、思考問題です。問5の平衡反応における「物質や速度定数の動き」をグラフから読み取ります。(a)に関して、油脂2の特徴として
- 平衡反応の材料なので最初はたっぷり存在し、反応速度が速い
- 徐々に失われて最後は平衡状態と成るため、一定速度で安定する
この特徴を表すグラフはBです。(b)に関して、脂肪酸メチルエステルの特徴として
- 反応によって生成する物質なので、最小は0
- 次第に量が増えて最後は平衡状態となるため、一定量で変化が止まる
この特徴を表すグラフはEです。(c)に関して、反応速度定数には「温度のみが変化を起こす」という重要な性質があります。今、問5では温度は常に一定なので、反応速度定数を表すグラフも常に一定となります。よって、正解はDです。
問7に関して、知識問題です。問5の平衡反応に関する◯✕問題を5つ答えます。問aに関して、ルシャトリエの原理より左辺の物質が増えれば、右辺の生成物が増えます。よって、正解は◯です。問bに関して、触媒は活性化エネルギーを下げて反応速度を上げるだけなので、反応結果には関わりません。よって、正解は✕です。問cに関して、反応速度を上げると正負両方の反応速度が上がりるので、正解は✕です。問dに関して、触媒は反応速度を上げるので、結果として時短になります。よって、正解は◯です。問eに関して、平衡状態では正負の反応速度が等しくなるため、見た目の反応が止まって見えるだけです。よって、正解は✕です。
問8に関して、思考問題です。問5の段階的な変化に関して、中途に存在する物質の種類を答えます。グリセリンには3種類の枝(上・中・下)がありますが、この枝が1個だけ置換されたもの、2個だけ置換されたものの種類を数えます。上の枝と下の枝は「本質的に同じ」とみなせるため
- 1個だけ置換:(真ん中の1個)(端の1個)の2パターン
- 2個置換:(真ん中+脇の1個)(両脇2個)の2パターン
となり、合計4種類が正解となります。
受験生としての解説
問1に関して、不飽和脂肪酸とミセルは共通テストレベルなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、「せっけんとは高級脂肪酸のアルカリ塩である」と言い切ることは不合格者さんに厳しく、合格者さんはやり遂げてくる部分です。よって、合否を分ける1問です。
問3に関して、問2と同様の理由で不合格者さんには厳しく、合格者さんはやり遂げてくるレベルです。よって、合否を分ける問題です。
問4に関して、けん化価の最も基本的な問題ですが、不合格者さんの一定数は正解できないレベルです。合格する人は正解してきます。よって、最もベーシックな問題ですが、合否を分ける1問です。
問5に関して、複雑な問題文を読んで簡略化する必要があります。不合格者さんには厳しく、合格者さんは正解してくるレベルです。よって、合否を分ける1問です。
問6に関して、時間がたっぷりあれば簡単な問題ですが、大急ぎの九大入試では難易度が上がります。合格者さんでも全問正解は難しいレベルなので、正解できれば他者に差をつける1問です。
問7に関して、平衡反応における基本問題なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問8に関して、数学の「場合の数」からの出題です。パターンを数えるだけなので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
本問で注意したいのは「問7・問8が簡単」という部分です。大量の小問で疲れていると思いますが、問7は基礎知識、問8は数を数えるだけです。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:問7・問8を読み飛ばさない
大問4
講師としての解説
「芳香族」と「構造決定」からの出題です。
知識の必要性に関して、やや簡単です。本問全体が芳香族化合物の知識問題ですが、最も主流の簡単な部分からの出題です。思考力の必要性に関して、ほぼ不要です。全体が知識問題です。
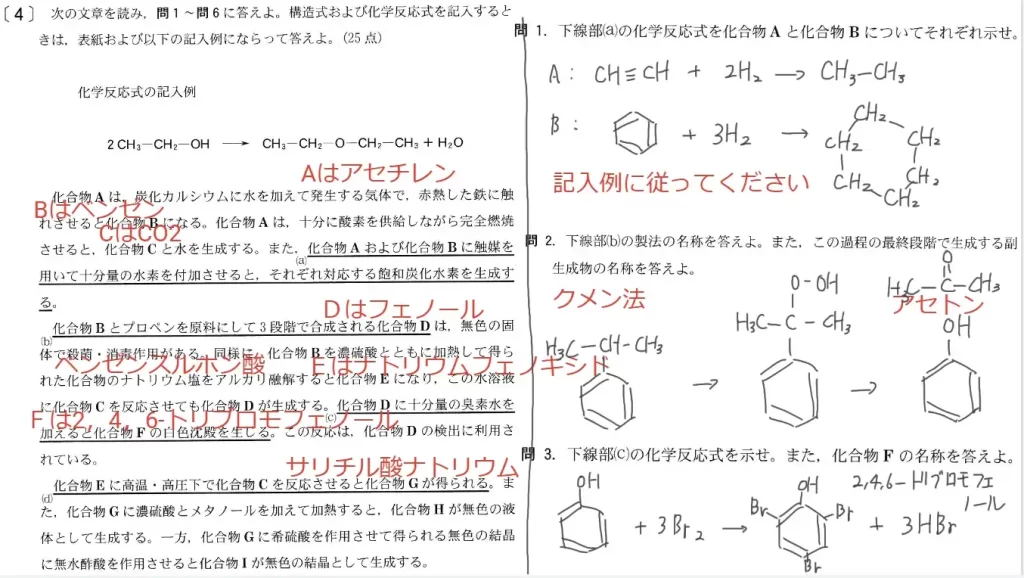
問1に関して、知識問題です。化合物A・BにH2を付加する反応式を答えます。化合物Aは「炭化カルシウムに水」より「アセチレン」が正解です。化合物Bは「アセチレンに赤熱した鉄」なので「ベンゼン」が正解です。それらを「完全燃焼させた」化合物Cは二酸化炭素です。Aに水素を付加させてエタン、Bに水素を付加させてシクロヘキサンが出る反応式を書けば正解です。
問2に関して、知識問題です。化合物Dは「ベンゼンとプロペンを原料にして3段階」より「フェノール」が正解です。この3段階の反応は「クメン法」が正解です。
問3に関して、知識問題です。化合物Fは「フェノールに臭素を反応」より「2,4,6-トリブロモフェノール」が正解です。
問4に関して、知識問題です。下線部dの反応式は「ナトリウムフェノキシド+二酸化炭素 → サリチル酸ナトリウム」となります。
問5に関して、知識問題です。化合物Hは「サリチル酸ナトリウムに濃硫酸とメタノール」より「サリチル酸メチル」が正解です。化合物Iは、サリチル酸ナトリウムを希硫酸でサリチル酸に戻した後「無水酢酸を作用」なので「アセチルサリチル酸」が正解です。
問6に関して、知識問題です。塩化鉄(Ⅲ)水溶液で呈色するのは「フェノール類」です。よって、正解は「D・E・F・G・H」となります。Eの「ナトリウムフェノキシド」ですが、問題文の「十分な酸性になっている」という文言よりフェノールに変化しているため呈色します。
受験生としての解説
問1に関して、共通テストと同等なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、クメン法も共通テストと同等なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、トリブロモフェノールは問1・問2に比べてややマイナーですが、不合格者さんでも正解してきます。
問4に関して、本分野の中でもかなり重要な式なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問5に関して、問題も後半ですが共通テストと大差ないレベルです。サリチル酸系の流れは本分野の主流なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問6に関して、塩化鉄(Ⅲ)の呈色は不合格者さんの一定数が不正解となりますが、合否を分ける1問というほど難しくはありません。
- 知識:★★(やや簡単)
- 思考:★(簡単)
- 総合:★★(やや簡単)
- 短評:完答したい1問
大問5

講師としての解説
「陽イオン交換膜」と「アミノ酸」からの出題です。
知識の必要性に関して、普通程度です。陽イオン交換膜とアミノ酸に関して基本知識を問われています。思考力の必要性に関して、普通程度です。問2がやや難しいですが、他は考える要素が少ないです。
問1に関して、知識問題です。陽イオン交換樹脂に関する語句問題を8つ答えます。スチレンとp-ジビニルベンゼンに濃硫酸でスルホ基を与えたものが陽イオン交換樹脂です。よって「ア:スチレン」「イ:濃硫酸」「エ:スルホ」が正解です。複数のモノマーを重合させてポリマーを作っているので「ウ:共」重合と言います。塩化カルシウム水溶液に「ク:陽」イオン交換樹脂を投入すると、樹脂の「カ:水素」イオンが「キ:カルシウム」と置き換わるため、pHは「オ:酸」性を示します。
問2に関して、思考問題です。化合物1はフェーリング反応を示しているので、還元性より「グルコース」が正解です。化合物2は、まずニンヒドリン反応を示したことからアミノ酸です。そしてpH2.5という強い酸性からpH4.0になっただけで陽イオンではなくなったので「グルタミン酸」が正解です。化合物3はキサントプロテイン反応を示しているので、ベンゼン環を持つアミノ酸で「チロシン」が正解です。化合物4は、まずニンヒドリン反応を示したのでアミノ酸です。そして、pH11.0になってようやく陽イオンではなくなったので、塩基性アミノ酸の「リシン」が正解です。
問3に関して、知識問題です。(ⅰ)は「Cu2+ → Cu2O、赤色沈殿」なのでフェーリング反応です。(ⅲ)は「濃硝酸、アンモニア水、橙黄色」なのでキサントプロテイン反応です。
問4に関して、知識問題です。選択肢からアミノ酸を答えます。正解は以下の通りです。
- a:アラニン
- c:グリシン
- e:グルタミン酸
- f:システイン
- h:セリン
- i:チロシン
- k:リシン
問5に関して、知識問題です。不斉炭素原子を持たないアミノ酸は「グリシン」です。
問6に関して、思考問題です。問題文で指定されている「分子量の小さい」アミノ酸はグリシンとアラニンです。これら2つをN末端・C末端を入れ替えて結合させた2種類の構造を描くと正解です。
受験生としての解説
問1に関して、陽イオン交換樹脂に関する基礎知識なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、実験の内容を理解する必要があるため、合格者さんでも一定数は不正解になります。よって、正解できれば他者に差をつけられる1問です。
問3に関して、反応名を答えるだけなので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、アミノ酸を答えるだけなので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問5に関して、不斉炭素原子を持たないアミノ酸がグリシンである事は不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問6に関して、分子量が小さい2つは解りやすいですし、C末端・N末端の入れ替えも不合格者さんにとって難しくないです。よって、全ての受験生さんが正解したい問題です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:問3以降が簡単なので拾いたい
九州大学の化学2017年・平成29年度
大問1
講師としての解説
「アルミニウム」と「遷移元素」からの出題です。
知識の必要性に関して、やや難しいです。不動態の「クロム」、イオン化傾向の「マンガン」など、一般的な大学受験のゴロ合わせに入ってない知識が出題されています。思考力の必要性に関して、普通程度です。計算問題は難しくありません。
問1に関して、知識問題です。2004年に九大理学部OB森田浩介さんによって発見され、2016年にアジア初の新元素として命名された「①:ニホニウム」が、2017年九大化学のトップで出題されています。続いて、アルミニウムの知識問題です。アルミニウムは「ア:13」族元素です。ボーキサイトを精錬したアルミナ「A:Al2O3」から作られ、価電子数は「イ:3」個です。単体のアルミニウムは酸とも塩基とも反応するため「②:両」性元素と呼ばれており、結晶格子は「③:面心立方」格子で配位数は「ウ:12」充填率は「エ:74」%となっています。
問2に関して、知識問題です。アルミニウムは両性元素なので、NaOHと反応してH2を発生する事を思い出せば正解できます。過剰NaOHで錯イオン「テトラヒドロキシドアルミン酸イオン」となる方向からでも正解できます。
問3に関して、知識問題です。不動態を形成する金属には「手にある(鉄・ニッケル・アルミニウム)」というゴロ合わせがありますが、難関大レベルになると「クロム、コバルト」も出題されるので注意してください。本問の正解は「クロム、Cr」です。
問4に関して、知識問題です。イオン化傾向を問う問題ですが、問3同様、ゴロ合わせに入ってない「マンガン、Mn」が出題されています。マンガンのイオン化傾向は「アルミニウムの次」と憶えておいてください(ただし、マグネシウムと銅がかなり離れているので、その間にマンガンが来そうな事は予測できます)
問5に関して、思考問題です。面心立方格子の密度に関する式を立て、「分子量=」の形でまとめると正解できます。コツは、質量と体積をバラバラに計算する事で。まとめて密度で計算すると頭が混乱しますが「質量だけ」と考えれば「分子量÷アボガドロ定数×原子4個」とすぐ解りますし、「体積だけ」と考えれば「縦×横×高さ」です。そして、最後に「密度=質量/体積」となります。
問6に関して、知識問題です。亜鉛の電子殻に含まれる「電子の個数」を答えます。まず、周期表のゴロ合わせを思い出してください。「水平リーベ僕の船(省略)閣下スコッチばくろ(Cr)うまん、テコにド(Cu)ア(Zn)が」という事で、亜鉛の原子番号は30番と解りました。遷移元素は「電子殻への電子の入り方」が不規則になってはいますが
- K殻:最大2個
- L殻:最大8個
- M殻:最大18個
の合計28個は決まっているため、原子番号30番の亜鉛は「N殻が2個」と導き出せます(原子番号28番のニッケルまではこの方法が使えないので注意です)
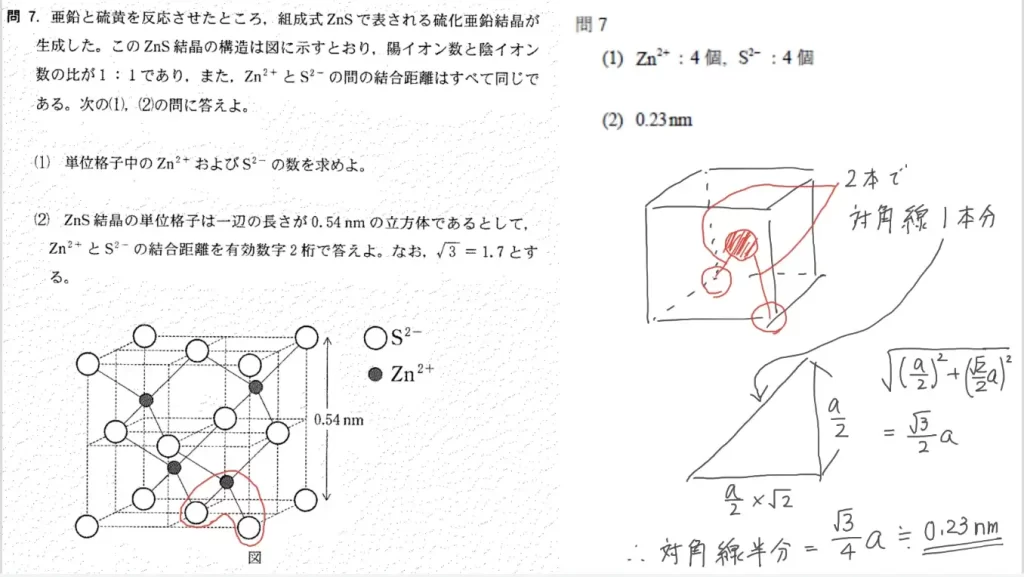
問7に関して、思考問題です。まず(1)ですが、Zn2+の単位格子中の個数は「1/8×8+1/2×6=4個」となります。S2-の個数は見たままで4個となります。続いて(2)ですが、単位格子を8分割(縦半分、横半分、高さ半分)したブロック1個の内「Zn2+」を含むブロックで考えると解りやすいです。求める「Zn2+とS2-の結合距離」の2倍が、ブロックの対角線1本分となります。よって、単位格子の一辺の長さaとして「対角線1本文=√3/2×a」となり、「対角線1/2本分=√3/4×a≒0.23ナノメートル」が正解です。
受験生としての解説
問1に関して、「エ:充填率」を除けば不合格者さんでも正解してくるレベルです。充填率に関して、時間がたっぷりあれば簡単な問題です。しかし、大問1は小問が7つもある上に、小問1だけで語句問題が8つもあるので、素早く作図・計算するとなると合格者レベルの能力と言えます。
問2に関して、基礎知識ではありますが不合格者さんの一定数は正解できないレベルです。逆に言えば、不合格者さんでも一定数は正解してくるので、全ての受験生さんが正解したい問題です。
問3に関して、クロムが不動態を作ることは不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、マンガンのイオン化傾向は合格者さんでも難しいです。よって、正解できれば他者に差をつける1問となります
問5に関して、密度の式を立てるだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問6に関して、遷移元素の電子の入り方は合格者さんでも難しいレベルです。よって、正解できれば他者に差をつける1問となります。
問7に関して、やや難しい図形問題ですが、九大数学に比べれば明らかに簡単です。よって、不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
- 知識:★★★★(やや難しい)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:小問1・5・7の計算問題は正解したい
大問2

講師としての解説
「沸点上昇・凝固点降下」からの出題です。
知識の必要性に関して、普通程度です。沸点上昇・凝固点降下の式を使います。この式(Δt=Km)に登場するmは「モル濃度」ではなく「質量モル濃度」である事がやや難しいです。思考力の必要性に関して、難しいです。取り掛かりとなる小問1、締めくくりとなる小問5で思考力を要求されます。
問1に関して、思考問題です。溶媒を投入した後の溶液の沸点を求める問題です。九大化学の導入でよくあるパターン「沸点上昇の式」に値を代入する問題かと思いきや、「溶質Aの式量」が与えられてないため式が立ちません。そこで別の取り組みを問題文から探してみると
- 1.0×10^5Paにおける溶媒Bの沸点はTBである
- 温度を1K上げるごとに蒸気圧はΔPだけ上昇する
- 溶質投入後の溶液の蒸気圧はPBAであった
という事が解ります。よって、これらの情報を総合すると「沸点=TB+(1.0×10^5-PBA)/ΔP」が正解となります。
問2に関して、思考問題です。問1で問題文に書かれていなかった「Aの式量」を求める問題です。ここで私たちが普段よく使う「沸点上昇=K×m」を使います。つまり「問1で求めた沸点上昇=K×m」で立式すると「未知数1つ、式1本」で正解となる「Aの式量」が求まります。
問3に関して、思考問題です。Aの電離で発生した陽イオン・陰イオンの溶解度積を答えます。問題文より、A1つから陽イオン・陰イオンが1つずつ電離するとわかっているので「Aのモル濃度=陽イオンのモル濃度=陰イオンのモル濃度」となります。よって、「溶解度積=陽イオン濃度×陰イオン濃度=Aのモル濃度の2乗」となり、Aのモル濃度を計算で求めれば正解となります。「Aのモル濃度=w/M÷V」です。
問4に関して、思考問題です。問3までの状況に加え、さらに溶質Aを溶かそうとしたが「全く溶けなかった」時に起こる変化を、4択から答えます。選択肢Aに関して、溶液の沸点が純溶媒の沸点を下回ることはないため、正解は✕です。選択肢B~Dに関して、根拠は全て「濃度が変化してないので、沸点も変化しない」となります。よって、正解は「Bが✕、Cが◯、Dが✕」です。
問5に関して、思考問題です。実験3の溶液から上澄みを取り、冷却させて溶媒Aを析出させ、凝固点を変化させています。この様に複雑な問題を解く際のコツは、部品に分解し、部品ごとに集中して計算し、最後に合体させることです。
- 抜いた上澄みの割合をx%とおく
- 上澄みに含まれる溶質の質量を求める
- 上澄みに含まれる溶媒の質量を求める
- 「凝固点降下の式」に上記を放り込んで合体
- 「x=・・・」の形でまとめれば正解
となります。
受験生としての解説
問1に関して、合格者さんでも厳しいです。難しい問題です。
問2に関して、本問自体は(沸点上昇の計算自体は)不合格者さんでも一定数が正解してくるレベルです。しかし、本問に参加するためには問1の正解が必要であり、問1とセットで難しい問題となります。
問3に関して、本問単体なら「合否を分ける1問」というレベルですが、参加するためには問1の正解が必要です。よって、問1とセットで難しい問題となります。
問4に関して、不合格者さんには厳しく、合格者さんは正解してくるレベルです。よって、合否をわける1問です。本問で大切な事は、問1~問3が正解できなくても、問4単体で問題に参加できることです。
問5に関して、短い試験時間を考慮すると、非医歯薬系の合格者さんでも多くの割合が不正解になる問題です。正解できれば他者に差をつける1問となります。
小問5つの中で最も難しいのが小問1です。よって、1番難しい問題を解かなければ「大問丸ごと0点」になってしまうという事で、非常に扱いの難しい1問でした。本問に関して、仮に小問1を突破しても、小問3・小問5が思考を要する問題ですし、小問2も通常の九大レベルの計算問題です。本問に全力を尽くすより、他の化学・物理の問題に力を入れたほうが高得点を回収できると思います。
- 知識:★★★(普通)
- 思考:★★★★★(難しい)
- 総合:★★★★★(難しい)
- 短評:医学科の合否を分ける1問
- 短評:小問4だけ単独で解ける事に気づきたい
大問3

講師としての解説
「アンモニア」からの出題です。
知識の必要性に関して、普通程度です。アンモニアに関する基本知識を幅広く問われています。思考力の必要性に関して、やや簡単です。軽めの計算問題があります。
問1に関して、知識問題です。アンモニアに関する語句問題を6つ答えます。アンモニアの水素原子と窒素原子は「ア:共有結合」しています。窒素原子が大きな「イ:電気陰性度」を有しているため、アンモニア分子の水素原子と「ウ:静電気力」で引き合っています。これを「エ:水素結合」と言います。また、アンモニウムイオンは、水素イオンと窒素原子が「オ:配位結合」しており、このアンモニウムイオンと塩化物イオンの間で「カ:イオン結合」したものが塩化アンモニウムです。
問2に関して、知識問題です。ハーバーボッシュ法に関する◯✕問題を4つ答えます。問(1)に関して、ハーバーボッシュ法は鉄触媒なので、正解は◯です。問(2)に関して、平衡定数は温度によってのみ変化する値なので、正解は✕です。問(3)に関して、アンモニアの生成は発熱はんのうなので、温度を上げると平衡が左へ移動し、平衡定数は小さくなります。よって、正解は✕です。問(4)に関して、ハーバーボッシュ法は高圧で行うので、正解は◯です。
問3に関して、知識問題です。アンモニアの実験室における製法の反応式を答えます。材料(左辺)は問題文で与えられており、右辺でアンモニアが生じる事も分かっているので、後は辻つまを合わせて「CaCl+2H2O」で正解となります。
問4に関して、知識問題です。空所キ~ケに化学式を入れ、ソルベー法の式を完成させます。
- 問題文に「炭酸」「ナトリウムの製法」と書いてある事を確認してください
- 「ナトリウム」は海から塩を持ってくればほぼ無料なので、(キ)には「NaCl」が入ると予想がつきます
- 「炭酸」は空気中の二酸化炭素を使えば無料なので、(ク)には「CO2」が入るだろうと予想がつきます
- よって(ケ)は「左辺-右辺」で残り物を固めた「NaHCO3」が入ると導き出せます
問5に関して、思考問題です。まず問(a)に関して、アンモニアの緩衝溶液のpHを答えます。問題文で「アンモニアの電離定数」が与えられているので、電離平衡の式を書いてください。実は目的の「水酸化物イオン濃度」を除く全ての数値(電離定数、アンモニウムイオンの濃度、アンモニアの濃度)が、問題文で既に与えられているので、計算するだけで正解できます。1点だけ注意が必要なのは、アンモニア水100mlと塩化アンモニウム水100mlを混ぜるので「体積が2倍の200mlになり、濃度が半分になる」ことです。問(b)に関して、塩酸を加えると「NH3+HCl → NH4+ + Cl-」という反応が置きます。結果として、塩酸1モルにつきNH3が1モル消費され、NH4+が1モル増えます。この関係を加えて濃度を再計算し、問(a)と同じプロセスをたどれば正解できます。
問6に関して、知識問題です。ポイントは問題文の「過剰のアンモニア水」です。アンモニア水は塩基性なので、アルカリ金属・アルカリ土類金属以外の金属イオンは概ね水酸化物を生じて沈殿します。しかし、アンモニアが過剰な場合「亜鉛、銅、銀」の水酸化物イオンは、錯イオンとなって再び溶けてしまいます。よって、(1)の正解は「Fe(OH)3、赤褐色沈殿」、(2)の正解は「[Cu(NH3)4]2+、濃青色溶液」となります。
丸暗記回避
鉄は信号機(緑→黃→赤)と憶えてください。
| Fe2+ 緑色 | Fe(OH)2 緑白色 |
| Fe3+ 黄色 | Fe(OH)3 赤褐色 |
受験生としての解説
問1に関して、共通テストと同等なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、1つ1つは難しくないですが、4問全て正解となると不合格者さんには厳しく、合格者さんはやり遂げてくるレベルです。よって、合否を分ける1問です。
問3に関して、与えられた材料から反応式を導くだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、ソルベー法の穴埋めなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問5に関して、問(a)がは不合格者さんでも正解してきます。問(b)は不合格者さんには少し難しいレベル、合格者さんは正解してくるレベルです。よって、合否を分ける1問となります。
問6に関して、不合格者さんでも正解してくるレベルです。よって、全ての受験生さんが正解したい問題です。
- 知識:★★★(普通)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:完答したい1問
大問4

講師としての解説
「構造決定」からの出題です。
知識の必要性に関して、やや簡単です。マルコフニコフ則を知っておく必要がありますが、九大対策をしていれば頻繁に学ぶものです。思考力の必要性に関して、普通程度です。構造決定問題の中では簡単な部類です。
問1に関して、思考問題です。まず、Aに水素を付加してできるものは1パターンしかないので「Cはプロパン」で確定。よって「Aはプロペン」で確定です。同様にBに水素を付加してできる分枝炭化水素は1パターンしかないので「Dは2-メチルブタン」で確定です。Bは炭素骨格までは判りましたが、二重結合の位置が不明です。
問2に関して、思考問題です。問題文の「Aに水を付加するとアルコールE・F」と「Eは少量しか生成しない」より、マルコフニコフ則から「Eは1-プロパノール」「Fは2-プロパノール」で確定です。また「Bに水を付加してできるG・Hは一級アルコールではない」という内容より、「Bは2-メチル-2-ブテン」で確定です。また「Gは少量しか生成しない」より、マルコフニコフ則から「Gは3-メチル-2-ブタノール」「Hは2-メチル-2-ブタノール」で確定です。
問3に関して、思考問題です。「A・Bに臭素を付加したものがI・J」という内容より「IとJも確定」します。これでE~Jまで揃ったので、不斉炭素原子を持つ化合物を見ると「G・I・J」が正解となります。
問4に関して、思考問題です。「化合物Bをオゾン酸化すると化合物K・L」および「Kは銀鏡反応を示す」より、「Kはアセトアルデヒド」「Lはアセトン」で確定です。
問5に関して、思考問題です。最も小さい質量を持つIの分子量は200です(79Brを2つ使用)そして、79Brの存在比が51%なので、2連続で持つ確率「51%×51%≒26%」が正解となります。
受験生としての解説
問1~問4に関して、構造決定の中でも簡単な部類なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問5に関して、簡単な確率計算なので、不合格者さんもその場で対応してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★★(やや簡単)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:完答したい1問
大問5

講師としての解説
知識の必要性に関して、普通程度です。天然高分子の基本知識があれば正解できます。思考力の必要性に関して、普通程度です。小問8は難しいですが、他は普通程度の計算です。
問1に関して、知識問題です。セルロースに関する文章の誤文修正を2ヶ所行います。「セルロース分子はβグルコースの1位と3位がグリコシド結合」と書いてありますが、「3位ではなく4位」が正解です。また「グルコースは分子内で水素結合をする」と書いてありますが「分子内ではなく分子間」が正解となります。
問2に関して、知識問題です。セルロースを分解していく過程の物質名を3つ答えます。セルロースを分解すると「C:セロビオース」になります。この際に使用される酵素は「A:セロビアーゼ」です。セロビオースを分解する際に使用される酵素は「B:セロビアーゼ」で正解となります。
問3に関して、知識問題です。セルラーゼとセロビアーゼの働きを確認する方法を5択から答えます。選択肢aに関して、この反応中にデンプンは無いため要素ヨウ化カリウム水溶液は不適切です。選択肢bに関して、セロビアーゼのはたらきで生じたグルコースは還元性を示すため、フェーリング溶液での確認は適切です。よって、正解です。選択肢cに関して、この反応中にアミノ酸・タンパク質は存在しないため、ニンヒドリン溶液は不適切です。選択肢dに関して、反応の前後でpHは大きく変わらないため、リトマス試験紙は不適切です。選択肢eに関して、セルラーゼはたらいてセルロースが消費されると白濁が薄くなります。よって、白濁の確認は正解です。
問4に関して、思考問題です。下線部(1)セルロースがグルコースに分解される反応を化学式で書くと「(C6H10O5)n + (n-1)H2O → nC6H12O6」となります。この反応式から得られる分子量と、問題文にかかれている実際のセルロースの質量(72.0g)で比の式を組むと「162n:180n=72.0:x」となり、式を解いて「x=80.0g」が正解となります。
問5に関して、知識問題です。アルコール発酵の化学式は「C6H12O6 → 2C2H5OH + 2CO2」で正解となります。
問6に関して、思考問題です。アルコール発酵によってCO2が0.500モル発生した時の、元になったセルロースの質量を答えます。反応を丁寧に遡って行きましょう。まず、アルコール発酵の式より、CO2の半分のモル数のグルコースが消費されています。そのグルコースがnモル集まってセルロースができていますから、今回使われたセルロースのモル数は「0.500÷2÷nモル」となります。今、セルロースは1モルで162nグラムなので、「0.500÷2÷n×162n=40.5グラム」が正解となります。
問7に関して、思考問題です。与えられた反応熱・燃焼熱の熱化学方程式を立てると
- C6H12O6 → 2CO2 + 2C2H5OH + 84.0kJ
- C6H12O6 + 6O2 = 6CO2 + 6H2O + 2820kJ
今「式2×1/2-式1×1/2」より「C2H5OH + 3O2 = 2CO2 + 3H2O + 1368kJ」となります。よって「1368kJ/モル」が正解となります。
受験生としての解説
問1~問3に関して、セルロースに関する基本知識なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4・問5に関して、基本的な問題ですが不合格者さんの一定数が不正解になるレベルです。よって、落とすと痛い1問となります。
問6・問7に関して、不合格者さんにはやや厳しく、合格者さんは正解してくるレベルです。よって、合否を分ける1問となります。
問8に関して、合格者さんでも難しいレベルです。よって、正解できれば他者に差をつけられる1問となります。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:
九州大学の化学2016年・平成28年度
大問1

講師としての解説
「16族元素」からの出題です。
知識の必要性に関して、やや簡単です。知識問題が続きますが、概ね共通テストレベルばかりです。思考力の必要性に関して、ほぼ不要です。知識問題の集合体です。
問1に関して、知識問題です。H2Oに関する語句問題を12個答えます。水分子では酸素・水素原子が「ア:共有結合」しています。O-H間の「イ:極性」が大きいため分子間で「ウ:静電気」的な結びつきである水素結合を形成しています。水分子に水素イオンが「エ:配位」結合することによりオキソニウムイオンとなります。温度が下がると氷となり、その酸素原子は「オ:正四面体」の各頂点に位置します。この構造において酸素原子は水素原子と「Y:2」個の共有結合、「Z:2」個の水素結合、合計「X:4」個の結合しています。また、三重点より高圧では液体の「カ:沸点」が上がり、逆に固体の「キ:融点」は下がります。三重点の固体ー液体の直線が左に傾いていることは、圧力が上がると固体の水素結合が切れて体積が「ク:減少」し、密度が「ケ:増加」する事を示しています。
問2に関して、知識問題です。16族元素の水素化合物の沸点を高い順に答えます。まず、水素結合を持つ酸素(水)が突き抜けて高く、他は「分子量」の順(分子間力の順)に沸点が高くなります。本問ではH2Oは対象外なので、正解は「H2Te>H2Se>H2S」となります。
問3に関して、知識問題です。フッ化水素の方が「分子の極性」が大きいのに、水の方が沸点が高い理由は、水の方が「水素結合の数が多いから」です。
問4に関して、オキソニウムイオンの電子式を描きます。ポイントは
- 水素は配位結合も共有結合も同じに書くこと
- 1価の陽イオンになるためカッコの外側に「+」をつけることです
問5に関して、知識問題です。オキソニウムイオンにおける「∠HOH」が水分子より大きくなる理由は「水素イオンが配位結合したことにより、非共有電子対の電気的反発が弱まるから」です。
問6に関して、知識問題です。三重点のグラフに関する用語を答えます。正解は以下の通りです。
- 固体ー液体を分ける線「融解曲線」
- 液体ー気体を分ける線「蒸気圧曲線」
- 気体ー固体を分ける線「昇華圧曲線」
- 3線が交わる点「三重点」
受験生としての解説
問1に関して、12個と多めの知識問題ですが、いずれも共通テストレベルなので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、分子間力の順に沸点が上がるだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、「水素結合の本数」も共通テストレベルの問題なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、電子式を描くだけなので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問5に関して、知識問題が続きますが、本問は少し詳しい内容となっています。不合格者さんにはやや厳しく、合格者さんは正解してくるレベルです。よって、合否を分ける1問です。
問6に関して、「昇華圧曲線」が難しいですが、他は余所の分野でも出てくるためおなじみです。よって、不合格者さんでも正解してくるため、全ての受験生さんが正解したい問題です。
- 知識:★★(やや簡単)
- 思考:★(ほぼ不要、知識問題)
- 総合:★(簡単)
- 短評:「昇華圧曲線」以外は完答したい問題
大問2

講師としての解説
「反応速度」からの出題です。
知識の必要性に関して、やや簡単です。濃度を使った速度計算が続く大問なので、それを支える基本知識があれば十分です。思考力の必要性に関して、普通程度です。小問の数が多いため、問題文について行く事は大変ですが、1問あたりの難易度は最後までそれほど高くなりません。
問1に関して、思考問題です。時間「t=0→t1」の間にPの濃度は「0 → [P]t1」になっているので「v0=[P]t1/t1」が正解となります。
問2に関して、思考問題です。時刻t1におけるAのモル数は「最初にあったAのモル数-反応によって減ったAのモル数」で表現できます。
- 最初あったモル数:[A]0V
- 反応で減ったモル数:[P]t1V
- 残っているモル数:V([A]0-[P]t1)=([A]0-v0t1)Vが正解です
問3に関して、知識問題です。平衡状態の時、正反応と負反応の速度が等しくなって、見た目は止まって見えています。よって「v+ = v-」が正解です。
問4に関して、思考問題です。問題文において「[E]eを使って答えよ」という内容なので、平衡時の式を立てる事になりそうです。よって、問3より「v+ = v-」の式も使えて都合が良いです。難点は[C]tと[D]tの扱いですが
- 初期状態:[C]0と[D]0
- 平衡反応によって減った濃度:[E]e
なので、平衡時の濃度は引き算で算出できます。後は「v+ = v-」の式に代入して「k2/k-2=・・・」とまとめれば正解です。
問5に関して、思考問題です。時刻tにおけるZの濃度ですが
- 時刻tまでに③式で発生したZの濃度:[X]0-[X]t
- 時刻tまでに④式で消費されたZの濃度:[Q]t
の引き算で出ます。よって、[X]0-[X]t-[Q]tが正解です。
問6に関して、思考問題です。Zを消滅させる要素は
- ③式の左方向への反応
- ④式の右方向への反応
なので、この2要素を合体した「k-3[Z]t + k4[Z]t」が正解となります。
問7に関して、思考問題です。ポイントは問題文の「Qが生成する速度が一定になった」という部分です。Qの速度が安定したという事は、中間生成物である「Zの生成と消滅の速度が等しくなった」ことを意味しており「③式右方向のZ生成速度=問6で求めたZ消滅速度」となります。この式を立て、問題文で要求された形に左辺を整えると、右辺が「k3/(k-3+k4)」となり、これが正解です。
受験生としての解説
問1に関して、算数の問題なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、問題文が長いため見た目よりは難しいですが、不合格者さんでも十分対応してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、反応速度の基礎知識なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、CとDの平衡時の濃度を表す部分が少し難しいです。不合格者さんの一定数が不正解になるレベルですが、合格者さんは正解してきます。よって、全ての受験生さんが正解したい問題です。
問5に関して、そろそろ不合格者さんには厳しいレベルです。合格者さんは正解してきます。よって、合否を分ける1問です。
問6に関して、正解を見せられるとすぐ解ることですが、不合格者さんが試験中に気づくことは難しいです。合格者さんでも気づかない人はいるでしょう。よって、合否を分ける1問です。
問7に関して、合格者さんでもやや難しいレベルです。よって、正解できれば他者に差をつける1問となります。
- 知識:★★(やや簡単)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:問5までは正解したい
大問3

講師としての解説
「反応熱」と「反応量」の計算問題です。
知識の必要性に関して、やや簡単です。熱化学方程式を使えれば正解できます。思考力の必要性に関して、やや難しいです。全編計算問題であり、特別難しい1問はありませんが平易な計算も少なく、やや歯ごたえのある問題が続きます。
問1に関して、思考問題です。与えられた3つの式①~③に加え、Fe2O3(固)の生成熱の式を④、COの生成熱の式を⑤とすると
- 反応熱の判明している式:①④⑤
- 反応熱の不明な式:②③
となります。よって、①④⑤を変形して②③を作れば反応熱が判り、正解は以下の通りです。
- ②式:①×-1+④×-2+⑤×3より491kJ/モル
- ③式:⑤×3-①+②より111kJ/モル
問2に関して、思考問題です。問1の式を応用します。問アに関して、①式の反応が起きても②式の反応が起きても、1モルのFe2O3からFeが2モル発生します。よって、Fe2O3を毎分10モル投入しているため、Feは毎分「20モル」が正解となります。
問イに関して、毎分100モルの空気が投入され、酸素:窒素=21:79と書いてあるので、酸素の投入量は毎分「21モル」が正解となります。
問ウに関して、投入された酸素が使われる反応は③式だけであり、③式より投入された酸素の2倍の炭素が消費されると解るので、消費される炭素のモル数は「42モル(21×2)」が正解です。
問エに関して、反応機に投入される酸素原子は
- Fe2O3由来:毎分10モル×3=毎分30モル
- 空気のO2由来:毎分21モル×2=毎分42モル
- 合計:72モル
この酸素原子をCOとCO2が「2:1」で排出される(問題文より)ので、COとCO2が消費する酸素原子は「1:1」となる。よって、CO2は毎分36モル(72÷2)の酸素原子を消費するので、CO2の排出量は毎分「18モル」が正解です。
問オに関して、毎分18モルのCO2と36モルのCOが排出され、ここで排出されるC原子と同量のC原子が容器に投入されているので、C原子の投入量は毎分「54モル」が正解です。
問カに関して、問オより、投入されるC原子の量は毎分54モル、問ウより、式③で消費されるC原子は毎分42モルと判っています。この式③で消費されなかったC原子が式②の反応へ向かうため、毎分12モルのC原子が式②へ向かいます。式②における反応比は「Fe2O3:C=1:3」なので、式②で還元されるFe2O3のモル数は毎分「4モル(12×1/3)」が正解となります。
問キに関して、ここまでの流れより、10モルのFe2O3から20モルのFeを生成する時、消費される炭素は54モルと判りました。よって、生成する鉄の54/20倍のモル数の炭素が消費されるので「100/55.8 × 54/20 × 12.0≒58g」が正解となります。
受験生としての解説
問1に関して、見た目より難しい問題です。理由は同タイプの問題の中でも「CO→CO2の反応熱」が見つけにくいためです。「反応熱=右辺の生成熱の総和-左辺の生成熱の総和」の活用に気付ければ一発ですが、式変形から求めていく場合は、ややクセのある変形過程となります。よって、不合格者さんには厳しいレベル、合格者さんでも一定数の不正解者が出る問題です。正解できれば他者に差をつける1問です。
問2の問ア~問ウに関して、問題文のヒントを読み取れればすぐに正解を出せる(1:1の関係)ため、不合格者さんでも正解できます。よって、全ての受験生さんが正解したい問題です。
問2の問エ~問キに関して、応用のレベルが上がり、問題文のヒントを複数組み合わせて正解を出していきます。よって、不合格者さんには厳しく、合格者さんでも最終問(キ)までたどり着けるのは一定数となります。よって、正解できれば他者に差をつける1問となります。
単純に計算問題なので、試験現場で素早く理解し、正確な計算に持ち込める「才能に恵まれた」トップ高校の学生さんに有利な問題です。才能で劣る学生さんは問2の(ア)~(ウ)だけ確実に拾い、残りは解ける所まで解ければ十分です。
- 知識:★★(やや簡単)
- 思考:★★★★(やや難しい)
- 総合:★★★★(やや難しい)
- 短評:問2(ア)~(ウ)は正解したい
大問4

講師としての解説
「構造決定」からの出題です。
知識の必要性に関して、普通程度です。構造決定の定番知識で正解できます。思考力の必要性に関して、普通程度です。構造決定としては難しくありません。深く追求していくより、広く浅くの出題です。
問1に関して、思考問題です。化合物Aの分子式を求める問題なので元素分析シていきましょう。化合物A61.5mgを完全燃焼させた結果より
- Cの質量:198 × 12.0/44.0 = 54.0(mg)
- Hの質量:67.5 × 2.00/18.0 = 7.50(mg)
- 物質量比「C:H=54.0/12 : 7.50/1.00 =3:5
- よって組成式は「C3H5」
- 分子量82.0よりA・B・Cの分子式は「C6H10」
上記が正解となります。
問2に関して、知識問題です。「ヨウ素と水酸化ナトリウムを加えて黄色沈殿」と書いてあるので、正解は「ヨードホルム反応」です。
問3に関して、思考問題です。問題文の「分子量100の化合物D」より、化合物A(分子量82.0)にH2Oが付加してDになった事が解ります。また「CH3が一つだけ」より、化合物Aは炭素鎖が一直線である事が解ります。よって
- AはC6H10
- Dはヨードホルム反応
- A・Dは炭素原子が一直線
- A + H2O =D(C6H12O)
より、Dの構造式は「CH3COCH2CH2CH2CH3」と解ります。一般名は「ケトン」で正解となります。
問4に関して、思考問題です。問題文の「三つの幾何異性体」より、化合物Bは「二重結合2個持ち」と解ります。ここで「十分な量の臭素」を付加させたものがEなので、B1モルに対し臭素が2モル(臭素原子が4モル)付加したと解ります。よって
- 化合物B:Br2 = 82.0:79.9×4=61.5(mg):x(mg)
- x=239.7 ≒ 240(mg)
上記が正解となります。
問5に関して、思考問題です。C原子が6個の化合物Bで「二重結合2個持ち」なので、素直に「2番目と4番目の炭素原子」に二重結合を付け、トランス型に描けば自然と正解が出ます。
問6に関して、知識問題です。アルコールに単体のナトリウムを加えるとH2が発生します。よって正解は「2CH3OH + 2Na → 2CH3ONa + H2」となります。
問7に関して、思考問題です。問題文の「十分な水素を付加させると分子量84.0」より、水素が1モルしか付加してない事が解るので「Cは二重結合1つ → 環状構造」と解ります。また問題文「二クロム酸カリウムで酸化されなかった」という内容より「Gは第三級アルコール」と解ります。
- 環状構造
- 三級アルコール
から予測されるGの構造異性体は「3つ」が正解です。その内1つの構造式を描けば完答となります。
受験生としての解説
問1に関して、元素分析は頻出事項なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、ヨードホルム反応も頻出事項なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、「ヨードホルム反応」と「炭素鎖一直線」は不合格者さんでも気づけますし、2つのヒントから正解を導く事も不合格者さんに難しくありません。よって、全ての受験生さんが正解したい問題です。
問4に関して、「二重結合2個持ち」から「臭素原子が4つ付加」も不合格者さんでもギリギリついて来れるレベルなので、合否を分けるほどの難易度ではありません。よって、全ての受験生さんが正解したい問題です。
問5に関して、C原子6個で「二重結合2個持ち」から「2番めと4番目のCに二重結合」は最初に考える事なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問6に関して、基本知識なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問7に関して、「環状構造」を見抜く部分が不合格者さんにはやや難しいレベルです。その後「環状×3級アルコール」から作図する部分は不合格者さんには厳しいでしょう。合格者さんは正解してきます。よって、合否を分ける1問です。
構造決定は九大化学の頻出分野です。厚く対策し、構造決定を得意にしておけば、才能で劣る学生さんでも本問は完答できるようになるレベルです。そして、本問の様な頻出問題、もしくは簡単な問題を正解していけば、九大の合格点を作れます。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:完答したい1問
大問5

講師としての解説
「アミノ酸」からの出題です。
知識の必要性に関して、普通程度です。アミノ酸・タンパク質・検出反応の基本知識を一通り問われています。思考力の必要性に関して、やや簡単です。小問5の計算以外は概ね知識問題です。
問1に関して、知識問題です。アミノ酸・タンパク質に関する語句問題を8つ答えます。アミノ酸に共通して存在する官能基-COOHは「ア:カルボキシ」基といい、同様に共通して存在する-NH2(アミノ基)と「ウ:脱水」縮合してペプチド結合します。アミノ酸は水溶液中において「イ:双性」イオンの形で存在しています。タンパク中のαーアミノ酸の配列順序を「エ:一次」構造といいます。ポリペプチド鎖において比較的せまい範囲で繰り返される、らせん状の「オ:αヘリックス」構造や波型状のβシート構造などの高次構造を「カ:二次」構造といいます。加水分解するとαーアミノ酸のみを生じるタンパク質は「キ:単純」タンパク質、他に糖類や脂質などを生じるものを「ク:複合」タンパク質といいます。
問2に関して、知識問題です。実験結果①に関して、酢酸鉛(Ⅱ)からの黒色沈殿は「PbS」なので、Sを含むアミノ酸「システイン」であることが解ります。実験結果②に関して、濃硝酸との加熱によってベンゼン環がニトロ化されて黄色になっています(キサントプロテイン反応)よって、ベンゼン環を持つアミノ酸「チロシン」と解ります。実験結果③に関して、側鎖に不斉炭素を持つアミノ酸は、与えられた表の中では「システイン」となります。
問3に関して、知識問題です。問2で求めた3つの正解の内、最も分子量が小さいのはシステイン、と表に書いてあります。よって、システインの構造式を描けば正解です。
問4に関して、知識問題です。問2の実験結果②の黄色反応は「キサントプロテイン反応」です。「黄サントプロテイン」と憶えると、楽して記憶を長く維持できます。
問5に関して、思考問題です。実験結果④の結果で生じた化合物Yの分子量を答えます。「臭素酸ナトリウム存在下で反応させる」はシステインのS原子による「ジスルフィド結合」を表しています。よって、化合物Yはシステインから水素分子が1つ外れたものが2つ結合した形です。よって「分子量=397×2-2.00=792」が正解です。
受験生としての解説
問1に関して、アミノ酸・タンパク質の基本知識なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、アミノ酸・タンパク質に関する試薬・反応・構造の基本知識ですが、基本とはいえ不合格者さんに完答はやや難しいです。合格者さんはこの辺りをシッカリ正解してくる部分なので、合否を分ける1問です。
問3に関して、システインの構造式を描くだけですが、それだけで1問成立しているように、不合格者さんはなかなか描けません。合格者さんはキッチリ描ける部分なので、合否を分ける1問です。
問4に関して、キサントプロテイン反応も不合格者さんの一定数が正解できず、合格者さんは確実に拾ってくる部分です。よって、合否を分ける1問より少し簡単な、落とすと痛い1問という感じです。
問5に関して、合格者さんでも少し難しいレベルです。よって、正解できれば他者に差をつける1問となります。
基本が幅広く、やや憶えにくい、アミノ酸・タンパク質からの出題でした。この分野では、トップ高校から九州大学を目指す人の中で「下位の学生さん」が知識不足で失点します。
憶える事が難しいのではなく、勉強する事が難しい分野なので、才能で劣る学生さんにとって逆転チャンスの1問となります。
- 知識:★★★(普通)
- 思考:★★(やや簡単)
- 総合:★★★(普通)
- 短評:才能で劣る学生さんにチャンス
九州大学の化学2015年・平成27年度
大問1
講師としての解説
「周期表」と「原子」からの出題です。
知識の必要性に関して、やや簡単です。小問5までは共通テストと同等か簡単です。小問6「遷移元素の最外殻電子」がやや難しいです。思考力の必要性に関して、やや簡単です。小問7の後半だけ、合格者さんでもやや難しいレベルになっています。
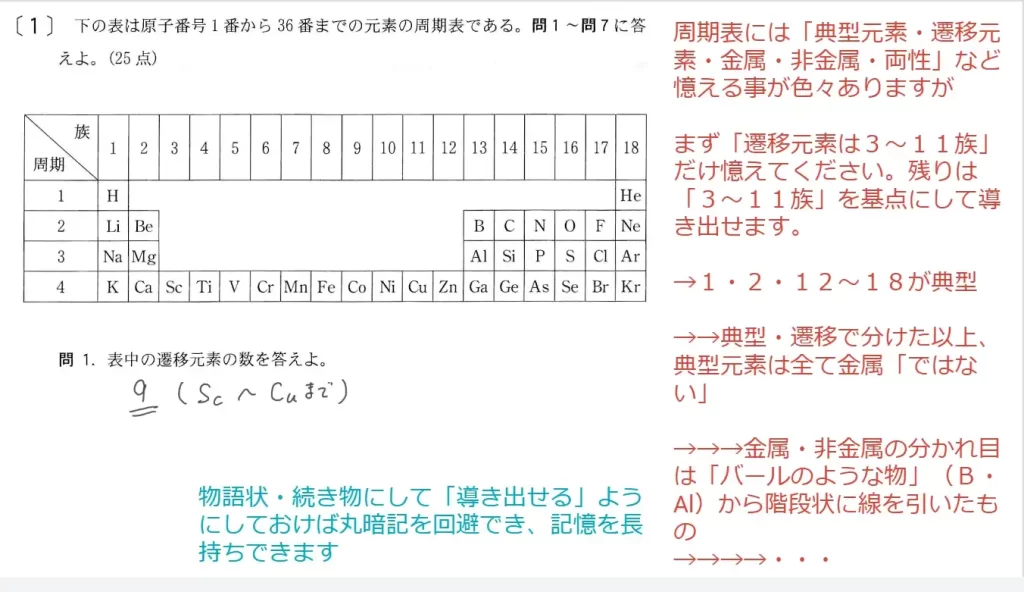
問1に関して、知識問題です。周期表1~4周期の中で、遷移元素は9つ(Sc~Cuまで)が正解です。
問2に関して、知識問題です。第3周期の元素で最も第一イオン化エネルギーが高いのは、最外殻電子が1個の「Na」です。
問3に関して、知識問題です。質量数13の炭素原子に含まれる中性子数は「中性子数=質量数-陽子数(原子番号)=13-6=7」が正解です。
問4に関して、知識問題です。ナトリウムイオンの最外殻電子数はNeと同じ「8」です。陽子数は原子番号のままで「11」が正解です。臭化物イオンの最外殻電子数は「8」です。陽子数は「35」となります。
問5に関して、知識問題です。問題で指定された全ての物質の「電子配置」は同じになりますが、陽子数は原子番号が進むほど多くなり、よって電子を強く引き付けるようになるため、イオン半径が小さくなります。最小は、原子番号が最大となる「Al3+」です。
問6に関して、知識問題です。マンガンの電子配置について、最外殻(N殻)のすぐ内側の電子殻は「ア:M」殻です。「イ:13」個の電子が存在します。
- 典型元素Ca(K殻2個、L殻8個、M殻8個、N殻2個)まではルール通り順番に入る
- 遷移元素(Caの次)に入る段階で「実はM殻に18個入れることが判明」
- よって、Sc(Caの次)からはまたM殻に入っていく
- ただし、CuとCr(ゴロ合わせ:ドクロ)だけは例外で、N殻からM殻への引きずり込みが起きる
- しかし、すぐ次の元素でN殻はカバーされて2個に戻る
真っ当なやり方は「電子軌道(s軌道、p軌道、d軌道)とエネルギー準位を理解すること」ですが、なかなかトップ高校以外の学生さんには難しい部分があります。そこで、とりあえず上記の様に憶えて点数だけは取れる状態にしておき、使いながら仕組み(電子軌道)を学んでいけばよいです。
問7に関して、前半は知識問題、後半は思考問題です。KMnO4におけるMnの酸化数は「Kが+1、O4が-2×4」なので「+7」です。MnCl2におけるMnの酸化数は「Cl2が-1×2」なので「+2」です。(ウ)(エ)に関して、以下のプロセスで正解となります。
- 与式の式量は「39.1x+86.9」
- 与式の過マンガン酸カリウムが1モル水にとけると、xモルのK+が生じ
- また、問題文の値より、実際のK+のモル数は「0.0052 × 250/1000 =0.0013モル」と解る
- よって「1.0/(39.1x+86.9) × x=0.0013」という関係式が成り立ち、x=0.119≒0.12と解る
- 最後に、過マンガン酸カリウムの「酸化数の合計」は0になるため「x+4(1-y)+3y-4=0」より「x=y」となるため「y=0.12」となる
受験生としての解説
問1~問5に関して、共通テストと同等か簡単な問題なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問6に関して、知識問題ですが不合格者さんはやや厳しいレベルです。合格者さんにも一定数の不正解が出るレベルです。
問7に関して、前半の「酸化数」は不合格者さんでも正解してきます。後半の計算問題は難易度が上がっており、合格者さんでも一定数の不正解が出るレベルです。
共通テストと同レベルの小問1~小問5・小問7前半を完答、小問6を正解、小問7後半がすぐ解けそうにないなら早めに見切って試験時間を節約・・・とできれば合格圏内です。才能で劣る学生さんでも苦労なくできるレベルです。
- 知識:★★(やや簡単)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:小問7後半以外を完答したい
大問2

講師としての解説
「気体の溶解度・分圧」からの出題です。
知識の必要性に関して、簡単です。基礎の中でも簡単な部分が出題されています。思考力の必要性に関して、普通程度です。普段の練習において「比の式を立てて解いている学生さん」には普通程度の問題ですが「割合計算で解いている学生さん」にとっては、状況・数値が複雑でやや難しい出題でした。
問1に関して、概ね思考問題です。気体の圧力・水への溶解などに関して答えます。問アに関して、ドライアイス中の二酸化炭素分子は互いに「ア:ファンデルワールス力」で結びついています。これは知識問題です。
問イに関して、単位格子あたりのCO2と1cm^3あたりのCO2で比の式を立てると「1.8×10^-23cm^3 : 44.0 × 4/(6.0×10^23)グラム = 1cm^3 : xグラム」となります。この式を解いて「x≒1.6グラム」が正解です。
問ウに関して、問イの計算と状態方程式を連携し「V=nRt/P=1/(1.0×10^5) × 4/(6.0×10^23) × 10/18 ×10^22 × 8.31×10^3 × 300 ≒ 0.92リットル」が正解となります。
問エに関して、初期濃度c・電離度αとして平衡の式を立てると「HCO3-とH+の濃度が等しい」ことが解ります。よって、以下のプロセスで正解の「0.22モル/リットル」が出ます。
- Ka=[HCO3-][H+]/[CO2]=[H+]^2/[CO2]より
- [CO2]=[H+]^2/Ka=(1.0×10^-3.50)^2/4.5×10^-7≒0.22モル/リットル
問オに関して、問題文より「CO2が27℃、1.0×10^5Paで0.831リットル水に溶けた」と書いてあります。よって、溶けていたモル数は「n=PV/RT=1.0×10^5×0.831/(8.31×10^3×300) = 0.0333モル/リットル」と解ります。今、ヘンリーの法則より「CO2の圧力と水に溶けているCO2の濃度」は比例関係となるので、問エの状態(水に溶けているCO2濃度0.222モル/リットル)の圧力は「1.0×10^5× 0.222/0.0333 ≒6.7×10^5Pa」となり、これが正解です。
問2に関して、知識問題です。二酸化炭素の電子式を描くと正解です。
問3に関して、知識問題です。固体が「液体を経ないで直接気体になること」を「昇華」といいます。
問4に関して、知識問題です。図bに示された形状を「面心立方格子」といいます。
受験生としての解説
問1に関して、問アは不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
問イ・問ウは、不合格者さんの一定数が正解できず、合格者さんは正解してくるレベルです。よって、合否を分ける1問より少し簡単です。
問エ・問オは、不合格者さんには難しく、合格者さんは正解してくるレベルなので、合否を分ける1問です。
問2~問4に関して、共通テストと同等か簡単なレベルなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。九大化学では「電子式を描かせるだけの問題」がよく出題されているので、ウッカリ忘れやすい分野ですが注意しておいてください。
- 知識:★(簡単)
- 思考:★★★(普通)
- 総合:★★(やや簡単)
- 短評:問2~問4は正解したい
大問3
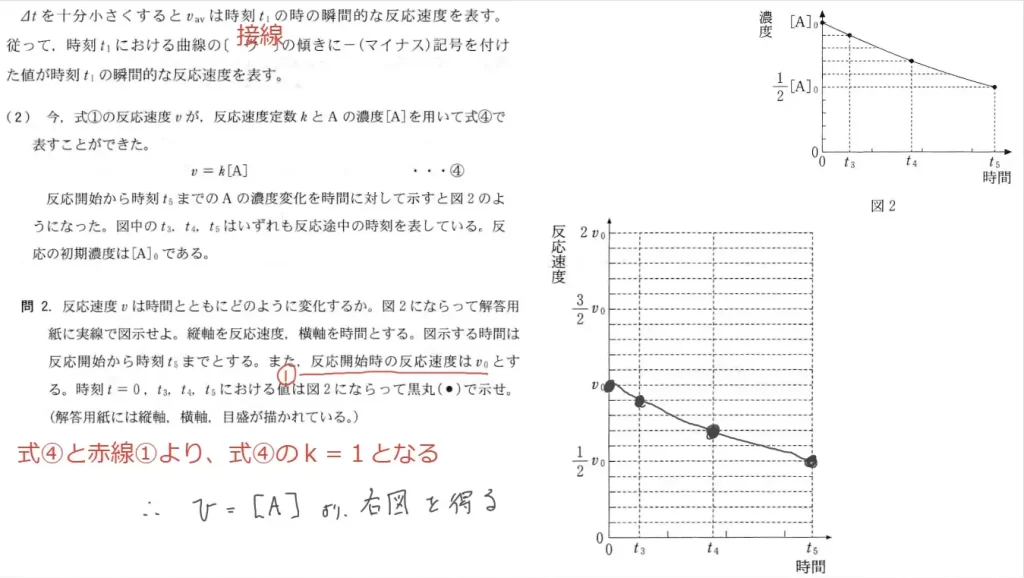
講師としての解説
「反応速度」からの出題です。
知識の必要性に関して、ほぼ不要です。考えて解く問題です。思考力の必要性に関して、やや強く必要です。立式、作図、式変形、数値代入、増減表、引っ掛けの様な半減期など、1つ1つは難しくないですがバラエティに富んだ出題です。
問1に関して、思考問題です。問アに関して、「平均速度=|濃度変化量|÷反応時間」となります。よって、「-([A]2-[A]1) ÷(t2-t1)」が正解となります。問イに関して、「Δ[A]=[A]2-[A]1、Δt=t2-t1」なので、問1の式に代入して「-Δ[A]/Δt」が正解となります。よって、Δtを極限まで小さくした時、瞬間的な反応速度は「ウ:接線」の傾きにマイナスを付けた値となります。
問2に関して、思考問題です。式④と問題文の「反応開始時の反応速度はv0」より、式④のk=1となります。よって式④は「v=[A]」となるため、問題文のグラフの濃度の点をそのまま解答用紙のグラフにプロットし、各点をなめらかにつないだグラフが正解となります。
問3に関して、思考問題です。[A]0 → 1/2[A]0に関して、濃度が半分になっているので、要する時間は半減期1回分「t1/2」が正解です。同様に、[A]0 → 1/4[A]0は半減期2回分なので「2t1/2」が正解です。
問4に関して、思考問題です。圧力変化を考察する問題なので、まず増減表を書きましょう。すると左辺の濃度が1/8まで低下した事がわかります。今、この反応は問題文より「体積一定・温度一定」と宣言されているため、圧力と物質量が比例関係にあります。よって「左辺の圧力が1/8になった」というのは「左辺の濃度が1/8になった」ことを表しており、式④より「v=1/8 × v0」よって正解は「v/v0=1/8」となります。
問5に関して、思考問題です。濃度が1/8になったという事は「濃度が半分になる事」が3回起きた、と言い換えることができます。よって「半減期3回分」が正解なので「3t1/2 = 6時間」より「t1/2 =2時間」が正解となります。
受験生としての解説
問1に関して、濃度変化と反応速度に関する数学系の問題ですが、九大数学よりも簡単なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、言われてみれば簡単なのですが、見た目より難しい問題です。入試本番の緊張と時間不足を考慮すると、不合格者さんの一定数は不正解になるレベルです。よって、合否を分ける1問より少し簡単、という感じです。
問3に関して、半減期の計算なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、増減表から圧力を経て物質量比に帰着させることは、不合格者さんには厳しく、合格者さんでも難しいです。よって、正解できれば他者へ差をつける1問です。
問5に関して、本問自体は簡単ですが、本問に参加するためには問4の正解が必要です。よって、問4とセットで、他者に差をつける1問となります。問4が正解できた人へのボーナス点です。
- 知識:★(簡単)
- 思考:★★★★(やや難しい)
- 総合:★★★(普通)
- 短評:小問2で脱落する事を防ぎたい
大問4

講師としての解説
「構造決定」からの出題です。
知識の必要性に関して、やや難しいです。有機化合物全般の盤石な知識が必要な事に加え、浸透圧の式も使います。思考力の必要性に関して、やや難しいです。問題文で与えらエた式量から物質を逆算したり、問6では問1~5で暑かった物質を総合的に応用します。
問1に関して、思考問題です。問題文の「油状の」という言葉よりAは「芳香族化合物」と思われます。さらに問題文の「水酸化ナトリウムを加えて加熱するとAが生じた」という内容より、Aは「弱塩基の遊離」によって発生したと考えられます。よって、Aは「芳香族」かつ「弱塩基」という事で、おそらく「アニリン」だろうと予想できます。その上で、問1の問題文に「(Aの)分子量は93」と書いてあります。今「93-C6H5(式量77)=16」であり、式量16は「-NH2」に相当するのでAは「ベンゼン環+NH2=アニリン」が正解です。
問2に関して、思考問題です。構造決定の定番「元素分析」がここで出ました。元素分析の結果、Bの組成式は「C6H6O」と解り、この時点で「Bはフェノール」とほぼ決まりです。問題文に「CO2を投入したらBが生じた」という内容が書いてあり、これは「弱酸の遊離」によるフェノールの遊離なので、確定です。Bのナトリウム塩とはナトリウムフェノキシド、さらに高圧CO2を加えてサリチル酸ナトリウム、そして希硫酸を加えて酸に戻したCが「サリチル酸」で確定です。
問3に関して、知識問題です。サリチル酸とメタノールで「サリチル酸メチル」が生成します。
問4に関して、思考問題です。問題文の「Dにホルムアルデヒドを反応させると、水に不溶な繊維原料」という内容より、Dは「ポリビニルアルコール」で確定です。Dの分子量に関して、ファントホッフの式(πV=nRT)を変形して「M=wRT/πV=1.00×8.31×10^3×300/(8.31×1.0)=3.00×10^5」が正解となります。
問5に関して、思考問題です。「化合物A(アニリン)と化合物EからFが生じる」という内容なので、Fは「アニリン由来の物質」と解ります。問題文より「Fの分子量は135」と書いてあるので、ここからベンゼン環(77)を引くと「135-77=58」となり、側鎖の式量は58(-NHCOCH3)と解ります。よって、Fは「ベンゼン環+NHCOCH3=アセトアニリド」で確定です。そして「A(アニリン)+E=F(アセトアニリド)」なので、Eは「酢酸」で確定です。
問6に関して、思考問題です。まず、加水分解後の物質が
- A(アニリン)
- B(フェノール)
- C(サリチル酸)
なので、混合物Xには
- アセトアニリド
- 酢酸フェニル
- アセチルサリチル酸
が含まれていたと考えられます。そして、E(酢酸)とD(ポリビニルアルコール)が生成したので、高分子化合物は「ポリ酢酸ビニル」と予想できます。そして、加水分解後に酢酸とエタノールを生じている事から「酢酸エチル」も含まれていたと予想できます。
これらをまとめた「酢酸エチル、酢酸フェニル、アセチルサリチル酸、ポリ酢酸ビニル」が正解となります。
受験生としての解説
問1に関して、不合格者さんには少し難しいレベルです。不正解になる人と「分子量93」に気付いてギリギリ正解できるぐらいのレベルです。合格者さんは正解してきます。よって、合否を分ける1問です。
問2に関して、問1より簡単で、問1の正解が無くても参加できます。よって、不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
問3に関して、サリチル酸は本分野の主軸となる物質なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、「ホルムアルデヒドと反応して水に不溶」から「アセタール化→Dはポリビニルアルコール」と導く事は、不合格者さんにはやや難しいです。合格者さんにも一定の不正解が出るレベルなので、正解できれば他者に差をつける1問です。
問5に関して、式量58から側鎖(NHCOCH3)を見抜くことは合格者さんでも難しいです。よって、正解できれば他者に差をつける1問です。
問6に関して、ここまでの話全体を理解し、全ての情報を総合的に応用する必要があるため、合格者さんでも難しいレベルです。医学科の合否を分ける問題です。
- 知識:★★★★(やや難しい)
- 思考:★★★★(やや難しい)
- 総合:★★★★(やや難しい)
- 短評:問4まで正解したい
大問5

講師としての解説
知識の必要性に関して、やや簡単です。基本知識・有名知識ばかりで構成されています。思考力の必要性に関して、やや簡単です。計算問題も基本レベルです。
問1に関して、知識問題です。高分子に関する語句問題を4つ答えます。高分子を構成する小さな分子を「ア:単量体」といい、単量体が「イ:付加」反応を起こす付加重合と、縮合を使った「ウ:縮合重合」があります。デンプンやセルロースは「エ:水」が取れる縮合重合によって形成されます。
問2に関して、知識問題です。上記、グルコースやセルロースに使われる結合を「グリコシド結合」といいます。
問3に関して、知識問題です。重合体の繰り返し回数の事を「重合度」といいます。
問4に関して、知識問題です。スクロースを加水分解すると、グルコースと「フルクトース」の等量混合物となります。
問5に関して、思考問題です。ポイントは問題文の「グルコースと同様に還元性を示す」です。よって、先端がアルデヒド基になった形を描けば正解です。
問6に関して、知識問題です。ポイントは問題文の「赤色沈殿」です。還元性の話が続いた上で赤色沈殿なので、正解は「フェーリング液」です。沈殿の組成式は「Cu2O」です。
問7に関して、思考問題です。1モルのスクロースから、1モルのグルコースと1モルのフルクトースが生じるため、2モル分の還元性を持ちます。よって、スクロースのモル数はCu2Oの半分となるため「70.0/143 × 1/2 × 342 ≒ 83.7g」となり、元のスクロースは100g存在していたため、正解は「83.7%」となります。
受験生としての解説
問1~問4に関して、高分子と糖類の基本知識を問う出題なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問5に関して、4つの図と問題文の「還元性」からアルデヒド基を導くことは不合格者さんでも成してきます。よって、全ての受験生さんが正解したい問題です。
問6に関して、本問も有名な基本知識なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問7に関して、ようやく本番スタートという感じですが、本問も「序盤の小問レベル」の計算問題です。よって、不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
- 知識:★★(やや簡単)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:完答したい1問
九州大学の化学2014年・平成26年度
大問1

講師としての解説
「気体」と「蒸気圧」からの出題です。
知識の必要性に関して、普通程度です。難しい知識は必要ありませんが、基本の柔軟な運用を問われています。思考力の必要性に関して、普通程度です。1問あたりはやや簡単なレベルですが、後半になるほど積み重なって難易度が上がります。
問1に関して、思考問題です。フラスコの中のAに関する状態方程式(PV=nRT)より「n=PV/RT=1.01×10^5×0.831/(8.31×10^2×373) ≒2.7×10^-2モル」が正解です。
問2に関して、思考問題です。問題文にて「底に溜まった質量は1.15g」と与えられており、設問分で「Aの密度は0.789g/cm^3」と与えられています。よって、求める体積x(ml)として「密度=質量/体積=1.15/x=0.789」これを解いて「x≒1.5ml」が正解です。
問3に関して、思考問題です。フラスコ内のAが液体になったという事は、Aの蒸気圧は問題文で与えられた「6.10×10^3Pa」になっています。よって、A(気体状態)の状態方程式より「n’=PV/RT=6.10×10^3×0.831/(8.31×10^3×293)=0.00208モル」と、A(気体状態のモル数)が判ります。よって、「求める割合=(Aの全モル数-気体になったモル数)÷Aの全モル数=(0.0270-0.000208)÷0.0270≒92%」が正解です。
問4に関して、思考問題です。問3より、92.2%のAが液化し、その質量は1.15gでした。よって100%の(気体+液体の)Aの質量を求める事ができます(1.15 × 100%/92%=1.24g)そして、そのモル数は問1より0.0270モルと判明しています。よって、「分子量=質量/モル数」に代入すると「M=1.24 ÷ 0.0270=45.9≒46」が正解となります。
問5に関して、思考問題です。まず、最低でもC・H・Oが1つずつ必要です。よって「12+1+16=29」は不可避の値となります。よってこの値を分子量から引き(46-29=17)残った「17の組み合わせ」を考えてみましょう。
- Oが1個+Hが1個 → CH2O2(ホルムアルデヒドなど)
- Cが1個+Hが5個 → C2H6O(エタノールなど)
となり成立します。よって、上記2つが正解です。
問6に関して、まず、設問分に「二重結合や環状構造は含まれない」と書いてあるので、問5の2つの候補の内「CH2O2」は不可と解ります。よってAの分子式は「C2H6O」なので、Aは「エタノールかジメチルエーテル」となります。今、エタノール沸点は78℃、ジメチルエーテルは-24℃であり、問題文に「物質Aは20℃で液体」という内容が書いてあります。よって、Aは「エタノール」で確定です。
受験生としての解説
問1に関して、状態方程式を立てて解くだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、質量と密度が離れた場所に書いてあるため、不合格者さんの中には気づけない人もいるでしょう。しかし、概ね不合格者さんでも乗り越えてくるレベルなので、全ての受験生さんが正解したい問題です。
問3に関して、「割合」がからんできたので、不合格者さんにはそろそろ厳しくなってきました。合格者さんは正解してくるレベルなので、合否を分ける1問です。
問4に関して、1問1問は普通レベルですが、積み重なってきたことにより不合格者さんには徐々に厳しいレベルになってきました。合格者さんはまだまだついて来れるレベルなので、合否を分ける1問です。
問5に関して、不合格者さんでも正解できるレベルですが、本問に参加するには問4の正解が必要となります。よって、問4とセットで合否を分ける1問となります。
問6に関して、エタノールの沸点(78℃)とジメチルエーテルの沸点(-24℃)をある程度知っておく必要があるため、合格者さんでも厳しい問題です。化学が得意な学生さんなら「エテールの沸点は低い」事を知っているので、正解できるでしょう。よって、正解できれば他者に差をつける1問となります。
割合・密度・蒸気圧が絡むためやや重い作りですが、1問1問は難しくないので粘り強くついて行きたい大問です。小問4まで頑張れた人には、小問5がおそらくボーナス点になりますし、小問6も正解できないとしても「エタノール or ジメチルエーテル」の確率50%ボーナス得点の様な問題です。これを拾って他者に差をつけたいところです。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:小問4+小問5のセット得点を取りたい
大問2
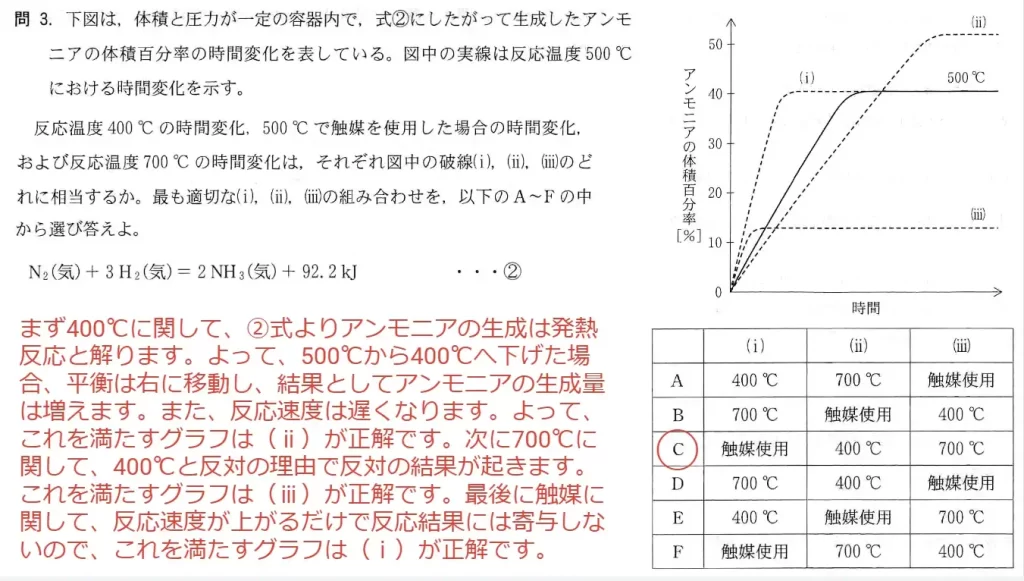
講師としての解説
「アンモニア」と「熱化学方程式、化学平衡、中和」からの出題です。
知識の必要性に関して、普通程度です。ヘスの法則、ルシャトリエの原理、濃度計算などよく使う知識を問われています。思考力の必要性に関して、普通程度です。問2~問4にかけて、熱化学、化学平衡、濃度計算、と入れ替わる分野に対応する必要があります。1問あたりはやや簡単です。
問1に関して、硫酸アンモニウムは強酸+弱塩基でできているため、水溶液は「ア:弱酸性」を示します。これは電離した「イ:アンモニウム」イオンの一部が水に「ウ:H+」を与えて「エ:アンモニア」になろうとする傾向があるためです。
問2に関して、思考問題です。設問文の情報より以下の4式を立てられます。
- CH4(気)+2O2(気)=CO2(気)+2H2O(液)+892kJ
- H2(気)+1/2O2(気)=H2O(液)+286kJ
- CO(気)+1/2O2(気)=CO2(気)+283kJ
- H2O(液)=H2O(気)-44.0kJ
正解を導く式は上記の「1式-2式×3-3式-4式」で作れるため、「892-286×3-283-(-44.0)=-205kJ」で正解です。
問3に関して、思考問題です。まず400℃に関して、②式よりアンモニアの生成は発熱反応と解ります。よって、500℃から400℃へ下げた場合、平衡は右に移動し、結果としてアンモニアの生成量は増えます。また、反応速度は遅くなります。よって、これを満たすグラフは(ⅱ)が正解です。次に700℃に関して、400℃と反対の理由で反対の結果が起きます。これを満たすグラフは(ⅲ)が正解です。最後に触媒に関して、反応速度が上がるだけで反応結果には寄与しないので、これを満たすグラフは(ⅰ)が正解です。
問4に関して、思考問題です。アンモニアと硫酸の中和に関して「放出したH+のモル数=受け取ったH+のモル数」の式を立てると「2×0.150× x/1000 =1×0600× 60.0/1000」となり「x=1.20×10^2(ml)」となります。これが正解の1つです。
次に、硫酸アンモニウムの濃度に関して、上記の計算結果より、中和後の溶液の体積は「60.0+1.20×10^2=180ml」となります。生成する硫酸アンモニウムの物質量は、反応したアンモニア物質量の1/2倍なので「0.600× 60.0/1000 × 1/2× 1000/180=1.00×10^-1モル/リットル」が正解となります。
受験生としての解説
問1に関して、アンモニアの電離に関する共通テストの様な出題なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、熱化学方程式の足し引きには複雑で難しい問題がありますが、本問は最も簡単な部類なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、共通テストと同等の出題なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、前半「中和に必要な硫酸の体積」は共通テストと同等の出題なので、不合格者さんでも正解してきます。後半「硫酸アンモニウムの濃度」は共通テストより少し難しい程度なので、やはり不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
アンモニアを軸として分野が矢継ぎ早に変わるため、特別簡単でもなく、難しくもありません。しかし、全体としてやや時間のかかる作りとなっているため、才能に恵まれたトップ高校の学生さんでも、練習不足な場合は「時間消費」で足元を救われます。
逆に言えば、才能で劣る学生さんにとって逆転チャンスの1問です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:完答したい1問
大問3

講師としての解説
「系統分離」からの出題です。
知識の必要性に関して、やや難しいです。1つ1つの知識は簡単ですが、無機化学の幅広い知識を問われています。思考力の必要性に関して、やや簡単です。問4「溶解度積の計算問題」まで含めて、ほぼ全て知識問題と言える内容です。知識の運用でやや思考力を使います。
問1に関して、知識問題です。まず操作1に関して、投入された希塩酸から塩化物イオンが生じます。この塩化物イオンで沈殿するのは「Ag+、Hg2+、Pb2+」なので、ここでは「B:AgCl」が沈殿します。続いて操作2に関して、溶液が酸性の状態で硫化水素(硫化物イオン)が投入されています。「酸性時」に、この硫化物イオンで沈殿するのは「Sn2+、Pb2+、Cu2+、Hg2+、Ag+」なので、ここでは「D:CuS」が沈殿します。操作3に関して、アンモニアの投入によって溶液にOH-が生じ、これが「アルカリ金属・アルカリ土類金属、以外の金属」と結びついて水酸化物沈殿を生じます。よって「F:Al(OH)3、Fe(OH)3」となります。最後に操作4に関して、炭酸アンモニウムの投入によって溶液中には「炭酸イオン、CO3 2-」が生じます。この炭酸イオンで沈殿するのは「Ba2+、Ca2+」なので、ここでは「H:CaCO3」が沈殿します。
問2に関して、知識問題です。過剰な水酸化ナトリウムに錯イオンを生じて溶ける元素は「Al、Zn、Sn、Pb」です。よって本問では[Al(OH)4]-となります。
問3に関して、知識問題です。希硝酸と硫化水素の半反応式を合体させれば正解となります。
- HNO3 + 3H+ +3e → NO + 2H2O
- H2S → 2H+ + S + 2e
- 1×2+2×3より
2HNO3 + 3H2S → 2NO + 4H2O + 3S
問4に関して、思考問題です。沈殿B(AgCl)は水にわずかに溶けて「AgCl → Ag+ + Cl-」と電離します。この際、Ag+とCl-は1:1の関係で電離するため、溶解度積に関して「溶解度積=[Ag+][Cl-]=[Ag+]^2=2.0×10^-10」となります。よって「[Ag+]=√2.0 × 10^-5 ≒ 1.4×10^-5」が正解となります。
問5に関して、知識問題です。カリウムの炎色反応は、ゴロ合わせ「リヤカー無きK村(Kがカリウム、村が紫)」より「紫色」が正解です。
受験生としての解説
問1に関して、系統分離は不合格者さんにはやや厳しいレベルです。合格者さんは安定して高得点を出す部分なので、合否を分ける1問です。
問2に関して、過剰NaOHの沈殿は不合格者さんでも正解できますが、本問に参加するためには問1の正解が必要です。よって、問1とセットで合否を分ける問題です。
問3に関して、半反応式を合体させるだけの基本知識ですが、不合格者さんの一定数が不正解になるレベルです。合格者さんは正解してくるので、合否を分ける1問です。
問4に関して、溶解度積の問題は不合格者さんには少し難しいレベルですが、本問に参加するためには問1の正解が必要となっています。よって、問1とセットで合否を分ける1問となります。
問5に関して、炎色反応は共通テストレベルなので不合格者さんでも正解してきますが、本問に参加するためには問1の正解が必要です。よって、問1とセットで合否を分ける1問となります。
- 知識:★★★★(やや難しい)
- 思考:★★(やや簡単)
- 総合:★★★(普通)
- 短評:0点か満点に分かれやすい
大問4

講師としての解説
「構造決定」からの出題です。
知識の必要性に関して、普通程度です。芳香族化合物、ヨードホルム反応に関する知識が必要です。思考力の必要性に関して、普通程度です。ラスト小問6の正解を目指すなら「やや難しい」です。
問1に関して、思考問題です。問題文の「いずれもベンゼン環を1個持ち」より、化合物Aの側鎖に当たる部分は「C9H12O - C6H5(ベンゼン環) = C3H7O」となります。つまり「二重結合が無い」と解ります。さらに問題文より「(Aに)ヨウ素と水酸化ナトリウムを反応させると化合物E」と書いてあるので、Aは「二重結合ナシのヨードホルム反応陽性 → CH3CHOH持ち」と解ります。さらに問題文より「(Aが変化した)Eを過マンガン酸カリウムで酸化させるとC8H6O4の化合物F」と書いてあり「O原子を4つ持つ → つまり、酸化されて-COOHになる側鎖を2つ持つ」と解ります。ここでAの構造が確定します「CH3-ベンゼン環-CH(OH)CH3」が正解です。
問2に関して、知識問題です。すでに構造が判っている化合物Aが、ヨードホルム反応によって変化した姿を問われています。ヨードホルム反応後の物質は以下の形となります。
- CH3が本体からはずれ
- 残ったCがカルボキシ基となり
- カルボキシ基のHが取れてNaがつく(中和反応)
よって「CH3-ベンゼン環-COONa」が正解となります(COOHも可)
問3に関して、知識問題です。(化合物Aのヨードホルム反応で生じた)化合物Eを酸化すると化合物Fとなり、Fは「(ア)と反応させるとポリエチレンテレフタラート」より
- Fは「テレフタル酸」で確定
- よって(ア)は「エチレングリコール」で確定
となり、正解です。
問4に関して、思考問題です。問題文の「(Bを)酸化したところ、反応しなかった」より、Bは3級アルコールと解ります。また、問題文の「B以外は不斉炭素原子をもつ」より、Bは不斉炭素原子を持たないと解ります。以上より、Bの構造は「ベンゼン環-C(CH3)2OH」が正解です。
問5に関して、思考問題です。ここまでの流れにより、化合物Cは
- 不斉炭素原子を持つ
- 1級アルコール
と判っているため、構造は「ベンゼン環-CH(CH3)CH2OH」で正解となります。
問6に関して、ここまでの流れより化合物Dは
- 不斉炭素原子を持つ
- 2級アルコール
と判っています。ここから想像できるDの構造は
- ベンゼン環+側鎖が1本:-CH2CH(OH)CH3、-CH(OH)CH2CH3の2つ
- ベンゼン環+側鎖が2本:「CH3と-CH(OH)CH3」のオルト位・メタ位の2つ
よって、合計4種類が正解となります。
受験生としての解説
問1に関して、不合格者さんには難しい問題です。合格者さんは正解してくるレベルなので、合否を分ける1問です。
問2に関して、不合格者さんには厳しいレベルです。合格者さんでも「ヨードホルム反応後の形」は一定数が知らないレベルです。よって、正解できれば他者に差をつける1問となります。
問3に関して、基本的に問1からの続き物なので、本問に参加するには問1の正解が必要です。しかし、問題文「Aをアと反応させるとポリエチレンテレフタラート」の記述より、本問単体で解くことが可能となっています。よって、不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
問4に関して、3級アルコールは形が解りやすいので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問5に関して、問1~問4の内容を部分的に使って正解する問題なので、不合格者さんには厳しいレベルです。合格者さんは正解してくるので、合否を分ける1問です。
問6に関して、合格者さんでも難しいレベルです。よって、正解できれば他者に差をつける1問です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:小問5まで正解したい
大問5A
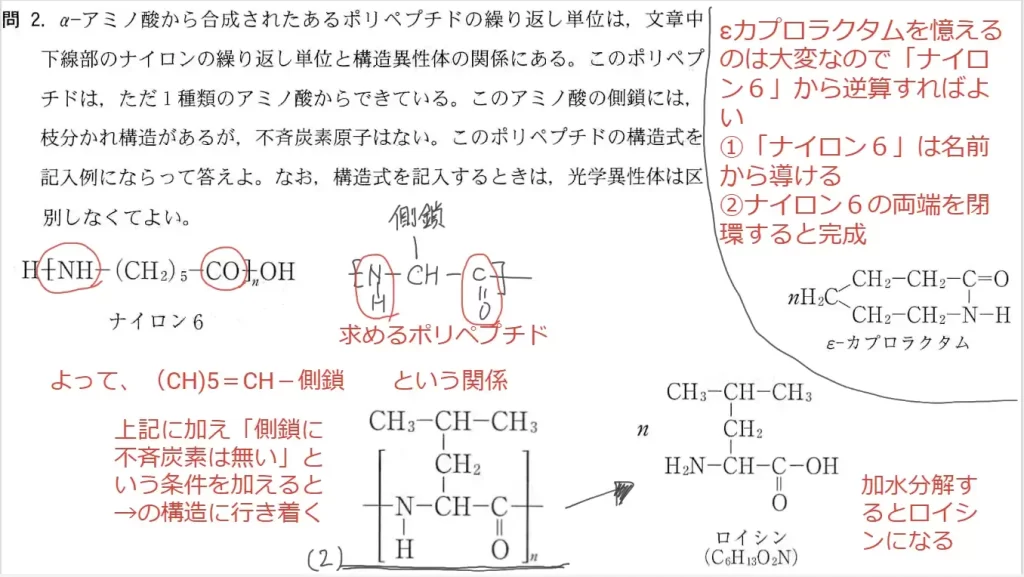
講師としての解説
「高分子化合物」からの出題です。
知識の必要性に関して、普通程度です。高分子化合物の基礎知識で足ります。思考力の必要性に関して、やや難しいです。問2の繰り返し単位の構造、問3アセチル基の割合問題などは難しいです。逆に問4・問5は簡単です。
問1に関して、知識問題です。高分子に関する語句問題を3つ答えます。合成高分子にはアミド結合や「ア:付加」重合で得られる化合物があります。一方タンパク質は天然高分子であり、多数のαアミノ酸が「イ:縮合」重合した化合物です。この配列順序をタンパク質の「ウ:一次」構造といいます。
問2に関して、思考問題です。求めるポリペプチドとナイロン6が構造異性体の関係なので
- ナイロン6の「(CH2)5」
- ポリペプチドの「CH-側鎖」
上記2者の各原子数が等しいと解ります。ここに問題文の「側鎖に不斉炭素原子は無い」を加えると、求めるポリペプチドは「ロイシンをペプチド結合したもの」と解ります。よって、この構造式を描くと正解です。
- ナイロン6は構造を名前から導き出せます(6はC原子6個の意味)
- εカプロラクタムからナイロン6ができる事は有名な暗記事項です
- よって、ナイロン6の構造を名前から導き、その両端の「CO」と「NH」をつないで閉環すれば、それがεカプロラクタムです
問3に関して、思考問題です。まず、重合に使われているnは任意の値なので「n=1」でも成り立たねばなりません。そこで、n=1を代入し「分子1個、または1モル」で考えると簡単になります。
- ポリ酢酸ビニル1モル:86グラム
- ポリビニルアルコール1モル:44グラム
- OCOCH3をOHに100%入れ替えると「-42グラム」
- 実際は70%入れ替えなので「-42×70%=-29.4グラム」
- よって「(86-29.4)/86=65.81%≒66%」で正解
問4に関して、思考問題です。100個の部屋に20種類のアミノ酸が自由に入れるので「20の100乗」通りが正解です。
問5に関して、思考問題です。グリシンの数をxと置くと「xグリシン+(10-x)アラニン-9H2O =686」となり、これを解いて「x=3」です。よって、ポリペプチド1モルから3モルのグリシンが得られます。問題ではポリペプチド2モルなので「75(グリシンの分子量)×3×2=450グラム」が正解となります。
受験生としての解説
問1に関して、高分子の語句問題なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、合格者さんでも難しいレベルです。よって、正解できれば他者に差をつける1問となります。
問3に関して、アセチル基の割合計算は不合格者さんには厳しく、合格者さんは正解してくるレベルです。よって、合否を分ける1問です。
問4に関して、九大数学の「場合の数・確率」の方が難しいので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問5に関して、連立方程式で正解できるため、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問1・問4・問5は簡単なので落とせない問題です。問3「アセチル基の割合問題」は難関の頻出、九大でも繰り返し出題されています。問2は時間さえあれば難しくないですが、短い試験時間なので不正解も仕方ないところです。
- 知識:★★★(普通)
- 思考:★★★★(やや難しい)
- 総合:★★★(普通)
- 短評:完答したい1問
大問5B

講師としての解説
「酵素」と「糖類」と「油脂」からの出題です。
知識の必要性に関して、普通程度です。酵素・高分子・油脂と幅広い基礎知識を問われています。思考力の必要性に関して、普通程度です。ケアレスミスが起きやすいので慎重に計算を進める必要があります。
問1に関して、知識問題です。酵素に関する語句問題です。酵素が決まった気質にしか働かない性質を「ア:基質特異性」といい、この反応を起こす場所を「イ:活性」部位といいます。酵素の反応速度を最大にする温度を「ウ:最適温度」といいます。例えば、グルコースのβグリコシド結合を加水分解する酵素を「エ:セルラーゼ」といいます。また、リパーゼは油脂を3分子の脂肪酸と1分子の「オ:グリセリン」に分解します。
問2に関して、知識問題です。βグルコース2分子が結合した化合物は「セロビオース」が正解です。
問3に関して、知識問題です。グルコースの鎖状構造は、構造式右肩部のヘミアセタール構造がはずれてOがOHになり、1位の炭素がアルデヒド基になったものが正解です。
問4に関して、知識問題です。トリグリセリドの強塩基による加水分解を「けん化」と言います。
問5に関して、思考問題です。リノール酸はステアリン酸(C17H35COOH)から数えて3番めの高級脂肪酸なので、二重結合を2個含みます。よって、H原子が4つはずれたC17H31COOH「分子量280」が正解です。同様の方式で、エイコサペンタエン酸は「C19H39COOH」からH原子10個(二重結合5個分)はずれたC19H29COOH「分子量302」が正解です。
問6に関して、思考問題です。まず、トリグリセリドAの分子量を求めましょう。グリセリン+リノール酸+エイコサペンタエン酸+ステアリン酸-3H2Oなので「分子量904」となります。今、この油脂1モルにH2分子が7モル付加できるので、トリグリセリドBは「分子量918」となります。よって、比の式「A:B=904:918=11.3グラム:xグラム」が立つので、これを解いて「x≒1.15×10グラム」が正解となります。
受験生としての解説
問1・問2・問4に関して、基本知識なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、グルコース鎖状構造の作図は不合格者さんの一定数が不正解になるレベルです。合格者さんは正解してくるので、合否を分ける1問より少し簡単な問題となります。
問5に関して、二重結合の数が問題文に書いてあるため、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:完答したい1問
九州大学の化学2013年・平成25年度
大問1

講師としての解説
「原子」と「金属」からの出題です。
知識の必要性に関して、やや簡単です。概ね共通テストと同等です。思考力の必要性に関して、ほぼ不要です。知識問題です。
問1に関して、知識問題です。原子に関する語句問題を3つ答えます。原子から電子を1つ取り去るのに必要なエネルギーを「ア:第一イオン化エネルギー」といいます。原子に電子を1つ付加した時に放出されるエネルギーを「イ:電子親和力」といいます。また、化合物間の結合において、電子を引き寄せる強さを「ウ:電気陰性度」といいます。
問2に関して、知識問題です。第3周期の酸化物においてイオン結合で結ばれているもの(金属+非金属の関係)は「Na2OとMgO」が正解です。また、共有結合で結ばれているもの(非金属+非金属の関係)は「P4O10、SiO2、SO3」です。これらの中から酸性酸化物(非金属の酸化物)は「P4O10、SiO2、SO3」です。
問3に関して、知識問題です。(カ)~(ケ)に「金属」か「非金属」の言葉を入れていきます。一般に、電気陰性度の大きな元素は「カ:非金属」の性質を示し、小さな元素は「キ:金属」的な性質を示します。同周期の元素では、原子番号が大きくなるほど「ク:非金属」的な性質を有し、同族の元素では周期表の下に行くほど「ケ:金属」的な性質を示します。
問4に関して、知識問題です。「O・S・Ca・As・Se」の中で金属性質が最も大きな元素は、唯一の金属である「Ca」です。また、金属の性質を表すものとして
- C:延性・展性
- D:塩基性酸化物
- E:熱・電気の伝導性
が正解となります。
受験生としての解説
問1に関して、原子の基本知識なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、イオン結合・共有結合の条件は不合格者さんでも正解してきます。酸性酸化物の条件は不合格者さんの一定数が不正解になるレベルです。合格者さんは正解してくるレベルなので、概ね全ての受験生さんが正解したい問題です。
問3に関して、周期表の金属・非金属の1例を挙げるだけで正解できるので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、金属の性質は共通テストと同等なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★★(やや簡単)
- 思考:★(簡単)
- 総合:★(簡単)
- 短評:完答したい1問
大問2

講師としての解説
「酸化還元」からの出題です。
知識の必要性に関して、やや簡単です。銅と酸化還元に関して、共通テストと同等の知識で正解できます。思考力の必要性に関して、やや簡単です。酸化還元の計算問題も共通テスト同等です。
問1・問2に関して、知識問題です。銅に関する語句問題を10個答えます。周期表11族、赤みのある金属は「ア:銅」です。銅と濃硝酸を反応させると「イ:NO2」が生じ、この気体は「イ:下方」置換で捕集します。続いて、銅と希硝酸を反応させると「B:NO」が生じ、この反応では銅が「ウ:還元」剤、希硝酸が「エ:酸化」剤としてはたらいています。銅と熱濃硫酸を反応させると「C:SO2」が生じ、これが酸素と反応して「D:SO3」を生じます。硫酸銅水溶液の色は「オ:青」色です。この水溶液を電気分解すると、陽極から「E:O2」が得られます。
問3に関して、知識問題です。銅と希硝酸の反応式は「3Cu+8HNO3 → 3Cu(NO3)2+4H2O+2NO」です。
問4に関して、知識問題です。ルシャトリエの原理に関する問題なので、熱化学方程式を立て見やすくし、ケアレスミスを防ぎます。「2SO2+O2=2SO3+QkJ(Q>0)」です。各選択肢の平衡への影響は以下の通り。
- 触媒を加えると反応速度が上がりますが、反応結果には作用しません
- 与式は発熱反応なので、温度を上げると平衡は左へ移動します
- 加圧すると圧力を下げる方向、つまり平衡は右へ移動します
- 酸を加えると酸素を消費する方向へ、つまり平衡は右へ移動します
- 温度・体積一定でアルゴンを加えると全圧が上がりますが、反応式の各気体の分圧は一定なので平衡は動きません。
問5に関して、思考問題です。まず、陽極・陰極で起きる反応式を確認します。
- 陽極:2H2O → 4H+ + O2 +4e
- 陰極:Cu2+ + 2e → Cu
上記より、電子が4モル流れると「O21モル・Cu2モル」が生じるとわかります。よって、求める銅のモル数は発生O2の2倍となるため「4.48×10^2×10^3/22.4 × 2 × 63.6 ≒ 2.54グラム」が正解です。
受験生としての解説
問1・問2・問3に関して、銅+酸のまとめ問題は基本知識ですが、不合格者さんの一定数が不正解になる部分です。合格者さんは正解してくるレベルなので、落とすと痛い1問です。
問4に関して、ルシャトリエの原理は不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問5に関して、酸化還元反応に関する簡単な部類の計算です。共通テストと同等なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★★(やや簡単)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:完答したい1問
大問3

講師としての解説
「酸化還元」からの出題です。
知識の必要性に関して、普通程度です。半反応式の作り方、酸還元の定石を知っておく必要があります。思考力の必要性に関して、普通程度です。問2の2段階の中和が思考を要します。
問1に関して、思考問題です。平衡という事で、まず増減表を書きましょう。酸の濃度c・電離度αとして、各値は
- HA:c(1-α)
- H+とA-:どちらもcα
- Ka:cα^2/(1-α)
となります。今「α<0.05」なので「1-α≒1」と近似でき「K=cα^2」なので「α=√K/c」より、[H+]=√cK。「C=0.10、[H+]=1.0×10^-3」を代入して、Ka=1.0×10^-5モル/リットルで正解です。
問2に関して、思考問題です。混合後のNaOHの能動をyモル/リットルと置くと「塩酸が放出したH+ = 混合液が受け取ったH+」の式より「1×0.10×15/1000=1×y×20/1000」となり、これを解いて「y=0.075モル/リットル」と判ります。よって、混合液200ml(100ml+100mlなので)に含まれていたOH-のモル数は「0.075× 200/1000=1.5×10^-2モル」となります。よって、元々のHAの濃度をxモル/リットルとして「中和後に残ったOH- = 1×0.20×100/1000 - 1×x×100/1000 =1.5×10^-2」より、これを解いて「x=5.0×10^-2モル/リットル」が正解となります。
問3に関して、知識問題です。過マンガン酸イオンとシュウ酸の酸化還元反応の式を作る問題です。以下の要領で、半反応式を書いて合体させると正解できます。
- MnO4- + 8H+ + 5e → Mn2+ + 4H2O・・・①
- (COOH)2 → 2CO2 + 2H+ + 2e・・・②
- ①×2+②×5より
2MnO4-+6H++5(COOH)2 → 2Mn2+ + 8H2O +10CO2
以上で正解となります。複雑な式ですが、半反応式の前後関係「MnO4- → Mn2+、2COOH → 2CO2」さえ憶えておけば、残りは全て逆算で導き出せます。
問4に関して、思考問題です。問3に続き酸化還元反応なので、半反応式を書いていきます。
- MnO4- + 8H+ + 5e → Mn2+ + 4H2O・・・①
- H2O2 → 2H+ + O2 + 2e・・・②
よって「過マンガン酸カリウムが受け取ったeのモル数 = 過酸化水素が放出したeのモル数」の式より、求める濃度xとして「5×0.050×25/1000 = 2×x×100/1000」これを解いて「x≒3.1×10^-2モル/リットル」が正解となります。
受験生としての解説
問1に関して、実は型が決まったワンパターン問題なのですが、不合格者さんには難しいです。合格者さんは正解してくるので、合否を分ける1問です。
問2に関して、溶液を途中で取り出す「2段階の中和滴定」は定番ではありますが、合格者さんでも少し難しいレベルです。よって、正解できれば他者に差をつける1問です。
問3に関して、シュウ酸の半反応式は不合格者さんには難しいです。合格者さんは正解してくるので、合否を分ける1問です。
問4に関して、共通テストと同等なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:問2以外は正解したい
大問4
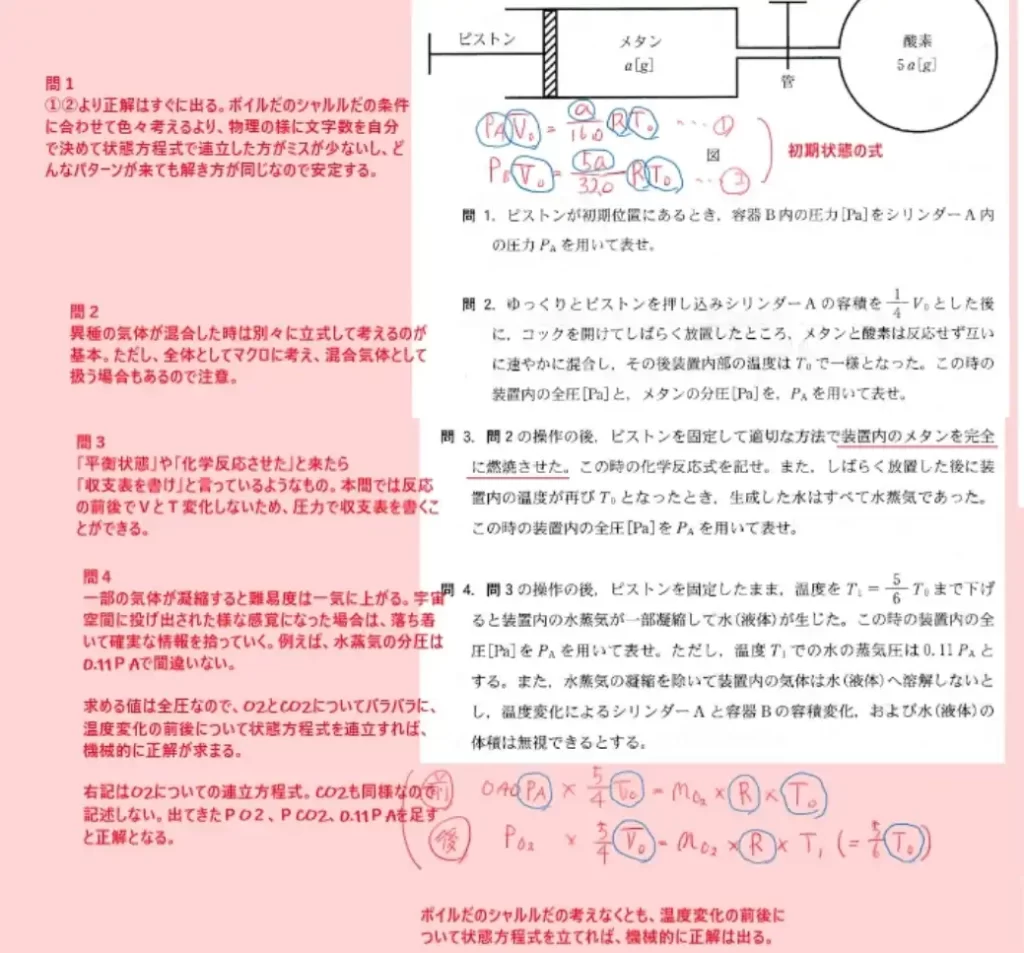
講師としての解説
「全圧・分圧・蒸気圧」からの出題です。
知識の必要性に関して、やや簡単です。ボイルシャルルの法則を使います。思考力の必要性に関して、普通程度です。コックとシリンダーの状態に合わせながら、内部の気体状態を算出していきます。最後は液体の水が発生した際の処理を問われています。
問1に関して、思考問題です。コックが閉じているのでシリンダーAと容器Bは完全に別物です。しかし、問題文に「A・Bは同温・同体積」という内容が書いてあるため、物質量の比がそのまま圧力の比となります。よって、「PB=PA × 5a/32.0 ÷ a/16.0 =2.5PA(Pa)」とPAで表せて正解となります。
問2に関して、思考問題です。気体の状態方程式(PV=nRT)を考えた時
- 気体の物質量nは一定
- 気体定数Rは一定
- 問題文「温度を一定に制御」よりTも一定
よって、状態方程式は「PV=一定」となります。コックを空けた後の体積は5/4V0であり、この時のメタンと酸素の分圧をPメ・P酸と置くと
- Pメ × 5V0/4 =PA × V0
- P酸 × 5V0/4 = 2.5PA × V0
- Pメ=0.80PA、P酸=2.0PA
- よって全圧=Pメ+P酸=2.8PA(Pa)が正解となります
問3に関して、以下の増減表より、反応後の全圧=0.40PA+0.80PA+1.6PA=2.8PA(Pa)が正解となります。
| CH4 + | 2O2 → | CO2 + | 2H2O | |
| 前 | 0.80PA | 2.0PA | 0 | 0 |
| 中 | -0.80PA | -1.6PA | +0.80PA | +1.6PA |
| 後 | 0 | 0.40PA | 0.80PA | 1.6PA |
問4に関して、思考問題です。問題文に「ピストンを固定したまま」と書いてあるので「Vが一定」となり、酸素と二酸化炭素に関しては「P/T=一定」となります。よって
- P酸’/(5T0/6) = 0.40PA/T0
- より、P酸’=0.333PA≒0.33PA(Pa)・・・①
- P二酸化炭素’/(5T0/6) = 0.80PA/T0
- より、P二酸化炭素’=0.666PA≒0.67PA(Pa)・・・②
- 水蒸気の圧力は液体が発生しているので0.11PA・・・③
- 全圧=①+②+③≒1.1PA(Pa)が正解となります
受験生としての解説
問1に関して、「同温・同体積」の条件から「圧力とモル数が比例関係」と見抜いて立式する事は、不合格者さんには少し難しいレベルです。よって、合否を分ける1問より少し簡単な問題です。
問2に関して、今度はボイルの法則ですが、こちらも不合格者さんには少し難しいとはいえ「不合格者さんには正解できない」というレベルでもありません。よって、合否を分ける1問より少し簡単な問題です。
問3に関して、本問は増減表を描いて埋めるだけなので不合格者さんでも正解してくるレベルです。しかし、本問に参加するには問2の正解が必要なので、問2とセットで合否を分ける1問より少し簡単な問題となります。
問4に関して、不合格者さんには厳しいレベルです。合格者さんは正解してくるレベルなので、合否を分ける1問です。
- 知識:★★(やや簡単)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:完答したい1問
大問5

講師としての解説
「構造決定」からの出題です。
知識の必要性に関して、普通程度です。けん化(加水分解でアルコール+カルボン酸)の知識が必要です。思考力の必要性に関して、やや難しいです。与えられた情報と炭素数から矛盾を削除しつつ正解を目指します。
問1に関して、思考問題です。まず、構造決定の定番「元素分析」をおこないます。
- C:29.69 × 12.0/44.0 =8.097(mg)
- H:6.74 × 2.00/18.0 =0.748(mg)
- O:11.25-(8.10+0.75)=2.40(mg)
- C:H:O=8.10/12.0 : 0.75/1.00 : 2.40/16.0 =9:10:2
問題文より「分子式は150」なので、組成式そのままC9H10O2が正解となります。
問2に関して、思考問題です。A・B・Cの分子式が判ったので解析を進めていきます。まずAに関して、「水酸化ナトリウムを加えると加水分解でD・Eが生じた」という内容より、エステル結合のけん化(よってD・Eはアルコールとカルボン酸)とわかります。また「炭酸ガスでDがエーテル層」という内容より、Dはフェノール類とわかりるので、Eがカルボン酸とわかります。
- 「Eは還元性を示さなかった」という内容からE≠ギ酸とわかり
- 「Dは構造異性体を持つ」よりD≠フェノールとわかり
- 分子量より「Dの炭素数+Eの炭素数=9」なので、Dの炭素数が7・Eの炭素数が2
- よってD「クレゾール」で確定、E「酢酸」で確定
となります。続いて化合物Cに関して。
- 化合物Hは「アンモニア性硝酸銀・・・」より、還元性を持つ唯一のカルボン酸「ギ酸」
- 化合物Iは「不斉炭素原子を持つ」より、Iは「ベンジルエタノール」
となり、問2の正解となります。
問3に関して、思考問題です。問2よりDは「クレゾール」と判っています。よって、Dの構造異性体は「オルト・メタ・パラクレゾール、ベンジルアルコール、メチルフェニルエーテル」の5種類が正解です。
問4に関して、思考問題です。飛ばしてきた化合物Bについて考えます。問題文[Bに水酸化ナトリウムで加水分解してF・Gが生じた」という内容より、これはエステルのけん化であり、F・Gはアルコールとカルボン酸と判ります。また問題文「Gはヨウ素と反応させると黄色沈殿」より、Gはヨードホルム反応陽性です。Fの「水に溶けにくい」「Fはナトリウム塩を生じた」という内容よりFが芳香族カルボン酸です。よって、Gはエタノールと判り、逆算でFが安息香酸と導かれます。よってBは「安息香酸エチル」であり、このけん化式が正解です。
問5に関して、思考問題です。問3よりHは「ギ酸」Iは「ベンジルエタノール」と判っています。よって、これらをエステル結合させたものが化合物Cで正解となります。
問6に関して、知識問題です。塩化ベンゼンジアゾニウムと「カップリング反応」するのは、フェノール類なのでD「クレゾール」が正解です。
受験生としての解説
問1に関して、元素分析なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、不合格者さんには難しく、合格者さんは正解してくるレベルです。よって、合否を分ける1問です。
問3に関して、構造異性体を探すだけなので不合格者さんでも正解できますが、本問に参加するためには問2の正解が必要です。よって、問2とセットで合否を分ける1問です。
問4に関して、不合格者さんには厳しいレベルです。合格者さんでも「ナトリウム塩」から「Fの方がカルボン酸」と確定させる部分がやや難しいです。よって、正解できれば他者に差をつける1問となります。
問5に関して、HとIをエステル結合させるだけなので不合格者さんでも正解できますが、本問に参加するには問3の正解が必要です。よって、問3とセットで合否を分ける1問です。
問6に関して、ジアゾカップリングの知識問題なので不合格者さんでも正解できますが、参加するには問3の正解が必要です。よって、問3とセットで合否を分ける1問です。
- 知識:★★★(普通)
- 思考:★★★★(やや難しい)
- 総合:★★★(普通)
- 短評:才能で劣る人の逆転チャンス
大問6

講師としての解説
「高分子」からの出題です。
知識の必要性に関して、普通程度です。高分子全般の基礎知識が必要です。思考力の必要性に関して、やや簡単です。計算問題が主体の大問ですが、問2~問5まで「繰り返し単位」を扱う同種の問題です。
問1に関して、知識問題です。高分子に関する語句問題を2つ答えます。アに関して、テレフタル酸とエチレングリコールの縮合で生じるのは「ポリエチレンテレフタラート」です。イに関して、スチレンとpジビニルベンゼンの共重合体にスルホ基を付けたものは「陽イオン交換」樹脂です。
問2に関して、思考問題です。セルロースの繰り返し単位の式量が「162n」、そこから生じるnモルのグルコースが「180n」です。よって、比の式「セルロース:グルコース=162n:180n=9.9×10^2グラム:xグラフ」を解いて「x=1.1×10^3グラム」が正解です。
問3に関して、思考問題です。問2の解き方をそのまま使えます。比の式「セルロース:トリアセチルセルロース=162n:288n=9.6×10^5グラム:yグラム」を解いて「y≒1.7×10^6グラム」が正解です。
問4に関して、思考問題です。ナイロン66の繰り返し単位内の原子量を合計すると226です。この226がn回繰り返すことで4.8×10^5グラムになっています。そして、繰り返し単位1つの中に2個のアミド結合が含まれています。よって「アミド結合の個数=n回×2=4.8×10^5÷226×2≒4.2×10^3個」が正解です。
問5に関して、思考問題です。問4と同じ仕組みで正解できます。ポリエチレンテレフタラートの繰り返し単位の式量は192です。これを9.4×10^2回繰り返したものが本問の正解なので「192×9.4×10^2≒1.8×10^5」となります。
問6に関して、知識問題です。アミド結合(-NHCO-)を持つのは「絹・羊毛・マルターゼ」です。
受験生としての解説
問1に関して、高分子に関する基本知識なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2・問3に関して、繰り返し単位の計算でもシンプルな部類なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4・問5に関して、問2・問3の流れがあるため、正解への流れを想像しやすくなっています。よって、不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
問6に関して、地味ですが「完全正解」となると難しいです。選択肢は10個ありますが、高分子中の多様な分野から選ばれた10個なので、1つ1つ思い出して検討する必要があります。合格者さんでも完全正解は難しいレベルなので、正解できれば他者に差をつける1問です。
- 知識:★★★(普通)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:問5まで完答したい
九州大学の化学2012年・平成24年度
大問1

講師としての解説
「14族」と「原子の構造」からの出題です。
知識の必要性に関して、やや簡単です。全て基本事項の確認です。思考力の必要性に関して、ほぼ不要です。知識問題の集合体です。
問1に関して、知識問題です。炭素に関する語句問題を5つ答えます。ケイ素・ゲルマニウムなど非金属と金属の中間の性質を示すものを「ア:半導体」といいます。炭素の単体には「イ:ダイヤモンド」「ウ:黒鉛」無定形炭素の3種類の「エ:同素体」があります。二酸化炭素が規則正しく配列してできた結晶を「オ:ドライアイス」といいます。
問2に関して、知識問題です。質量数13の炭素原子に含まれる「陽子は6個、中性子は7個」です。質量数-陽子=中性子です。
問3に関して、知識問題です。例「リチウム:K2L1」という具合に電子数を書きながら原子を表現する方法でケイ素を表します。「ケイ素:K2L8M4」ケイ素は典型元素なので、電子殻の外側から規則正しく電子が入ります。
問4に関して、知識問題です。ダイヤモンドの融点が高い理由を20字で表すと「全ての原子が共有結合している結晶だから」です。
問5に関して、知識問題です。CO・CO2・CH4に関して、各化合物の「炭素の酸化数は、+2・+4・-4」が正解です。
問6に関して、知識問題です。「電子を引き寄せる力」は「電気陰性度」です。
問7に関して、知識問題です。一酸化炭素、二酸化炭素、メタン、メタノールの中で「極性分子」は「COとCH3OH」が正解です。電子配置が空間的に対照的でなく、化合物全体の中で電気バランスに偏りがあるものを選べばよいです。
問8に関して、知識問題です。液体を経由せずに直せず気体になることを「昇華」といいます。具体例としては「ナフタレン」があります。
受験生としての解説
問1~問8に関して、全て1問1答形式で共通テストと大差ないレベルです。よって、不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
- 知識:★★(やや簡単)
- 思考:★(簡単)
- 総合:★(簡単)
- 短評:基本知識の集合体
大問2

講師としての解説
「金属イオン」からの出題です。
知識の必要性に関して、普通程度です。金属イオンに関する、難しくなく幅広い知識を問われています。思考力の必要性に関して、普通程度です。問題の作りが応用的であり、問題集であまり見かけないタイプなので思考力を要します。
問1に関して、知識問題です。金属イオンに関する語句問題を3つ答えます。アンモニア分子の窒素は「ア:非共有電子対」を持っているため、金属イオンと「イ:配位結合」を形成できます。それによって生じたイオンを「ウ:錯イオン」といいます。
問2に関して、知識問題です。アンモニアの電子式を描けば正解です。
問3に関して、知識問題です。銅イオンの入った溶液にアンモニア水を加えると青色沈殿の「エ:Cu(OH)2」が生じます。さらにアンモニア水を投じ過剰になると沈殿は溶け、「オ:[Cu(NH3)4]2+」を生じて深青色の溶液になります。Cu(OH)2を空気中で穏やかに加熱すると黒色の「カ:CuO」を生じます。
問4に関して、思考問題です。銅イオンの98.5%がCu(OH)2からCuOとなり、この質量が0.59グラムだったと書いてあります。今、CuOに含まれるCu原子と元の化合物に含まれるCu原子の比は1:1なので(選択肢の全ての物質で1:1になるから)求める物質の分子量xとして「1.20/x × 98.5% × 79.5(CuO)=0.59」となり、これを解いて「x≒159、硫酸銅(Ⅱ)」が正解となります。
問5に関して、思考問題です。設問文の各条件より以下の事がわかります
- 「無色」よりFe2+(黄色)Fe3+(緑)Cu2+(青)Ni(緑)は入ってない
- 「硫化水素で黒色沈殿」よりSn,Pb,Cu,Hg,Agのどれかが入ってる
- 「希塩酸で沈殿」よりAg,Hg,Pbのどれかが入ってる
- 「希硫酸で沈殿しない」よりBa,Ca,Pbは入ってない
- 「アンモニアを少量で褐色沈殿」はおそらくAg2O
- 「アンモニアで白色沈殿」は候補が多すぎる
- 「過剰アンモニアで褐色沈殿消滅」よりAg2O確定
上記に加え「全て酸化数が異なる」「全て族・周期が異なる」より絞り込んでいくと「A=Ag+、B=Al3+、C=Be2+」が正解となります。
受験生としての解説
問1~問3に関して、基礎知識なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、問題自体は難しくありませんが、問題文の書き方が難しいです。不合格者さんの一定数は問題文でつまづくレベルなので、合否を分ける1問となります。
問5に関して、「Ag+」は不合格者さんでも正解してきます。「Al3+」は合格者さんだけが正解するレベル。「Be2+」は合格者さんでも難しいレベルです。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:問4まで正解したい
大問3

講師としての解説
「電気分解」からの出題です。
知識の必要性に関して、強く必要です。高校の範囲を超えた「低電圧での電気分解」を問われています。思考力の必要性に関して、強く必要です。問2がかなり複雑です。1つ1つの要素は普通程度ですが、組み合わさる事で重厚な応用問題となっています。
問1に関して、思考問題です。両極板がプラチナという事で、各極板の反応は以下の通りです。
- 陽極:2H2O → O2 + 4H+ + 4e
- 陰極:2H+ + 2e → H2
上記より電子が1モル流れると気体が3/4モル生じるため「18.0/96500 × 3/4 ≒1.4×10^-4モル」が正解となります。
問2に関して、思考問題です。まず、回路全体に流れた電子のモル数を求めて起きましょう。「27.02/96500 = 2.8×10^-4モル」です。電極Aは銅が溶出する反応が起きていると考えられますが、電極Bは反応の序盤(溶液内にCu2+が無い時)は「2H+ 2e → H2」の反応が起きており、Aから銅が十分に溶け出した後半では「Cu2+ + 2e → Cu」の反応が起きていると考えられます。B極板において
- Cuの生成に使われた電子=2.54×10^-3/63.5 × 2=0.8×10^-4モル
- H2の生成に使われた電子のモル数=(全部-銅の分=)2.8×10^-4 - 0.8×10^-4 =2.0×10^-4モル
- よってH2の発生量:H2に使われた電子のモル数÷2=1.0×10^-4モル
- 正解の1つ・金属イオン濃度=(2.8×10^-4 - 0.8×10^-4)× 1/2 × 1000/10 =1.0×10^-2モル/リットル
次は硫酸の電離を考えます。
- 電離1段目:H2SO4 → H+ + HSO4-
- 電離2段目:HSO4- → H+ + SO4 2-
問題文より「1段目の電離は完全に行われる」との事なので、ここで生じるH+のモル数は「0.1 × 10/1000 =1.0×10^-3モル」となります。プラチナ板(陰極)で生じたH+を引き算し、水素イオン濃度を計算すると「(1.0×10^-3 - 2.0×10^-4)× 1000/10 =0.08モル/リットル」となります。この時、HSO4-のモル数は1段目の電離で発生したH+のモル数と等しいため[HSO4-]=1.0×10^-3× 1000/10 =0.1モル/リットルとなるので、2段階目の電離に関して増減表を描くと以下の様になります。
| モル/リットル | HSO4- → | H+ + | SO4 2- |
| 前 | 0.1 | 0.08 | 0 |
| 中 | -x | +x | +x |
| 後 | 0.1-x | 0.08+x | x |
よって、平衡定数K=0.01より「K=[H+][SO4 2-]/[HSO4-]=(0.08+x)× x/(0.1-x) =0.01」これを解いて「x=0.01」よって、水素イオン濃度は[H+]=0.08+0.01=9.0×10^-2モル/リットルとなります。これで終了です。
問3に関して、知識問題です。①の極板セットにおいて水素・酸素が発生するためには1.23V以上の起電力が必要となります。よって、0.1Vの電圧を1時間かけ続けても何も起きません。これに対し③の極板セットにおいては、亜鉛板が起電力0.1Vで十分溶け出せるため、亜鉛の溶出反応が起きます。以上が正解です。
受験生としての解説
問1に関して、不合格者さんの中でも一定数が不正解になるレベルです。よって、合否を分ける1問より少し簡単な問題です。
問2に関して、合格者さんでも正解は難しいです。医学科の合否を分けるレベルです。1つ1つの要素は難しくありませんが、複数の小問が1つに集約した複雑な作りは「医学科専用」と考えて良いでしょう。非医歯薬系の受験生さんが本問に取り組む時は「大問1.5個分の試験時間を本問に使う価値があるか?」と考え、見返りが十分な場合のみ取り組んでください。
問3に関して、高校の範囲を超えた出題なので、合格者さんでも正解は難しいです。医学科の合否を分ける問題です。化学が好きな学生さんなら
- かなり溶けやすい亜鉛板は溶けるだろう
- わざわざ問題にするぐらいだから、0.1V程度の低電圧ではプラチナ板の反応は起きないだろう
と、予測することは可能です。しかし「九大合格だけを考えるなら」こういう問題を積極的に回避し、簡単な問題だけで合格点を構築してください。そうすれば、戸畑高校で落ちこぼれて退学になるような学生さんでも九大合格できます。
- 知識:★★★★★(難しい)
- 思考:★★★★★(難しい)
- 総合:★★★★★(難しい)
- 短評:問1だけ正解したい
大問4

講師としての解説
「実在気体」からの出題です。
知識の必要性に関して、ほぼ不要です。概ね思考問題です。思考力の必要性に関して、普通程度です。全体的に数学の様な出題ですが、九大数学ほど難しくありません。
問アに関して、思考問題です。1.00モルの理想気体について状態方程式を立てると、PVi=RTより「Vi=RT/P」が正解です。
問イに関して、思考問題です。上記ViをZの式に代入して「Z=PV/RT」が正解です。
問ウに関して、思考問題です。クリプトンの体積が22.4リットルなので、上式へ代入して「Z=V/Vi=22.4/22.4=1」が正解です。
問エに関して、思考問題です。問ウと同様にプロパンの体積が21.8リットルなので、上式へ代入して「Z=V/Vi=21.8/22.4=9.73×10^-1」が正解です。
問オに関して、思考問題です。問題文で与えられたファンデルワールスの式「V-nb」の部分を見ると、1モルの分子が占める体積は「b=8.45×10^-2リットル」と解ります。よって、これを1分子に換算した「8.45×10^-2/(6.02×10^23)≒1.40×10^-23リットル=1.40×10^-1(nm^3)」が正解です。
受験生としての解説
問ア~エに関して、数学の様な出題であり、九大数学の方が難しいので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問オに関して、ファンデルワールスの式の一部をピックアップして正解を導くことは不合格者さんには難しいです。合格者さんでも一定数が不正解になるレベルなので、正解できれば他者に差をつける1問です
- 知識:★(簡単)
- 思考:★★★(普通)
- 総合:★★(やや簡単)
- 短評:エまで正解したい
大問5

講師としての解説
「構造決定」からの出題です。
知識の必要性に関して、普通程度です。芳香族化合物の典型的な知識で正解できます。思考力の必要性に関して、やや難しいです。「加熱で反応が進んだ」というヒントから無水フタル酸を見抜く部分と、核磁気共鳴分光測定の説明を理解する部分で思考を要します。
問1に関して、思考問題です。問題文でC・H・Oの質量比が与えられているので、これを原子量で割ると組成式が「C8H10O」と解ります。問題文の
- ヒント(1):Aの分子量は354(かつA=B+C+D)
- ヒント(3):化合物Cは化合物Bと同じ分子量
より、B・Cの炭素数が16以上だとAの分子量が354をオーバーするため、Bの分子式は「C8H10O」で確定し、これが正解です。
問2に関して、思考問題です。まずヒント(3)「B・Cはベンゼン環を有する」という内容より、B・Cの側鎖の式が「C8H10O - C6H5(ベンゼン環)=C2H5O」と判ります。続いて
- ヒント(4):B・Cは金属ナトリウムと反応して水素を発生
- ヒント(5):Cのみ塩化鉄(Ⅲ)で呈色
という内容より「Bがアルコール、Cはフェノール類」と解ります。よって、問2の正解となるB・Cの構造異性体は以下の通りです。
- B:ベンゼン環1置換体2種類+2置換体3種類=5種類
- C:ベンゼン環2置換体3種類+3置換体6種類=9種類
問3に関して、思考問題です。ヒント(6)「Eを加熱するとFが得られる」という内容より、Fは無水フタル酸・Eはフタル酸と解ります(ここの反応式を描くと問3の正解です)なぜなら、同ヒント(6)に「Bを酸化するとEが生じる」という内容が書いてあるからです。よって、Bがベンゼン環の2置換体かつ側鎖がオルト位である事も解ります。
問4に関して、思考問題です。
- ヒント(8):ヘキサメチレンジアミンと縮合重合してナイロン66、より化合物Dは「アジピン酸」
- ヒント(9):D(アジピン酸)はGを過マンガン酸カリウムと反応でも得られた
より、Gは「シクロヘキセン」と解ります。シクロヘキセンの二重結合を酸化開裂して横に伸ばすとアジピン酸になります。
問5に関して、思考問題です。ヒント(7)「核磁気共鳴分光測定の結果、化合物Cの水素原子は2種類で存在比1:1」という内容より、Cの構造は「フェノール+パラ位に-CH2CH3」と判ります。よって
- 唯一カルボキシ基を持つ化合物D(アジピン酸)が中央に来る
- 「-OH持ち」の化合物B・CがDの両脇に来る
- そして、B-D-Cの形で脱水縮合したものが化合物Aの構造しきである
と判り正解です。
受験生としての解説
問1に関して、元素分析なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、アルコール・フェノール類を見抜くところまでは不合格者さんでも正解してきます。しかし、構造異性体を全種類挙げる部分で一定数が不正解になるレベルです。合格者さんは正解してくるので、合否を分ける1問です。
問3に関して、「加熱してF」から無水フタル酸と見抜き、逆算してBの構造までたどることは不合格者さんには難しいです。合格者さんは正解してくるので、合否を分ける1問です。
問4に関して、シクロヘキセンを酸化開裂してアジピン酸、という流れは合格者さんでもやや気づきにくいです。よって、正解できれば他者に差をつける1問です。
問5に関して、核磁気共鳴分光測定からCの構造を決める部分は合格者さんでも難しいです。よって、正解できれば他者に差をつける1問です。
- 知識:★★★(普通)
- 思考:★★★★(やや難しい)
- 総合:★★★(普通)
- 短評:完答したい1問
大問6

講師としての解説
「酵素」と「油脂」と「アミノ酸」からの出題です。
知識の必要性に関して、普通程度です。3分野からの出題という事で、各分野の必須事項を問われています。思考力の必要性に関して、やや難しいです。問2・問3はシチュエーションを複雑にする事で応用がなされています。実は「いつも通りの事が問われている」と見抜けるか、日本語力が大切です。
問1に関して、知識問題です。酵素に関する語句問題を5つ答えます。デンプンは唾液と膵液に含まれる「ア:アミラーゼ」を経てマルトースとなり、酵素「イ:マルターゼ」の作用でグルコースへ分解されます。脂質の分解酵素は「ウ:リパーゼ」です。タンパク質の分解酵素は、胃で分泌される「エ:ペプシン」と膵液に含まれる「オ:トリプシン」などがあります。
問2に関して、思考問題です。複雑な問題なので情報を整理しましょう。
- 油脂1個にステアリン酸が2個、パルミチン酸が1個含まれている
- ステアリン酸1個は30.5kJ/molのエネルギーを持つATPを146個持っており、パルミチン酸は130個持っている
- 実際には油脂が1.00グラムある
よって、「油脂1.00グラムの総エネルギー=(1.00/862 × 146 ×2 + 1.00/862 ×130 ×1)×30.5≒14.9kJ」が正解となります。
問3①②に関して、思考問題です。まず溶液のpHが6.0という事で、この位の酸性度ですとアミノ酸の「-COO-」を「-COOH」に戻すことはできません。よって、グルタミン酸の2つのカルボキシ基はいずれも「-COO-」となり、電気的にマイナスの状態となっています。よって、グルタミン酸を含む「トリペプチド(2)が陽極側」へ移動します。同様に、pH6.0ではリシンの2つのアミノ基は「-NH3+」の状態なので電気的にプラスの状態となっています。よって、リシンを含む「トリペプチド(1)が陰極側」へ移動します。
問3③に関して、知識問題です。キサントプロテイン反応はベンゼン環のニトロ化によって起こるため、正解は「トリペプチド(3)、アミノ酸名チロシン」となります。
受験生としての解説
問1に関して、リパーゼ・ペプシン・トリプシンは合格者さんでも一定数が不正解になるレベルです。よって、正解できれば他者に差をつける1問です。
問2に関して、内容は平凡ですが問題文が難しく応用してあるため、不合格者さんには難しいレベルです。合格者さんなら「要するに油脂のけん化と同じ」と見抜けるレベルなので、合否を分ける1問です。
問3①に関して、電気泳動なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3②に関して、リシンの構造式は必須事項ではあるのですが、合格者さんでも描けない人が一定数いるレベルです。構造式を描くだけではありますが、正解できれば他者に差をつける1問です。
問3③に関して、キサントプロテイン反応という名前から「トリペプチド(3)、アミノ酸名チロシン」までは、不合格者さんでも正解してきます。しかし、その構造式を描くとなると、合格者さんでも一定数の不正解が出るレベルです。
普通の事しか問われてない大問ですが、才能に恵まれたトップ高校の学生さんでもなかなか高得点が難しい作りです。勉強が難しいのではなく「勉強する事」が難しい分野なので、才能で劣る学生さんでも勉強のやり方さえ分かれば満点を取れるようになります。
- 知識:★★★(普通)
- 思考:★★★★(やや難しい)
- 総合:★★★(普通)
- 短評:才能で劣る学生さんの逆転チャンス
九州大学の化学2011年・平成23年度
大問1

講師としての解説
「化学結合」からの出題です。
知識の必要性に関して、やや簡単です。周期表・電子配置に関する共通テストレベルの知識が必要です。思考力の必要性に関して、普通程度です。問キ・問クの「モノボラン、ジボラン」という多くの受験生さんにとって初見となる物質を理解する必要があります。
問1に関して、知識問題です。化学結合に関する語句問題を10個答えます。ホウ素は「ア:2」周期の「イ:13」族の元素です。価電子の数は「ウ:3」個で原子価は「エ:3」価となります。原子価とは原子が持っている「オ:不対電子」の数に相当します。アンモニアの窒素原子には1組の「カ:非共有電子対」があり、モノボランのホウ素にはありません。モノボランが2つ結合したジボランは、単結合が全て共有結合と仮定した場合(電子数16個)に比べ、実際の電子は「キ:4」個少ないので電子不足化合物と呼ばれています。2つのホウ素間にある水素との結合は、1つの結合あたり「ク:1」個の電子が共有されています。BH4-の立体構造はアンモニウムイオンと同じ「ケ:正四面体」形です。BH3の中心のホウ素原子は1組の「カ:非共有電子対」を受け入れることができます。BH4-はBH3のホウ素に水素化物イオンと呼ばれる水素の陰イオン1個が「コ:配位」結合した化合物で、BH4-のホウ素にはこれ以上原子が結合する部位が無いため安定しています。
受験生としての解説
問ア~カに関して、共通テストと同等の語句問題なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問キ・問クに関して、多くの受験生さんが初見となるジボンラン(B2H6)を使った応用です。合格者さんでも一定数は問題文を理解できず不正解者が出るレベルなので、正解できれば他者に差をつける1問です。
問ケ・問コに関して、問キ・問クの続き物ですが、本問だけ独立して共通テストレベルの語句問題と思うことができます。よって、合格者さんは正解してきますが、不合格者さんにはやや難しいレベルなので、合否を分ける1問です。
問キ・問クは理解しようと思えば、なかなか厄介です。仮に乗り越えたとしても「語句問題2つ分の得点」にしかならないので、のめり込まないよう注意してください。
- 知識:★★(やや簡単)
- 思考:★★★(普通)
- 総合:★★(やや簡単)
- 短評:問キ・問ク以外は完答したい
大問2
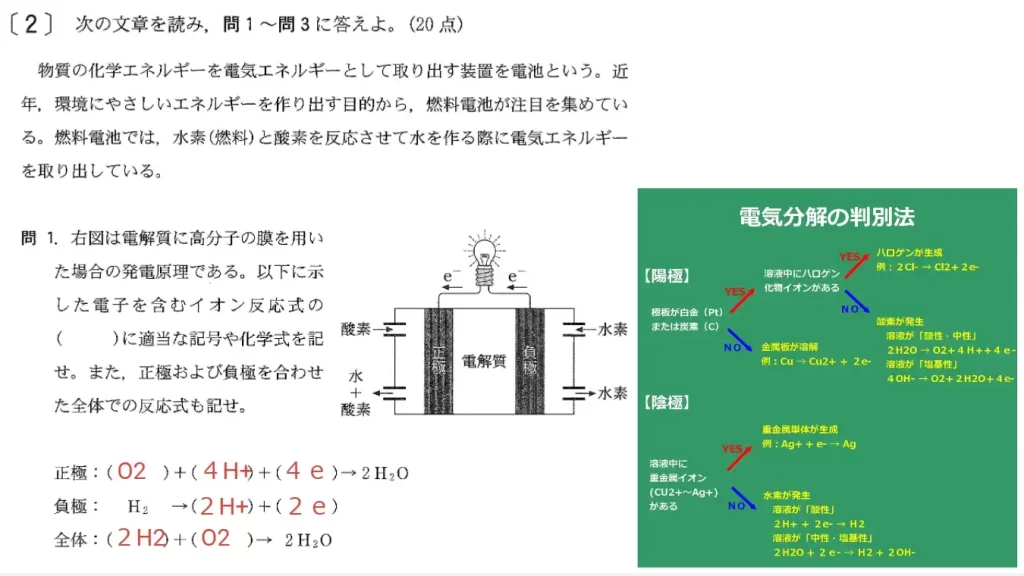
講師としての解説
「電池」からの出題です。
知識の必要性に関して、やや簡単です。燃料電池の基礎知識だけで正解できます。思考力の必要性に関して、普通程度です。問3で多くの受験生さんが初見となる物質を見せられ、化学的思考で正解を導きます。
問1に関して、知識問題です。燃料電池の化学反応式を完成させます。
- 正極:O2 + 4H+ + 4e → 2H2O
- 負極:H2 → 2H+ + 2e
- 全体:2H2 + O2 → 2H2O
となります。
問2に関して、思考問題です。水素2.0gは1モルなので、負極の反応式より電子が2モル流れることが解ります。よってその電気量は「9.65×10^4×2≒1.9×10^5クーロン」が正解です。
問3に関して、思考問題です。「燃料電池の電解質」として適切なものは、水素イオンを提供して反応を円滑にできる物質です。よって、選択肢(c)だけがスルホ基(-SO3H)を持っているため、これが正解となります。
受験生としての解説
問1に関して、燃料電池の反応式を完成させるだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、こちらも共通テストレベルの計算問題なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、不合格者さんには厳しいレベルです。合格者さんなら「スルホ基 → 陽イオン交換樹脂 → H+で反応を円滑化」という発想から(c)を選ぶでしょう。よって、合否を分ける1問です。
- 知識:★★(やや簡単)
- 思考:★★★(普通)
- 総合:★★(やや簡単)
- 短評:完答したい1問
大問3
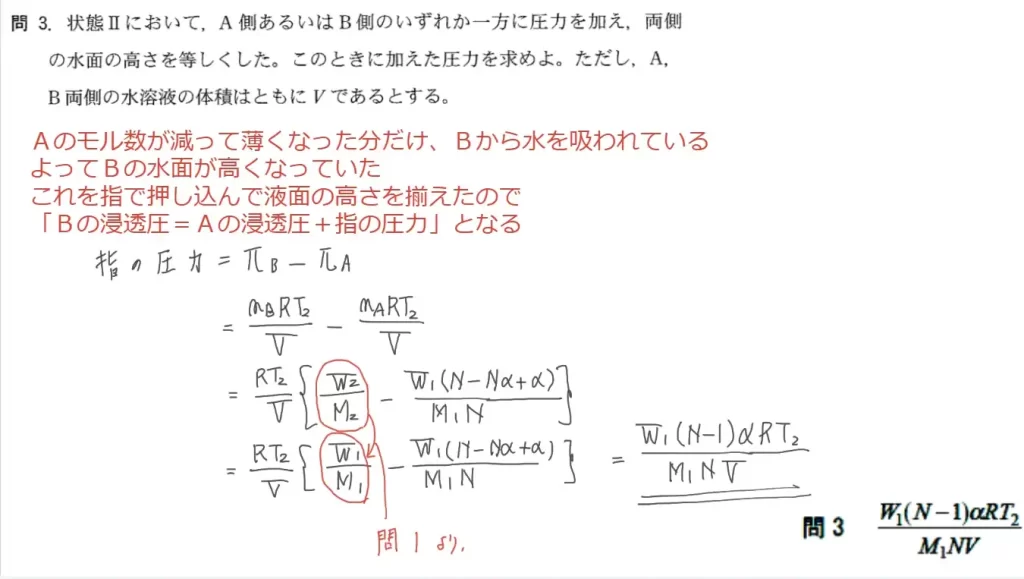
講師としての解説
「浸透圧」からの出題です。
知識の必要性に関して、普通程度です。基本的な知識で正解できます。浸透圧もコロイドも勉強が行き届きにくい分野なので、日頃の計画的な勉強が大切な1問です。思考力の必要性に関して、普通程度です。浸透圧の問題は「液面を圧す」ところまでしか応用しません。問2のコロイドの話から増減表に持ち込む部分で少し思考を要します。
問1に関して、思考問題です。いくつかの過程を経てA側・B側の液面が等しい高さになっていますが、最後の状態だけに着目してください。最終的に液面の高さが等しくなったという事はA側・B側の「モル濃度」が等しく、体積も等しいため「溶けている溶質のモル数が等しい」ことになります。よって「W1/M1 = W2/M2」となります。
問2に関して、思考問題です。問題文に「平衡が成り立った」と書いてあるので増減表を書いてください。閉校後の単量体とN量体の物質量が求まるので(単:(1-α)W1/M1、N量:W1α/M1N)足し合わせると正解です(総:W1(N-Nα+α)/M1N)
問3に関して、思考問題です。問2の「N量体の発生」によって、A側のモル濃度が薄くなりました。よって、A側の浸透圧が下がったためB側の液面が高くなり、これを圧力で押し込んで液面を等しくした状態です。「B側の浸透圧=A側の浸透圧+液面への圧力」という関係が成り立つため、求める圧力に関して「液面への圧力=B側の浸透圧-A側の浸透圧=nB・RT2/V – nA・RT2/V=RT2/V{W1/M1 – W1(N-Nα+α)/M1N}=W1(N-1)αRT2/M1NV」が正解となります。問1の正解「W2/M2 = W1/M1」を使って式変形することがポイントです。
問4に関して、知識問題です。少量の電解質を加えても沈殿しなかったが、多量の電解質で沈殿を生じたという事で、この現象は「塩析」が正解です。多量の電解質を投入することで親水コロイドから水和水を引き剥がし、その上で凝析・沈殿しています。
受験生としての解説
問1に関して、「浸透圧」という分野は九大受験生でも苦手とする人が多く、「関係式を示せ」という出題形式も簡単ではないため、問1とはいえ不合格者さんにはやや難しいです。合格者さんは正解してくるレベルなので、合否を分ける1問です。
問2に関して、N量体のコロイドへ話題が移った所から「増減表を書く」と発想する事は、不合格者さんにはやや難しいです。合格者さんは「平衡」という文字から増減表に移れるレベルなので、合否を分ける1問です。
問3に関して、よくある難関大レベルの浸透圧問題ではありますが、合格者さんでも少し難しいレベルです。よって、正解できれば他者に差をつける1問です。
問4に関して、コロイドの基礎知識ですが、勉強が行き届きにくい部分なので急に「塩析」と思い出すことは不合格者さんには厳しいです。合格者さんなら正解してくるレベルなので、合否を分ける1問です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:問2が合否の分かれ目
大問4

講師としての解説
「反応速度」からの出題です。
知識の必要性に関して、やや簡単です。反応速度に関する基礎知識があれば正解できます。必要な式は問題文で与えられているため、自分で立式する必要はありません。思考力の必要性に関して、普通程度です。問題文の言う通りに素直に式変形していけば完答できます。テクニカルな式変形はありません。
問ア~ウに関して、知識問題です。分子間で起こる化学反応は主に分子の衝突によって起こるため、単位時間あたりの衝突「ア:回数」が多いほど反応速度は上がります。今、Aの濃度を2倍すると反応速度が4倍となり、Bの濃度を2倍にすると反応速度が2倍になるような反応の速度式は「v=k[A]^2[B](←イ・ウの正解)」となります。
問エ~問カに関して、思考問題です。左辺の形(Δ[Z*]/Δt)に惑わされず、問題文の「Z*の生成する反応速度(を示すと)」に注目してください。正解が「v1-v2-v3」とすぐに解ります。各vを反応速度の式で置き換えたものが問オの正解で、「Δ[Z*]/Δt=k2[X][Y]-k2[Z*]-k3[Z*](←オの正解)」となります。問カは「上式=0」から変形するだけなので「カ:k1[X][Y]/(k2+k3)」です。
問キに関して、思考問題です。最後に問カで求めた[Z*]の式をv3の式に代入すれば「v3=k3[Z*]=k3(問カ)=k1k3[X][Y]/(k2+k3)(←キの正解)」となって終了です。
受験生としての解説
問ア~ウに関して、共通テストと同等のレベルなので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問エ~問カに関して、不合格者さんは左辺の「Δ[Z*]/Δt」に惑わされてやや難しいレベルです。合格者さんは正解してきます。よって、合否を分ける1問です。
問キに関して、問カの正解が必要なので、問カとセットで合否をわける1問です。問カまで正解できた受験生さんなら流れで正解できるでしょう
- 知識:★★(やや簡単)
- 思考:★★★(普通)
- 総合:★★(やや簡単)
- 短評:数学的な出題、九大数学より簡単
大問5
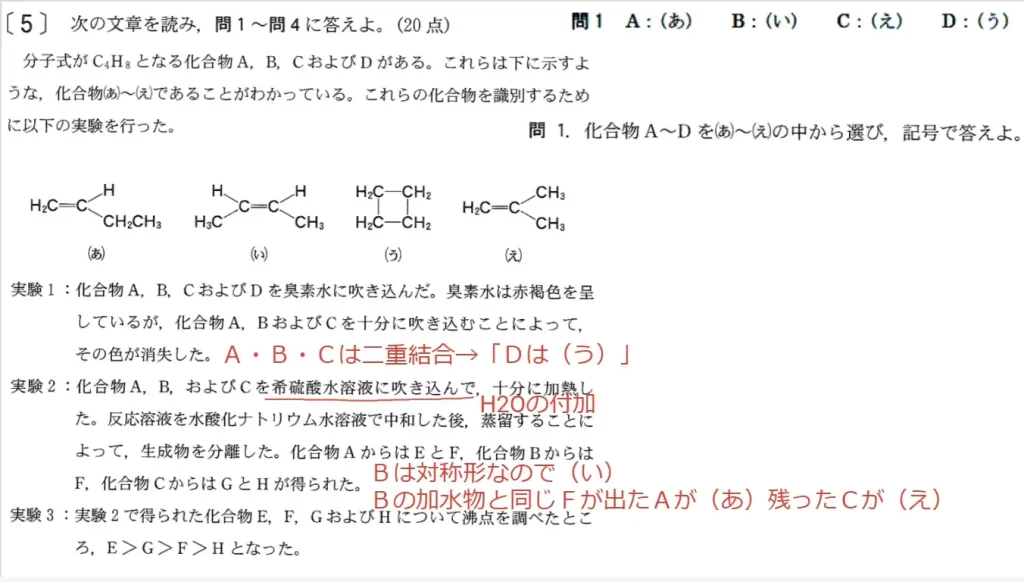
講師としての解説
「脂肪族」と「構造決定」からの出題です。
知識の必要性に関して、やや簡単です。脂肪族の基本知識だけで正解できます。思考力の必要性に関して、やや簡単です。実験2で「H2Oが付加」された事に気付ければ、構造の推定は簡単です。
問1に関して、思考問題です。
- 実験1:化合物A~Dを臭素水に吹き込んだ結果より「A~Cは二重結合を持ち、Dは持たない」ことが解ります。よって、Dは(う)で確定です。
- 実験2:問題文の「希硫酸水溶液に吹き込んで」は「H2Oの付加」を意味しています。よって、水の付加によって化合物F1種類しか生じなかった化合物Bは「対称形」と解るため、Bは(い)で確定です。Bの加水物Fと同じものを生じたAは(あ)、残ったCが(え)で確定となります。
問2に関して、知識問題です。H2Oを付加して化合物E・Fを生じるのは化合物Aです。よって、Aの二重結合を切り、HとOHを左右に付加した2パターンがE・Fとなります。Fは化合物BにH2Oを付加したパターンです。
問3に関して、知識問題です。化合物Bはシス型なので、トランス型を描けば正解となります。
問4に関して、知識問題です。不斉炭素原子と書いてあるので正解は「光学」異性体です。
受験生としての解説
問1に関して、「臭素水の脱色 → 二重結合の有無」は不合格者さんでも正解してきます。しかし「希硫酸水溶液に吹き込んで → H2Oの付加」と気づくことは合格者さんでも難しいです(合格者さんなら問題文の雰囲気から「H2Oの付加」を見抜いてきます)よって、(あ)は全ての受験生さんが正解したい問題です。(い)~(え)は合否を分けるレベルです。
問2・問3に関して、不合格者さんでも正解してくるレベルですが、本問に参加するには問1の正解が必要です。よって、問1とセットで合否を分ける1問です。
問4に関して、不斉炭素というキーワードから光学異性体を導くだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★★(やや簡単)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:完答したい1問
大問6

講師としての解説
「5大栄養素」からの出題です。
知識の必要性に関して、やや難しいです。ビタミンCの還元生・メチレンブルーによる還元性の確認など、普通の勉強では学びにくい知識が使われています。思考力の必要性に関して、普通程度です。セルロースのアセチル化に関する割合計算があります。
問1に関して、知識問題です。ニンヒドリン溶液(アミノ酸・タンパク質の検出)で呈色するものなので、以下が正解となります。
- B(卵白)
- F(アミラーゼ)
- G(プロテアーゼ)
- H(リパーゼ)
語尾に「-ase、アーゼ」が付いたら酵素です。酵素は主にタンパク質で構成されています。
問2に関して、知識問題です。問題文の「フェーリング液で赤色に変化」という内容より、還元性を持つ物質を選べば正解です。A(デンプン)はアミラーゼで分解されているため、炭素1位のアルデヒド基により還元性を有します。D(ビタミンC)は化学では「アスコルビン酸」という名前でエンジオール基がHを放出しやすいため還元性を示します。
問3に関して、思考問題です。問題文が難しく書いてあるので、解読していきましょう。
- 「セルロース1.62gに希硫酸を加えて長時間加熱すると、1.80gの生成物Iが得られた」とは、セルロースがグルコースに分解されたという事です
- 「1mol/Lの水酸化ナトリウム水溶液を加えたメチレンブルー溶液を青色から無色に変化させた」とは、グルコーコースがメチレンブルーを還元して、アルデヒド基がカルボキシ基に変わり、その後、NaOHと中和反応をしたという事です
よって正解は、鎖状グルコースの1位炭素(アルデヒド基)をカルボキシ基に変え、さらに-OHを-ONaに書き換えたものとなります。
問4に関して、思考問題です。セルロースに無水酢酸とりゅう酸触媒を加えているので、セルロースのヒドロキシ基のアセチル化と解ります。その比率に関して
- 1.62gのセルロースにおける100%がアセチル化されれば「+1.26g」
- 実際にはx%がアセチル化されて「+1.05g」
よって「1.62:1.05=100%:x%」という比の式が立ち、これを解いて「x=500/6 %」という値が出てきます。求める正解は「水酸基が何%残っているか=アセチル化されてないのは何%か」なので「100% - 500/6%≒17%」が正解となります。
受験生としての解説
問1に関して、アミノ酸・タンパク質の検出なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、正解の1つA(デンプン)は不合格者さんでも正解してきます。もう1つの正解D(ビタミンC)は合格者さんでも難しいです。
問3に関して、合格者さんでも難しいです。よって正解できれば他者に差をつける1問です。
問4に関して、難関大の定番「セルロースのアセチル化割合問題」なので、合否を分ける1問です。
- 知識:★★★★(やや難しい)
- 思考:★★★(普通)
- 総合:★★★★(やや難しい)
- 短評:問3②のアセチル化問題を落としてはいけない
九州大学の化学2010年・平成22年度
大問1

講師としての解説
「気体」からの出題です。
知識の必要性に関して、普通程度です。やや簡単な知識の集合体ですが、量は多いです。思考力の必要性に関して、普通程度です。やや簡単な問題の連続ですが、問題文の文字数が多いので素早く処理しましょう。
問1に関して、知識問題です。まず実験1~9で発生する気体を確認しましょう。
- 酸化マンガン+過酸化水素=O2の発生
- 亜鉛+希硫酸=H2の発生
- H2+O2=H2Oの発生
- カーバイド+水=CH≡CHの発生
- 硝酸銀+アンモニア=Ag2Oの発生
- ベンゼンを加熱石英管へ投入=C6H6の発生
- 石灰石+希塩酸=CO2の発生
- 水酸化カルシウム+二酸化炭素=CaCO3の発生
さらに二酸化炭素を追加=Ca(HCO3)2の発生 - 銅+濃硫酸=SO2の発生
よって、三重結合を含む化合物は「(d)C2H2」が正解です。
問2に関して、知識問題です。直線分子でないものは以下の5つです。
- 空間的な電子の配置により直線ではないもの:H2O、C6H6、SO2
- イオン結合なのでそもそも分子ではないもの:Ag2O、CaCO3
問3に関して、知識問題です。まず下線部①の式ですが「水酸化カルシウムに二酸化炭素を吹き込むと炭酸カルシウムが沈殿した」という文章を、そのまま式にするだけで正解です。
- Ca(OH)2+CO2 → CaCO3 + H2O
式②に関して、これは「過剰に二酸化炭素を吹き込むとCa(HCO3)2が出る」ことを知っておけば、式を逆算で導けます。
- CaCO3+CO2 → Ca(HCO3)2
- 左辺に足りないものは「H2個、O1個」より
- CaCO3+CO2+H2O → Ca(HCO3)2
式③に関して、ポイントは「熱濃硫酸の半反応式の、変化の前後物質」さえ憶えておけば、正解を導き出せます。
- 熱濃硫酸の半反応式の前後「H2SO4 → SO2」←これだけ憶えてください
- H2SO4 + 2H+ +2e → SO2 +2H2O(Oの数をH2Oで修正、Hの数をH+で修正、電気バランスをeで修正、導けます)
- Cu → Cu2+ + 2e(←これは憶えなくても、よく見かけるほぼワンパターンです)
- 上2式を合体「Cu+2H2SO4 → CuSO4+2H2O+SO2」が正解です
問4に関して、知識問題です。気体に関する◯✕問題を6つ答えます。
- 問1:Ag2O沈殿は褐色なので、正解は◯です
- 問2:H2は水上置換法(水に溶けにくい)SO2(水に溶けやすく空気より重い)は下方置換法で集めるため、正解は✕です
- 問3:青色の正体はCu2+なので、正解は◯です
- 問4:実験8の反応式が左右両方向に起こるため、天井が溶けて床で固まり鍾乳洞となります。正解は◯です
- 問5:ベンゼンにH2を付加してシクロヘキサンを作ろうと思ったら、Pt触媒でH原子を一気に圧着する必要があり大変です(1個1個Hを付けようとするとベンゼン環は復元してしまう)よって、正解は✕です
- 問6:赤褐色で酸性雨を引き起こす気体はNO2であり、SO2は無色です。よって、正解は✕です
問5に関して、思考問題です。まず、求める熱化学方程式を確認すると「H2(気) + 1/2O2(気) = H2O(液) + QkJ」となります。今、問題文で与えられた4つの熱量を式にすると
- 2O=O2(気)+496kJ
- 2H=H2(気)+436kJ
- 2H+O=H2O(気)+926kJ
- H2O(気)=H2O(液)+44kJ
上記より「3式-(2式+1式×1/2)+4式」で求める式と同じ式となるため、「Q=926-(436+496×1/2)+44=286kJ」が正解となります。
問6(ア)に関して、思考問題です。「密度=質量÷体積」より、「体積=質量/密度=M/ρ」となります。これは1モルの話なので、アボガドロ定数で割ってあげれば問題分の「1分子あたり」となります。よって、(ア)の正解は「M/ρNA」です。(イ)に関して、水の沸点が酸素・水素より高い理由は、分子間に「イ:水素結合」があるからです。
受験生としての解説
問1に関して、実験1~9まで全て基本知識ですが「完璧に」となると不合格者さんには厳しいです。合格者さんには難しくないため、合否を分ける1問です。
問2に関して、不合格者さんでも正解してくるレベルです。よって、全ての受験生さんが正解したい問題です。
問3に関して、式1・3は不合格者さんでも正解してきます。式2は、合格者さんだけが正解してくるレベルです。
問4に関して、6問オール正解となると合格者さんでもやや難しいレベルです。よって、正解できれば他者に差をつける1問です。
問5に関して、不合格者さんは「熱化学方程式」を苦手とする人が多いです。これを克服した人が合格者さんなので、合否を分ける1問です。
問6に関して、不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:試験時間に注意、完答したい1問
大問2
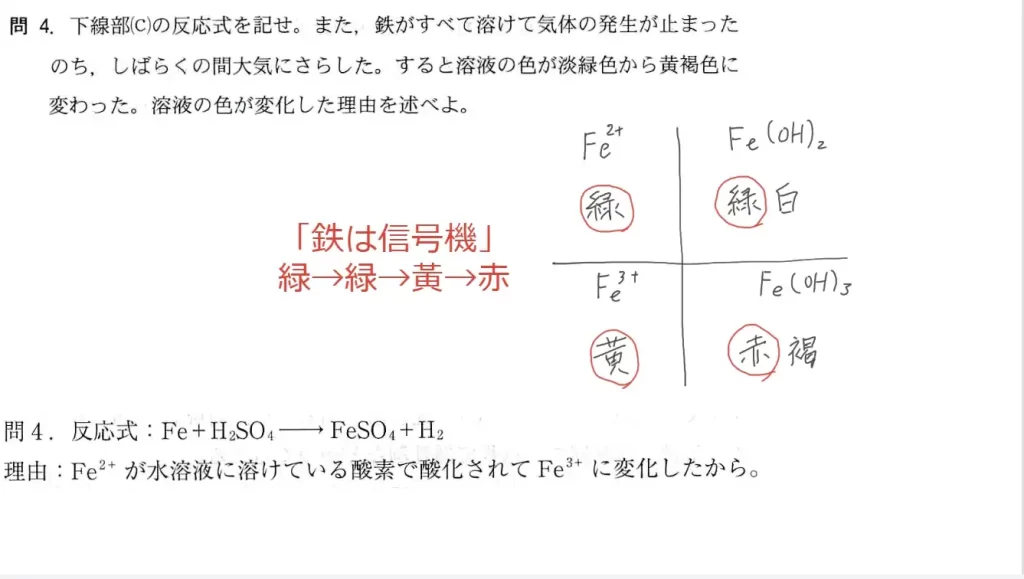
講師としての解説
「鉄」からの出題です。
知識の必要性に関して、普通程度です。鉄に関して幅広い知識を問われています。しかし、ヘキサシアノ鉄Ⅲイオンやチオシアンイオンの様な難しい方向へは向かわず、基礎の範囲内に収まっています。思考力の必要性に関して、普通程度です。鉄の含有量に関する計算や、酸化還元の式を自分で気づいて立式するなど、普通程度に思考を問われています。
問1に関して、知識問題です。鉄には54Fe、56Fe、57Fe、58Feという四種類の安定な「ア:同位体」が存在します。天然の鉄鉱石を溶鉱炉で一酸化炭素を通じて還元した物を「イ:銑鉄」といい、不純物・炭素含有量を除いたものを「ウ:鋼」といいます。鉄に濃硝酸を作用させると「エ:不動態」を形成し、ほとんど反応しません。空気中の水分で参加したFe2O3・nH2Oは粒子サイズは非常に小さいですが、単位質量あたりの「オ:表面積」が非常に大きいです。
問2に関して、思考問題です。56Feの割合をx%と置くと、「M=54×a/100 + 56×x/100 + 57× {100-(a+b+x)}/100 + 58× b/100」となり、これを解いて「x=5700-100M-3a+b」が正解となります。
問3に関して、知識問題です。問題文で赤鉄鉱・磁鉄鉱が酸化鉄(Ⅲ)・四酸化三鉄と与えられているので、そのまま立式すれば正解できます。
- 赤鉄鉱:Fe2O3 +3CO → 2Fe +3CO2
- 磁鉄鉱:Fe3O4 +4CO → 3Fe + 4CO2
問4に関して、知識問題です。鉄に希硫酸を作用させると水素が発生する反応です。よって「Fe + H2SO4 → FeSO4 + H2」と素直に立式すれば正解です。
問5に関して、思考問題です。塩化鉄に塩素を作用させるというあまり見かけない式ですが、だからこそ酸化還元反応だと解ります。各々の半反応式は以下のとおりです。
- Cl2 + 2e → 2Cl-・・・①
- Fe2+ → Fe3+ + e・・・②
- ①+②×2の後2Cl-を両辺に補って
- 2FeCl2 + Cl2 → 2FeCl3
となり正解です。右辺に「FeCl3」が出ていますが、「Cl-」で沈殿するのは「Ag,Hg,Pb」なので固体が水中に沈んでいるわけではありません。水溶液中では「Fe3+」の状態で存在しているため、アンモニア水を加えると「OH-」によって「Fe3+ + 3NH3 + 3H2O → Fe(OH)3 + 3NH4+」という反応が起きます。この時、金属の水酸化物として沈殿した「Fe(OH)3」が正解です。
受験生としての解説
問1に関して、ア~エは不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。オはやや難しいですが、合格者さんなら正解してくるレベルです。
問2に関して、やや複雑ですが、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、赤鉄鉱・磁鉄鉱の化学式につながる名前が与えられているので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、鉄に希硫酸で水素が発生することは中学で習い、高校で再確認します。よって、不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
問5に関して、酸化還元反応と気づく事は不合格者さんには難しいです。合格者さんにとってもやや難しいレベルなので、正解できれば他者に差をつける1問です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:小問5つから1問ミスにしたい
大問3

講師としての解説
「電気分解」と「溶解度積」からの出題です。
知識の必要性に関して、普通程度です。イオン化傾向・電気分解の判別法の知識が必要です。思考力の必要性に関して、やや難しいです。1つ1つの計算は普通程度ですが、積み重なって複雑になっていきます。
問1に関して、知識問題です。ZnOは塩基性酸化物なので、酸である水溶液Aと中和反応します。よって(ア)の正解は「ZnO + 2H+ → Zn + H2O」となります。(ウ)に関して、亜鉛の方が銅よりイオン化傾向が高いため、亜鉛と銅の間で電子の授受が発生します。よって「Zn + Cu2+ → Zn2+ + Cu」が(ウ)の正解です。溶液中の銅が減ってくると今度は水素イオンが電子を受け取るようになり、(エ)の正解は「Zn + 2H+ → Zn2+ + H2」となります。そして、H+が消費されることによってpHが大きくなり、OH-が優勢になってくると[Al3+][OH-]^3がAl(OH)3の溶解度積を超えたところで「Al3+ + 3OH- → Al(OH)3」の反応が起きます。これが(カ)の正解です。
問2に関して、知識問題です。電気分解において、陰極で電子を受け取るCu2+が「完全に消費された」と書いてあるので、次に電子を受け取るのは水素イオンです。よって「水素」が正解となります。
問3に関して、思考問題です。(イ)に関して、反応式は「ZnO+H2SO4 → ZnSO4+H2O」なので、計算式の内容は「(元々あったH2SO4のモル数-反応で消費されたH2SO4)×1000ml/500ml」となります。これを計算すると「5.0×10^-2 × 500/1000 - 5.0×10^-3)×1000/500=4.0×10^-2モル/リットル」が正解です。
続いて問3(オ)ですが、Al(OH)3の沈殿が始まる時の「OH-の濃度」をxモル/リットルと置くと、問題文より水酸化アルミニウムの溶解度積は1.0×10^-32なので
- [Al3+][OH-]^3=1.0×10^-1 × x^3 = 1.0×10^-32
- よって、x=(100)^-1/3×10^-11
- [H+]=1.0×10^-14/[OH-]=1.0×10^-14/x
- よって、pH=-log[H+]=3+1/3・log100≒3.7
よって、「pHは3.7」が正解となります。
問3(キ)ですが、「流れた総電子数-Cuの析出に使われた電子数=H2の生成に使われた電子数」という計算式でH2のモル数を求め、22.4リットル/モルをかければ正解できます。その計算式は「1.00-1.0×10^-1 × 500/1000 × 2)× 1/2 ×22.4≒1.0×10リットル」となり、「1.0×10」が正解です。
問3(ケ)に関して、水溶液AにH+を供給できるのはH2SO4だけであり、硫酸1モルにつき2モルのH+が生じます。逆に言うと、諸々の反応が終了した後「残ったH+の濃度の半分」が「硫酸の濃度」と言えます。諸所の反応において、陰極で銅が析出し、陽極では水が電子を放出して酸素が発生(2H2O → O2 + 4H+ +4e)する際にH+が生じます。そのモル数は析出した銅のモル数の2倍なので、「(H2SO4の濃度×2+銅の析出量×2)× 1000/500 × 1/2」と立式すれば硫酸の濃度が求まります。よって「(5.0×10^-2 × 500/1000 ×2 + 1.0×10^-1 × 500/1000 ×2)× 1000/500 × 1/2 =1.5×10^-1モル/リットル」が正解となります。
問3(コ)ですが、問題文の「電解終了後、さらに1.0×10^-2モルのZn粉末と1.0×10^-2モルのCu粉末を添加」と書いてありますが、H+とのイオン化傾向より、Cu粉末は本問に無関係となります。よって、加えたZnの分だけ「Zn + H2SO4 → ZnSO4 + H2」の反応が起きて水素が発生します。溶液における
- H2SO4のモル数:1.5×10^-1 × 500/1000 = 7.5×10^-2(モル)
- Znのモル数:1.0×10^-2(モル)
なので完全に消費されるのはZnです。そして、Znと同じモル数だけH2が発生します。よって、発生するH2の体積は「1.0×10^-2 × 22.4 ≒ 2.2×10^-1(リットル)」が正解となります。
受験生としての解説
問1に関して、4本の式を立てる問題ですが、その内容・仕組みは4本とも(3本とも)異なっており、簡単ではありません。不合格者さんにはやや厳しく、合格者さんなら正解してくるレベルなので、合否を分ける1問です。
問2に関して、陰極で電子を受け取る順番は「イオン化傾向」で明らかなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、(イ)は不合格者さんでも正解してきます。しかし、(オ)からは不合格者さんには厳しく、合格者さんでも一定数が不正解になるレベルです。よって、正解できれば他者に差をつける1問です。
- 知識:★★★(普通)
- 思考:★★★★(やや難しい)
- 総合:★★★★(やや難しい)
- 短評:アイウエカは正解したい
大問4

講師としての解説
「反応速度」からの出題です。
知識の必要性に関して、普通程度です。触媒と反応速度の知識を問われています。思考力の必要性に関して、やや難しいです。反応速度に関する式変形がやや難しいです。
問1に関して、知識問題です。触媒に関する語句問題を5つ答えます。触媒を加えると化学反応が速くなる理由は「ア:活性化エネルギー」が小さくて済むからです。よって、反応熱そのものは「イ:変わらない」です。触媒は作用の仕方で「ウ:均一触媒」と「エ:不均一触媒」に分かれます。酵素は細胞内の化学反応で触媒としてはたらきますが、酵素が触媒として作用する物質を「オ:基質」といいます。
問2に関して、思考問題です。式①の平衡時の濃度関係は以下のとおりです。
| E | +S | ↔E・S |
| c-[E・S] | [S] | [E・S] |
よって「K=[E・S]/[E][S]=[E・S]/(c-[E・S])[S](mmol/L)^-1」が正解となります。
問3に関して、思考問題です。問2の正解より
- 「K・(c-[E・S])・[S]=[E・S]
- よって「[E・S]=Kc[S]/(1+K[S])ミリモル/リットル」が正解です
問4に関して、思考問題です。問題文で「vmaxを求めよ」との指示なので、まずはvの式を立てましょう。「v=k[H2O][E・S]=5.0Kc[S]/(1+K[S])=5.0c[S]/([S]+1/K)」となります。この式は[S]=-1/K、v=5.0cを漸近線とする双曲線の第一象限を表しているため「vmax=5.0c=5.0×0.30=1.5(mmol/L・s)」が正解となります。
問5に関して、思考問題です。問4の結果より「vmax=5.0c」と解っているので「v=5.0Kc[S]/(1+K[S]) = Kvmax[S]/(1+K[S])」となります。今、題意の「vmaxの半分となるSの濃度」をx(mmol/L)とおくと「vmax/2=Kvmaxx/(1+Kx)」より「Kx=1」となります。K=0.10なので「x=1.0×10ミリモル/リットル」が正解となります。
受験生としての解説
問1に関して、触媒に関する知識問題なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2・問3に関して、増減表を書いて平衡の式を立て、式を変形していくだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4・問5に関して、立式・式変形が難しくなってきたため、合格者さんでも一定数の不正解者が出ます。よって、正解できれば他者に差をつける1問となります。
- 知識:★★★(普通)
- 思考:★★★★(やや難しい)
- 総合:★★★★(やや難しい)
- 短評:問3まで正解したい
大問5

講師としての解説
「構造決定」からの出題です。
知識の必要性に関して、普通程度です。二重結合、環状構造、酸化、マルコフニコフ則など、構造決定に使う基本知識で正解できます。思考力の必要性に関して、普通程度です。問2でB・Cを決定する際にややクセがありますが、他は簡単です。
問1に関して、思考問題です。まず元素分析で化合物Bの分子式を明らかにしましょう。
- C:26.4 × 12/44 =7.2(mg)
- H:13.5 × 2/18 =1.5(mg)
- O:11.1-(7.2+1.5)=2.4(mg)
- C:H:O=7.2/12:1.5/1:2.4/16=4:10:1
- よって分子式(C4H10O)n
- 上記はn≧2では構造が成立しないためn=1で確定
- よって分子式は「C4H10O」が正解
問2に関して、思考問題です。問題文の
- 化合物Dにヨウ素と水酸化ナトリウム水溶液を加えて温めた結果、黄色沈殿
- 化合物Dにアンモニア性硝酸銀水溶液を加えて温めたが、変化は無かった
より、Dは「エチルメチルケトン」以外に候補が無いため確定します。よって、Bは「2-ブタノール」と確定します。続いて化合物Cを求めます。問題文の
- 化合物Eにヨウ素と水酸化ナトリウム水溶液を加えて温めたが変化は無く
- 化合物Eにアンモニア性硝酸銀水溶液を加えて温めた結果、金属析出
という内容より、Eはアルデヒドと解ります。そして、化合物Aが「Bは2-ブタノール」という情報から「直線形」と決まり、Aを元に生まれたC(そしてE)も直線形と解ります。よって、Eは「ブチルアルデヒド」Cは「1-ブタノール」と確定します。
問3に関して、水を付加してB・Cになるのは「1-ブテン」だけなので、これがAで正解となります。構造異性体については、環状構造が2つ、直線形が1つ、枝分かれ構造が1つ、合計4つを描けば正解です。
問4に関して、思考問題です。まず操作名は「a、ヨードホルム反応」「b、銀鏡反応」です。化合物D・Eの構造については、既に問2で求めています。「D、エチルメチルケトン」「E、ブチルアルデヒド」です。
問5に関して、思考問題です。マルコフニコフ則(水素の数が少ないC原子は新しく水素原子を持ちにくい)より、Aに水を付加した際の「副生成物・C」が生成する量が少ないです。よって、Cが正解です。
問6に関して、思考問題です。問題文「過マンガン酸カリウムで(ア)のみ色の変化」という内容より、(ア)は酸化可能な物質であるためDが候補から消えます。よって、酸化された(ア)はEであり、化合物Fはブタンのカルボン酸「酪酸」となります。
受験生としての解説
問1に関して、「n=1」の根拠がやや見つけにくいですが、元素分析なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、問題文のヒントから「Dはエチルメチルケトン以外は候補がない」という理由で確定させる部分が少し難しいです。合格者さんでも意外に苦労する、見た目より難しいレベルなので、合否を分ける1問です。
問3に関して、不合格者さんでも正解してくるレベルですが、本問に参加するためには問2の正解が必要です。よって、問2とセットで、合否を分ける1問です。
問4に関して、問2で正解を出しているため、問2と同様です。
問5・問6に関して、本問自体は不合格者さんでも正解してきますが、本問に参加するためには問2の正解が必要です。よって、問2とセットで合否を分ける1問です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:完答したい1問
九州大学の化学2009年・平成21年度
大問1

講師としての解説
「元素」からの出題です。
知識の必要性に関して、普通程度です。ケイ素・鉄・カルシウムなど頻出元素の特徴を問われています。思考力の必要性に関して、普通程度です。試験現場で「クラーク数の定義」を理解し、その場で応用する問題です。数学では「医学科の合否を分ける難問」になるタイプですが、本問は普通程度の難しさです。
問1に関して、知識問題です。酸素のクラーク数が大きい理由は、地球を構成する岩石の多くに酸素の化合物が含まれているからです。不正解の選択肢は生物・空気の話ですが、地球を構成する岩石とはスケールが違います。
問2に関して、思考問題です。ポイントは問題文「質量百分率」です。クラーク数は地球に存在する元素の「重さの割合」を示したものなので、原子量が1しかない水素は、かなりたくさんあっても質量百分率が大きくなれません。その事を30字以内で解答にふさわしく書くと「水素は原子量が小さいため原子数が多くても総質量が小さい」(から)となります。
問3に関して、知識問題です。元素に関する間違った記述を2ヶ所修正する問題です。ここでクラーク数の表で隠されている元素(ア)~(エ)が必要になるため、問題文から明らかにしていきます。
- イ:「この化学反応に伴う大きな発熱・・・簡易カイロだね」より、ホッカイロの素材である「鉄」と解ります
- ウ:「ウの酸化物は水分と容易に化学反応するので・・・湿気取りに役立っています」より「カルシウム」と解ります
- ア:「シリカゲルはアの酸化物」より「ケイ素」と解ります
では、問題を解いて行きましょう。
- (1):「酸素のみが周期表の第1周期に属する」が正しくないです。「第1周期 → 第2周期」と修正すれば正解です
- (3):14族元素は「C,Si,Ge,Sn,Pb」より2位のSiが該当するため正しい文章です
- (4):「17族元素の単体は電子を受け取り、他の物質を還元する」が正しくないです。「還元 → 酸化」と修正すれば正解です
これで問3は完答ですが、残りも確認しておきましょう。
- (5):クラーク数の10位以内に18族元素はないため、正しい文章です
- (2):最後までハッキリしなかった(エ)の元素ですが、カリウムです。よって、炎色反応を示すので(リヤカー無きK村)正しい文章です
問4に関して、知識問題です。まず、下線部(c)の化合物とは「酸化マグネシウム」です。これについて間違っている文章、及び修正ポイントは以下の2つです。
- (1):「分子 → イオン結晶」に修正すると正解です。マグネシウムは金属元素、酸素は非金属元素なので、この結合はイオン結合です。よって、分子ではありません
- (3):「二重結合 → イオン結合」に修正すると正解です
問5に関して、知識問題です。正解の反応式は以下のとおりです。
- (d)4Fe + 3O2 → 2Fe2O3
- (e)CaO + H2O → Ca(OH)2
受験生としての解説
問1に関して、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、判定が難しい問題です。合格者さんであれ、不合格者さんであれ、表を見て「気づいた人」が正解できる問題です。
問3に関して、不合格者さんにとってやや厳しいレベルですが、実は正解(間違った2コの文章を修正)するだけなら簡単な作りになっています。よって、不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
問4に関して、「イオン結晶だから」という理由で誤った選択肢を見分ける事は、不合格者さんにはやや難しいレベルです。合格者さんは正解してくるので、合否を分ける1問です。
問5に関して、問題文で言われた通りに化学式を書けば正解が出るタイプなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:問2の不正解は仕方ない(準備不可能)
大問2

講師としての解説
「電気分解」からの出題です。
知識の必要性に関して、普通程度です。電気分解の陽極・陰極で発生する反応を判別します。思考力の必要性に関して、普通程度です。電気分解における変化を正しく導き、それを数式にして計算します。
問1に関して、思考問題です。まず、各極板で起こる反応を確認しておきましょう。
- 陽極:4OH- → O2 + 2H2O + 4e・・・①
- 陰極:2H2O + 2e → H2 + 2OH-・・・②
よって、陰極では流れた電子のモル数の半分のH2が発生するため「1.0×38600/96500 × 1/2 × 22.4×10^3 ≒4.5×10^3(ml)」が(ア)の正解です。同様に(イ)の正解は「1.0×38600/96500 × 1/4 ×22.4×10^3 ≒2.2×10^3(ml)」となります。
問1(ウ)に関して、中和滴定の問題です。溶けている溶質(水酸化ナトリウム)のモル数は40/40=1モルと分かるのですが、電気分解によって「水量」が変化しているため、これを確認し「濃度」を確定させましょう。
- 陽極+陰極=全体の反応式:2H2O → 2H2 + O2
- 電気分解によって消費されたH2O:1.0×38600/96500 × 2/4 × 18 =3.6グラム
- 現在の水量=元々あった水量-電気分解で減った水量=183.6-3.6=180.0グラム
- よって中和の式:1× 20/1000 =xグラム × 1モル/(40+180)
- これを解いて「x=4.4グラム」が正解
問1(エ)(オ)に関して、思考問題です。問題文に標準状態と書いてあるため、A・Bの体積224mlより、A・Bのモル数は0.010モルと解ります。ここで反応に関する増減表を書くと以下の通りです。
| 2H2 | +O2 | → 2H2O | |
| 前 | 0.010モル | 0.010 | 0 |
| 中 | -0.010 | -0.0050 | +0.010 |
| 後 | 0 | 0.0050 | 0.010 |
よって、状態方程式より「P=nRT/V=(0.0050+0.010)×0.082×400/0.448≒1.1(atm)」が(エ)の正解です。また(オ)では-55℃という温度により、水蒸気は全て固体になっているためO2だけを考えればよく「P’=nRT/V=0.0050×0.082×218/0.448≒2.0×10^-1(atm)」が正解です。
問2に関して、知識問題です。Na+よりH+の方がイオン化傾向が低いため、電気分解の陰極では「A:H2」が発生します。陽極はプラチナ板でありハロゲンイオンも無いため、水が電子を受け取って「B:O2」が発生します。実験3においては電極が炭素であり、溶液にハロゲンイオン(Cl-)が存在するため、陽極では「C:Cl2」が発生します。
問3に関して、知識問題です。「2Cl- → Cl2 +2e」を電子式で書けば正解です。
受験生としての解説
問1(ア)(イ)に関して、水が電子を授受する反応式はやや難しいですが、不合格者さんでも正解してくるレベルです。よって、全ての受験生さんが正解したい問題です。
問1(ウ)に関して、電気分解によってH2Oが微妙に失われ、それを踏まえた濃度計算をする事は、合格者さんでも少し難しいです。よって、合否を分ける1問より少し難しい問題です。
問1(エ)(オ)に関して、数値はやや複雑ですが、増減表を書いて状態方程式を計算するだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、電気分解の極板で起こる反応は不合格者さんでも身に着けてくる部分です。よって、全ての受験生さんが正解したい問題です。
問3に関して、電子式は不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:完答したい1問
大問3

講師としての解説
「凝固点降下」と「化学平衡」からの出題です。
知識の必要性に関して、普通程度です。凝固点降下と化学平衡の基本知識で正解できます。思考力の必要性に関して、難しいです。小問1の正解を出すだけで水溶液Ⅰ~Ⅲの全容を計算する必要があります。九大受験生なら「難しい大問でも(1)だけは解かねば」と思うのが普通ですが、(1)から医学科レベルの難問です。
問1に関して、思考問題です。求める値が「Bの物質量」なので、Bに関する凝固点降下の式(凝固点降下度=モル凝固点降下×質量モル濃度)を書き
- 凝固点降下度
- 溶媒Hのモル凝固点降下
- 溶媒Hの質量
を求めれば「Bのモル数」があぶり出しで得られると想像がつきます。問題文より「凝固点降下度は2.0×10^-1」「溶媒Hの質量1.0kg」と書いてあるので、目指すべきは「溶媒Hのモル凝固点降下」となります。そこで利用できそうなのが「溶媒Hに溶質Aを溶かした時の数値」という事で、溶質Aの実験データを分析すると以下の通り。
- 溶媒Hの質量:1.0kg
- 凝固点降下度:2.0×10^-1
- Aのモル数:不明(だがAを溶媒Sに溶かした実験と同じモル数)
- 溶媒Hのモル凝固点降下:不明
という事で「未知数2つ、式1本」なので、またしても正解に届きません。しかし、Aのモル数が「溶媒Sに溶かした実験と同じモル数」と判ったので「溶質Aを溶媒Sに溶かした実験データ」を調べます。今度こそ正解に手が届くはずです。
- 溶媒Sの質量:5.0×10^-1kg
- 溶媒Sのモル凝固点降下:2.5×10^-1
- 溶質Aのモル数:不明
- 凝固点降下度:5.0×10^-1
という事で「5.0×10^-1=2.5×10^-1 × Aのモル数/5.0×10^-1」を解いて、「Aのモル数=0.10モル」と解りました。ここから上記を逆算して、本問の正解「Bのモル数」に届かせます。「Aのモル数」を「溶媒HにAを溶かした凝固点降下の式」に代入すると「2.0×10^-1 = Hのモル凝固点降下 × 0.10モル/1.0」より「Hのモル凝固点降下=2.0」となります。これを1番最初の式「溶媒Hに溶質Bを溶かした時の凝固点降下の式」に代入すると「2.0×10^-1 = 2.0 × Bのモル数/1.0」となり、これを解いて「Bのモル数=1.0×10^-1モル」が正解となります。
問2に関して、思考問題です。問1より、溶媒Hのモル凝固点降下は2.0と解っているので「凝固点降下度=2.0 × 1.0モル/10=2.0×10^-1ケルビン」が正解となります。
問3に関して、思考問題です。AとBの溶液を混合したものが溶液Ⅲ(2リットル中にA・Bが0.10モルずつ溶けている)です。「化学平衡」と書いてあるので増減表を書くと以下の通りです。
| A | +B | ↔C | |
| 前 | 0.050mol/L | 0.050 | 0 |
| 中 | -0.050+xA | -0.050+xA | +0.050-xA |
| 後 | xA | xA | 0.050-xA |
よって、正解の平衡定数KHは「KH=[C]/[A][B]=(0.050-xA)/xA^2=(5.0×10^-2-xA)/xA^2リットル/モル」となります。
問4に関して、思考問題です。A・Bを溶かした溶媒Hを各々1.0kgずつ混ぜたものが溶液Ⅲでした。よって、溶液Ⅲの「質量は2.0kg」であり、問題文に「体積は2.0リットル」と書いてあるので、本問(問4)で問われている「溶液Ⅲ1.0kgあたり」というのは「溶液Ⅲ1.0リットルあたり」と読み取ることができます。よって、上記問3の増減表「平衡後の濃度」をそのまま足し合わせたものがnと解るので「n=xA+xA+0.500-xA=5.0×10^-2+xAモル」が正解となります。
問5に関して、思考問題です。溶液Ⅲに関する凝固点降下の式より「1.5×10^-1 = 2.0 × (0.050+xA)/1.0」を解いて「xA=0.025」と解ります。よって、平衡定数KHの式に代入して「KH=(0.050-xA)/xA^2(これは問3の正解)=(0.050-0.025)/(0.025)^2=4.0×10リットル/モル」が正解となります。
受験生としての解説
問1に関して、いきなり「医学科の合否を分ける問題」と言える難易度です。非医歯薬系の合格者さんでも厳しいレベルです。
問2に関して、問1のデータを使い凝固点降下の式を立てるだけなので、不合格者さんでも正解できるレベルです。しかし、本問に参加するためには問1の正解が必要なので、問1とセットで医学科の合否を分ける難問となります。
問3に関して、増減表を書いて平衡定数を出すだけなので、不合格者さんでも正解できるレベルです。しかし、本問に参加するには問1の正解が必要なので、問1とセットで医学科の合否を分ける難問です。
問4に関して、混合溶液の質量が2.0kgと気付き、その体積が2.0リットルである事から「増減表の濃度結果がそのまま使える」と気づく事は合格者さんでも難しいです。本問は「医学科の合否を分ける難問」ほど難しくありませんが、合否を分ける1問より難しいレベルです。
問5に関して、本問自体は不合格者さんでも正解できますが、参加するためには問1~問4の正解が必要です。よって、セットで医学科の合否を分ける難問となります。
- 知識:★★★(普通)
- 思考:★★★★★(難しい)
- 総合:★★★★★(難しい)
- 短評:医学科の合否を分ける問題
大問4

受験生としての解説
「化学平衡」からの出題です。
知識の必要性に関して、やや簡単です。増減表・状態方程式・ルシャトリエの原理などよく使う知識メインで正解できます。思考力の必要性に関して、普通程度です。分圧の割合を計算、圧平衡定数を計算などがあります。
問1に関して、思考問題です。問題文で生成熱の式が与えられているので書いてみましょう。
- N2(気)+2O2(気)=N2O4(気)-9.2kJ・・・③
- 1/2N2(気) +O2(気)=NO2(気)-33.2kJ・・・④
-③+④×2より「N2O4(気)=2NO2(気)-57.2kJ」となり正解です。
問2に関して、知識問題です。ルシャトリエの原理に従い操作ⅰ~ⅴの平衡の移動を答えます。
- ⅰ:圧力を加えると総分子数が減る方向に動くので、左に移ります
- ⅱ:温度・体積一定なので希ガスを加えても分圧は変化しないため、移動しません
- ⅲ:問1より与式は吸熱反応なので加熱すると、右に移ります
- ⅳ:圧力・温度一定で希ガスを加えると、体積が増えるため気体の分圧が下がります。よって、総分子数を増やす方向、右に移ります
- ⅴ:触媒を加えても反応結果には寄与しないため、移動しません
問3に関して、思考問題です。「平衡状態」と書いてあるので増減表を書きましょう。
| N2O4(気) | ↔2NO2(気) | |
| 前 | 8.0×10^-2 | 0 |
| 中 | -0.080×0.20 | +0.080×0.20×2 |
| 後 | 6.4×10^-2 | 3.2×10^-2 |
温度一定・体積一定より、圧力と濃度は比例関係となる(PV=nRT)ので「NO2の分圧=3.2×10^-2/(6.4×10^-2+3.2×10^-2)≒33%」が正解です。
問4に関して、思考問題です。求める値が圧平衡定数なので、N2O4とNO2について実際の圧力を状態方程式(PV=nRT)を使って求めます。
- P(N2O4)=nRT/V=6.4×10^-2×8.31×10^3×313/1.0・・・⑤
- P(NO2)=nRT/V=3.2×10^-2×8.31×10^3×313/1.0・・・⑥
- 圧平衡定数KP=⑥^2/⑤≒4.2×10^4(Pa)が正解です
受験生としての解説
問1に関して、生成熱の式を立てて引き算するだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、ルシャトリエの原理なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、増減表を書いて「温度・体積一定」から分圧の式に持ち込むだけですが、不合格者さんの一定数が不正解になるレベルです。よって、合否を分ける1問より少し簡単な問題です。
問4に関して、圧平衡定数を出すだけですが、本問に参加するには問3の正解が必要となります。よって、問3とセットで合否を分ける1問より少し簡単な問題となります。
- 知識:★★(やや簡単)
- 思考:★★★(普通)
- 総合:★★(やや簡単)
- 短評:完答したい1問
大問5

講師としての解説
「芳香族」と「糖類」からの出題です。
知識の必要性に関して、やや簡単です。作図の問題、構造決定などありますが、ヒントに使える図が問題文で与えられています。思考力の必要性に関して、やや簡単です。問題数は多いですが、1問あたりは薄味です。
問1に関して、知識問題です。糖類に関する語句問題を3つ答えます。図で示されたサリシンAを加水分解すると、サリチルアルコールBと「ア:グルコース」が生成します。グルコースは水溶液中では「イ:3」種類の異性体(α、鎖状、β)の平衡状態として存在しています。これに還元剤を加えて、グルコースの「ウ:アルデヒド」基を還元したものが、糖アルコールDです。
問2に関して、知識問題です。問題文「サリチルアルコールBの第1級アルコールを酸化するとサリチル酸」より、Bの形状は「サリチル酸の-COOHを-CH2OHに変えたもの」と解ります。また、問題文「グルコースのアルデヒド基が還元されて糖アルコールD」という内容より、Dの形状は「鎖状グルコースの1位の炭素を-CHOから-CH2OHに変えたもの」と解ります。
問3に関して、思考問題です。1モルのサリシン(分子量286)から1モルのサリチル酸(分子量138)が生じるので「1.43/286 × 138 =0.69グラム」が正解です。
問4に関して、知識問題です。問題文で言われた通りに立式するだけで正解できます。
- 「フェノールにナトリウムを作用させて生成したナトリウムフェノキシド」
2C6H5OH(←ベンゼン環で書いてください) + 2Na → 2C6H5ONa + H2 - 「フェノールに水酸化カリウムを作用させて生成したカリウムフェノキシド」
C6H5OH + KOH → C6H5OK + H2O
問5に関して、思考問題です。まず(c)に関して、無水酢酸を加水分解すると酢酸が生じます。問題文で言われた通りに立式すれば「(CH3CO)2O + H2O → 2CH3COOH」で正解です。続いてサリチルアミドHに関して、ポイントは問題文の「分子内にアミド結合を持つ」という記述です。サリチル酸メチルで「アミド結合」できるのは側鎖のC1ヶ所だけなので、この部分でアミド結合を作ったものが正解と解ります。
問6に関して、思考問題です。まず、元素分析からIの分子式を求めましょう。
- C:6.16 × 12.0/44.0 =1.68(g)
- H:1.44 × 2.0/18.0 =0.16
- O:2.16-(1.68+0.16)=0.32
- C:H:O=1.68/12.0:0.16/1.0:0.32/16.0=7:8:1
よって組成式C7H8Oであり「分子量108」という指定より、これがそのまま分子式となります。ベンゼン環を除いた式は「C7H8O-C6H5=CH3O」なので、化合物Iは「Iを含めて」5種類(1置換体2つ、2置換体3つ)の構造異性体が考えられます。これを問題文と照らし合わせていくと
- 「酸化されて安息香酸」→Iはベンジルアルコール
- 「酸化されにくいK」→メチルフェニルエーテル
- 「酸化されてサリチル酸」→Lはオルトクレゾール
- 「酸化されてパラヒドロキシ安息香酸」→Mはパラクレゾール
- 消去法でNがメタクレゾール
となります。
問7に関して、知識問題です。塩化鉄(Ⅲ)で呈色するのは「フェノール類(ベンゼン環に直接OHがついたもの)」なので、これに該当しない「A・D・F・I・J・K」が正解となります。理由は「ベンゼン環に結合するヒドロキシ基を持たないから」で23字(24字以内で解答)となります。
受験生としての解説
問1に関して、糖に関する基本知識なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、言われた通りに作図するだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、モル計算としては簡単な部類なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、問題文に言われた通り立式するだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問5に関して、(c)は不合格者さんでも正解してきます。サリチルアミドHについては、問題文で言われた通りの事をするだけではありますが、サリチル酸メチルからアミド結合でHに持ち込む事は、不合格者さんの一定数が不正解になるレベルです。よって、合否を分ける問題より少し簡単な問題です。
問6に関して、構造決定の中でも簡単な部類なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問7に関して、塩化鉄(Ⅲ)の呈色条件は合格者さんは必ず知っているレベル、不合格者さんの一定数が知らないレベルです。よって、合否を分ける1問より少し簡単な問題となります。
- 知識:★★(やや簡単)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:完答したい1問
大問6A

講師としての解説
「糖類」と「油脂」からの出題です。
知識の必要性に関して、やや簡単です。糖類・油脂の基本知識で解けます、光合成の反応式も基本レベルです。思考力の必要性に関して、やや簡単です。油脂のけん化の応用タイプとしてメチルエステルが使われていますが、けん化と同じ解き方で正解できます。
問1に関して、知識問題です。糖類と油脂に関する語句問題を10個答えます。動物は糖類を分解して得たエネルギーを生命活動に利用しますが、これは糖類の分解を「ア:酵素」を用いて促進する酸化反応です。これに対し光合成は、二酸化炭素の「イ:還元」反応です。デンプンやセルロースを構成するグルコース基本単位にはヒドロキシ基が「ウ:3」個あります。ほとんどの植物に含まれる「エ:スクロース」は還元性を持たない二糖類です。グルコース溶液から作られる異性化糖は、グルコースを「オ:フルクトース」に変異させることで甘みを増しています。生物の遺伝情報を伝達する核酸は、糖と「カ:リン酸」とのエステルです。核酸の塩基は環状構造をとっており、炭素、水素、酸素、「キ:窒素」からなります。DNA分子では、二本の鎖中の塩基の間で「ク:水素」結合により結びついて二重螺旋構造をとっています。油脂は脂肪酸と「ケ:グリセリン」のエステルです。油脂や脂肪酸のメチルエステルを水酸化ナトリウムで加水分解すると「コ:セッケン」ができます。
問2に関して、知識問題です。光合成の化学反応式は「6CO2 + 6H2O → C6H12O6 + 6O2」です。水と二酸化炭素から栄養(グルコース)ができる反応です。
問3に関して、思考問題です。反応の関係せいは「1油脂+3メタノール → 3メチルエステル + 1グリセリン」という事で、メタノールとメチルエステルが1:1の関係になっています。よって、「メタノール:メチルエステル=32:296=xグラム:592グラム」となり、これを解いた「x=64.0グラム」が正解となります。
受験生としての解説
問1に関して、酵素・糖類・油脂の基本問題ですが、10問全て正解となると不合格者さんにはやや厳しいです。合格者さんは正解してくるので、合否を分ける1問です。
問2に関して、光合成の反応式は不合格者さんでも書けます。よって、全ての受験生さんが正解したい問題です。
問3に関して、割合の計算問題ですが簡単な部類なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、
問5に関して、
- 知識:★★(やや簡単)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:完答したい1問
大問6B

講師としての解説
「高分子化合物」と「アミノ酸」からの出題です。
知識の必要性に関して、やや簡単です。全18問の大半が基本レベルです。思考力の必要性に関して、ほぼ不要です。知識問題です。
問1に関して、知識問題です。10個の文章に書かれた間違いを修正していきます。
- 乳酸における鏡像の関係は「光学」異性体です
- ラクトースを酵素で分解すると「グルコース」とガラクトースになります
- オレイン酸の「二重」結合に水素を付加させると飽和脂肪酸になります
- 天然ゴムの主成分は「イソプレン」です
- グルコースの還元性は「アルデヒド」基のはたらきです
- グリシンは炭素原子を「2」個もちます
- フェニルアラニンはカルボキシ基と「アミノ」基を持つ双性イオンです
- アジピン酸はカルボキシル基を「2」個持ちます
- 卵白アルブミンが強酸や加熱により立体構造を変化させることを「変性」といいます
- マルトースはαグルコースが脱水縮合した「二糖類」です
問2に関して、知識問題です。8つの条件に該当する物質を、10個の選択肢から全て選びます。
- 条件ア:ヒドロキシ基とカルボキシ基を1個ずつ持つのは、10個の選択肢では乳酸だけです
- 条件イ:カルボキシル基とアミノ基を1個持つのはアミノ酸(グリシンとフェニルアラニン)です
- 条件ウ:天然高分子化合物は「自然にあるもの」なので天然ゴム・卵白アルブミンです
- 条件エ:「濃硝酸で黄色」はキサントプロテイン反応であり、ベンゼン環のニトロ化によって起こるため、ベンゼン環を持つ物質(フェニルアラニン・卵白アルブミン)です
- 条件オ:ナイロン66の原料はアジピン酸です
- 条件カ:チロシン(アミノ酸)と結合してジペプチドを作るのは、同じくアミノ酸(グリシン・フェニルアラニン)です
- 条件キ:ビウレット反応は「2個以上のペプチド結合」で呈色するので卵白アルブミンのみです
- 条件ク:不斉炭素原子を1つ持つのは乳酸・フェニルアラニンです
受験生としての解説
問1に関して、不合格者さんでも10問完答してくるレベルです。よって、全ての受験生さんが全問正解したい問題です。
問2に関して、不合格者さんでも正解してくるのは「ア・イ・ウ・オ・カ・ク」です。不合格者さんだと一定数の不正解が出るのは「エ・キ」です。よって、概ね全ての受験生さんが正解したい問題です。
- 知識:★★(やや簡単)
- 思考:★(簡単、オール知識問題)
- 総合:★(簡単)
- 短評:完答したい1問
九州大学の化学2008年・平成20年度
大問1

講師としての解説
「水素結合」と「分子の構造」からの出題です。
知識の必要性に関して、やや簡単です。語句問題は共通テストと同等です。思考力の必要性に関して、やや簡単です。水素結合に関する作図があります。
問1に関して、知識問題です。水素結合と原子の構造・極性について語句問題を7つ答えます。水素結合は水素原子よりも「ア:電気陰性度」が大きな原子によって起こされます。H2Oには水素結合があるため、同族のH2S,H2Se,H2Teに比べ沸点が異常に「イ:高い」です。H2O原子では電気陰性度の差によりO原子がわずかに「ウ:負」に帯電、H原子がわずかに「エ:正」に帯電しています。CH4分子において、C-H間には電気陰性度の差による電気的偏りが存在しますが、CH4が「オ:正四面体」形になっているため、分子全体として空間的な電気バランスがとれているため「カ:無極性」分子となっています。タンパク質の複雑な構造の形成に関して「キ:アミド結合」間の水素結合が重要な役割を果たしています。
問2に関して、知識問題です。まず水素化合物の名前に関して、15族が「アンモニア」17族が「フッ化水素」です。その結合の形は記入例に沿い、分子内の「N-HとH-F」は実線で結び、分子外の「N・・・HとH・・・F」は点線で結んでください。
問3に関して、知識問題です。タンパク質におけるアミド結合間の水素結合を図示します。
- 手順1:アミノ酸(H2NCH(R)COOH)を横向きに並べ「-NH2 HOOC-」で脱水してつなげてください
- 手順2:手順1で作ったアミノ酸の横並びをもう1つ下の段に書き、C=OとN-Hが互い違いになるように並べてください
- 手順3:C=OのOと、N-HのHを点線(水素結合)でつなげば完成です
受験生としての解説
問1に関して、電気陰性度・分子の形状による電気的バランスは理解しやすい部分なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、分子の名前を答えて水素結合を点線で結ぶだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、タンパク質の作図、それに伴う水素結合の作図という事で、不合格者さんの中に不正解者が一定数出るレベルです。よって、合否を分ける1問より少し簡単な問題です。
- 知識:★★(やや簡単)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:完答したい1問
大問2
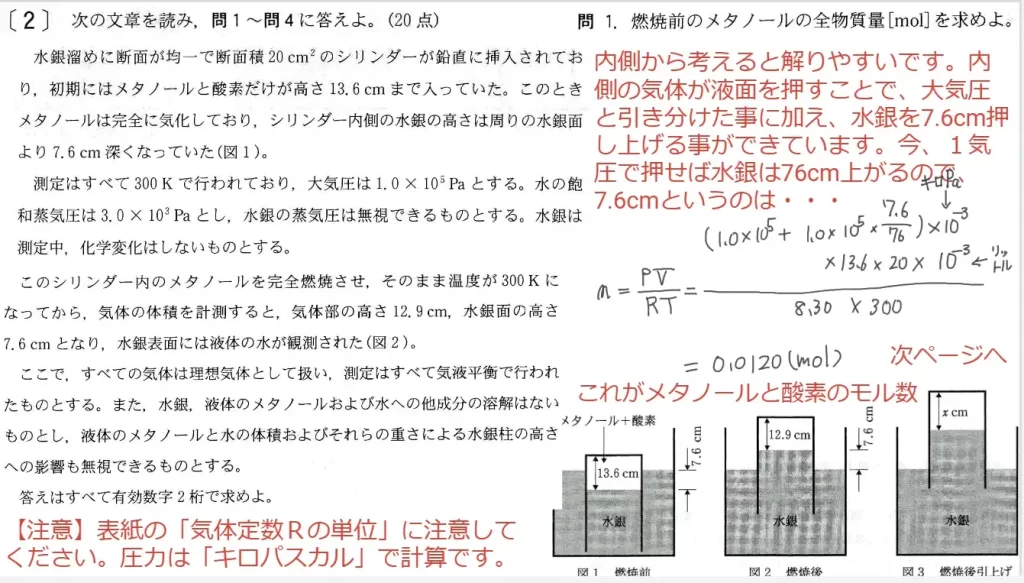
講師としての解説
「気体の計算」からの出題です。
知識の必要性に関して、普通程度です。水銀柱、飽和蒸気圧、増減表、状態方程式などが必要です。思考力の必要性に関して、やや難しいです。問題集でよく見かけるシチュエーションですが、計算が複雑です。
問1に関して、思考問題です。まず、図1の状態「メタノール+酸素」の圧力とモル数を求めましょう。シリンダー内の気体の圧力は「1気圧+水銀7.6cm分」となっています。これを数値で表すと「1.0×10^5×10^-3+1.0×10^5×10^-3× 7.6/76 =1.10×10^2キロパスカル」となります。よって、シリンダー内の気体に状態方程式を用いると「モル数=n=PV/RT=1.10×10^2×(13.6×20×10^-3)/(8.30×300)=0.0120モル」となります。
続いて、シリンダー内の気体を燃焼させた後を考えます。
| CH3OH | +3/2O2 | → CO2 | +2H2O | 総モル数 | |
| 前 | xモル | 1.20×10^-2-x | 0 | 1.20×10^-2 | |
| 中 | -x | -3/2x | +x | ||
| 後 | 0 | 1.20×10^-2-5/2x | x | 1.20×10^-2-3/2x |
上記の表より「燃焼後のO2とCO2のモル数」が分かれば「xの値=燃焼前のメタノールのモル数」が解り正解となります。そこで、状態2のシリンダーを考えます。シリンダー内の圧力のつり合いの式は「CO2+O2+H2O+水銀7.6cm=外圧」であり、水は飽和水蒸気圧なので「CO2+O2=外圧-H2O-水銀7.6cm=1.0×10^5 - 1.0×10^5×7.6/76 - 3.0×10^3=0.87×10^2キロパスカル」となります。よって、シリンダー内の気体の状態方程式より「CO2+O2のモル数=n’=PV/RT=0.87×10^2×(12.9×20×10^-3)/(8.30×300)=9.01×10^-3モル」となります。よって、この値が上記「増減表の右下の値」とイコールでつながるため
- 1.20×10^-2-3/2x=9.01×10^-3
- x=1.99×10^-3≒2.0×10^-3モル(これが正解です)
問2に関して、思考問題です。問2の増減表を見ると、発生する水のモル数は「燃焼で発生したCO2の2倍」と解ります。よって、その質量は「1.99×10^-3×2×18=0.0716グラム」となります。一方、燃焼後に飽和蒸気圧で存在している水の質量は、状態方程式(PV=w/18・RT)を変形して「w=18PV/RT=18×3.0×10^3×10^-3×0.258/(8.30×300)=0.00559グラム」となります。よって「液体の水の質量=燃焼で生じたH2-気体のH2O=0.0716-0.00559=0.0660≒6.6×10^-2グラム」が正解です。
問3に関して、思考問題です。問1作った増減表より「発生したCO2のモル数=燃焼前のメタノールのモル数」と解ります。よって、シリンダー内のCO2に関する状態方程式より「P=nRT/V=2.0×10^-3×8.3×300/0.258=19.3≒1.9×10^4パスカル」が正解となります。
問4に関して、思考問題です。発生したH2Oが全て水蒸気になった瞬間の状態方程式を考えます。この時、水蒸気の圧力は飽和蒸気圧(3.0キロパスカル)に等しいです。よって、求める高さをxとして「V=20x=nRT/P=2.0×10^-3×2×8.3×300/3.0」これを解いて「x=166≒1.7×10^2センチメートル」が正解となります。
受験生としての解説
問1に関して、最初の問題ですが燃焼後の系全体の解析まですることになるため、合格者さんでも正解は難しいです。よって、正解できれば他者に差をつける1問となります。
問2・問3・問4に関して、問1が正解できた人は、高確率で流れに乗って解けるレベルです。よって、問1とセットの関係になっているので、正解できれば他者に差をつける1問です。
- 知識:★★★(普通)
- 思考:★★★★(やや難しい)
- 総合:★★★★(やや難しい)
- 短評:問1が勝負どころ
大問3

講師としての解説
「溶解度」と「電離平衡」と「酸化還元」からの出題です。
知識の必要性に関して、普通程度です。ヘンリーの法則、増減表、半反応式など定番の知識を使います。思考力の必要性に関して、普通程度です。溶解度、化学平衡、割合と計算の種類が豊富です。
問1に関して、思考問題です。まず(1)に関して、大気中のCO2の分圧は「1.0×10^5×0.038%=38パスカル」と解ります。よって、ヘンリーの法則より「CO2の濃度=3.4×10^-2× 38/(1.0×10^5)=0.129×10^-4≒1.3×10^-5モル/リットル」が正解です。
続きて問1(2)に関して、平衡状態を考えるので増減表を書きます。CO2の濃度をc、電離度をαとすると
| CO2 | + H2O | ↔ H+ | + HCO3- | |
| 前 | c | 0 | 0 | |
| 中 | -cα | +cα | +cα | |
| 後 | c(1-α) | cα | cα |
- 電離定数K=[H+][HCO3-]/[CO2]=(cα)^2/c(1-α)=cα^2/(1-α)≒cα^2(CO2が水に溶けた炭酸は弱酸なのでα<0.05は明らか、よって近似できる)
- α=√K/c
- [H+]=cα=√cK=√1.3×10^-5×4.3×10^-7=√5.59×10^-12=2.36×10^-6≒2.4×10^-6モル/リットル」
問2に関して、知識問題です。SO2は酸化剤としては最弱クラスですが、より最弱に近いH2Sが相手の時だけは酸化剤としてはたらきます。よって、両者の半反応式は以下のとおりです。
- H2S → S + 2H+ + 2e・・・①
- SO2 + 4H+ + 4e → S + 2H2O・・・②
- ①×2+②より「2H₂S + SO₂ → 3S + 2H₂O」
問3に関して、思考問題です。右辺に「CaSO₄・2H₂O」が出るを目指して式を作っていきます。とりあえず材料「CaCO₃、H₂O、SO₂、O₂」を左辺に起きます。
- CaCO₃+SO₂+H₂O+O₂ → CaSO₄・2H₂O
- そして左右の原子数を合わせていくと
- 2CaCO₃+4H₂O+2SO₂+O₂ → 2CaSO₄・2H₂O+2CO₂
これで正解です。
問4に関して、思考問題です。問3の反応式より、1モルのSO₂を処理するには1モルのCaCO₃があればよいと解ります。
- 1分間に排出される硫黄:1000グラム×2.4%×1/32=0.75モル
- 必要な石灰石=0.75×100(CaCO₃の式量)=7.5×10グラム(これが正解です)
受験生としての解説
問1に関して、(1)(2)ともにヘンリーの法則・化学平衡の典型的な流れです。しかし、典型=簡単というわけでもなく、不合格者さんの一定数で不正解者が出るレベルです。よって、合否を分ける1問より少し簡単な問題です。
問2に関して、SO₂とH₂Sは酸化還元の中でも有名パターンなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、材料と生成物を両辺に書いて係数をあわせていくだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、問3の式を書けた人にとっては難しくない計算です。よって、問3とセットで全ての受験生さんが正解したい問題です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:問3・問4のセット問題を落としたくない
大問4

講師としての解説
「反応速度」からの出題です。
知識の必要性に関して、ほぼ不要です。化学というより数学の出題です。思考力の必要性に関して、難しいです。図形から数学的意味を読み取る問題が多く、最後はやや複雑な計算が付与されています。
問1に関して、思考問題です。問題文「気体分子の質量と気体分子の平均速度の2乗の積で表され、それは、絶対温度に比例する」をそのまま式にすると「Mv²∝T」となり「v∝√T/M」が(ア)の正解です。
問2に関して、思考問題です。20K上昇させた後の速度をv’とすると「v’/v=√626/M÷√606/M=√1.033・・・≒1.0倍」となり「1.0倍」が(イ)の正解となります。
問3に関して、思考問題です。以下の2点に注意してグラフを選びます。
- 温度が高いT₂で高い運動エネルギーの分子が多く見られる
- 加熱によって全ての分子の運動エネルギーが平均的に上がるわけではなく、分子が持つ運動エネルギーの分布が増す
よって、正解のグラフは(d)となります。
問4に関して、思考問題です。まず、TとEの性質を確認すると
- Tが大きくなるほどグラフが右に動くので、分布面積が増す
- Eが小さくなるほど積分領域が増えるため、分布面積が増す
その上で、分布面積を表すしき「1/e^f」を見ると、EとTの関数fが分母側に来ているため「fが小さくなるほど分布面積が増す」ことが読み取れます。よって
- fが小さくなること
- Eが小さくなること
- Tが大きくなること
が、等価であるため、これを表している式はf=(エ)が正解となります。
問5に関して、思考問題です。問4の正解の理由を35字以内で説明すると「絶対温度を高く活性化エネルギーを低くするほど分布面積が増えるから。」(33字)となります。
問6に関して、思考問題です。まず、中学生のx・yグラフと思って図を眺めてください。関係式は「y=-ax+b」と中学時代に習いました。これを本問に置き換えると
- x軸 → 1/T軸
- y軸 → logk軸
- y切片:b → B
と問題文に書いてあるので値お起き直して「logk=-A/T+B」が正解です。
問7に関して、思考問題です。問6で立てた式に、実際に値を代入して数値を求めます。求める値は「k2/k1=(エ)倍」なので
- log(k2/k1)=logk2-logk1=-21890/626-(-21890/606)=1.15(なぜなら問6より)
となり「k2/k1=e^1.15」となります。
- log₁₀(k2/k1)=1.15log₁₀e=1.15×0.4343=0.4999≒0.50
- よって、k2/k1=10^0.5=√10=√2×√5=1.414×2.236≒3.2倍(これが正解です)
受験生としての解説
問1に関して、問題文に書いてある通りに立式するだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、「何倍になりますか?」と問われて「1.0倍になります」と答えるのは勇気が要ります。そこさえ乗り越えれば、計算は簡単なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、不合格者さんの中に一定数の不正解者が出るレベルです。合格者さんは正解してきます。よって、合否を分ける1問より少し簡単な問題です。
問4・問5・問6・問7に関して、判定が難しい問題です。化学の学力を基準に「合格・不合格レベル」で分かれるというより、数学が得意な人ほど有利な問題です。レベル的には、問4~問6が「合否を分ける1問より少し難しいレベル」問7が「医学科の合否を分けるレベル」とみなせます。
- 知識:★(ほぼ不要、数学の問題)
- 思考:★★★★★(難しい)
- 総合:★★★★(やや難しい)
- 短評:数学が得意な人ほど有利
大問5

講師としての解説
「構造決定」からの出題です。
知識の必要性に関して、やや簡単です。構造決定の中でも簡単な部類、頻出の物質ばかりです。思考力の必要性に関して、やや簡単です。計算は組成式とフタル酸の分子量の確認。問題はあまり深入りしておらず、知識問題の様な展開です。
問1に関して、知識問題です。エチレンやプロピレンに臭素を入れる脱色されるのは、不飽和結合への「ア:付加」反応が起こるためです。ベンゼンに濃硫酸を加えて加熱すると「イ:スルホ」基を導入することを「ウ:置換」反応といいます。化合物A~Fがベンゼン環に直結したヒドロキシ基を持たない事は、「エ:塩化鉄(Ⅲ)」水溶液を加えても特有の紫色を示さないことで確認できます。
問2に関して、思考問題です。元素の質量比が既に当たられているので、分子量で割れば組成式が求まります。「C:H:O=64.9/12 : 6.3/1 : 28.8/16 =6:7:2」より、組成式「C6H7O2」が正解です。
問3に関して、知識問題です。「ヨウ化カリウム、水酸化ナトリウム、黄色沈殿」より、化合物Dはヨードホルム「CHI₃」が正解です。
問4に関して、思考問題です。問題文「Eを加熱すると水蒸気を発して化合物Fが生成した。Fは水と反応してEに戻る」より、FはEの無水物と解ります。本問は主に芳香族の話題で進んできたため「芳香族で無水物を生じる」と言えば、フタル酸です。フタル酸の分子量を計算すると「C8H6O4=166」これは問題文「化合物Eの分子量を測定すると166」に一致するため「Eはフタル酸」で確定です。よって「Fは無水フタル酸」で確定です。
問5に関して、知識問題です。酸化されてフタル酸を生じる芳香族炭化水素なので、以下の条件を満たす構造式を1つ書けば正解です。
- ベンゼン環に直結する炭素が2つある
- 2つの炭素はオルト位
受験生としての解説
問1に関して、基本知識の語句問題なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、組成式の導出なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、ヨードホルムの化学式を書くだけなので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、無水物である事、フタル酸である事が解りやすく書いてあるので、不合格者さんでも正解してきます。しかし、一定数は不正解になるレベルでもあります。よって、合否を分ける1問より少し簡単な問題です。
問5に関して、問4とセットの関係で、問4が正解できた学生さんなら容易に正解できます。よって、問4とセットで合否を分ける1問より少し簡単な問題です。
- 知識:★★(やや簡単)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:完答したい1問
大問6A
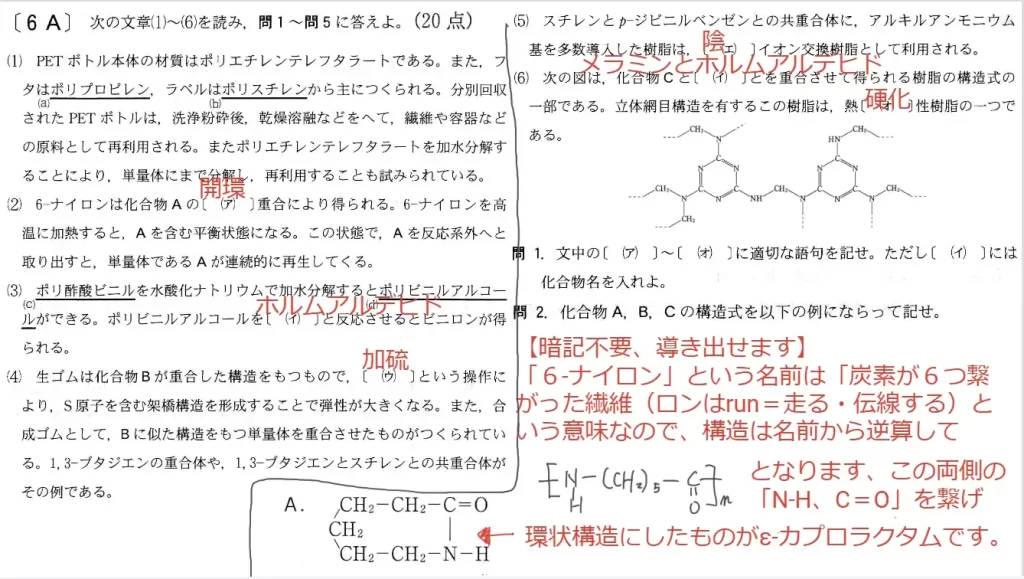
講師としての解説
「合成高分子」からの出題です。
知識の必要性に関して、普通程度です。合成高分子に関する基本知識一式で正解できます。思考力の必要性に関して、普通程度です。問5の応用問題はやや難しいですが、問4の計算問題は共通テストと同等です。
問1に関して、知識問題です。6-ナイロンはε-カプロラクタムの「ア:開環」重合で得られます。ポリビニルアルコールを「イ:ホルムアルデヒド」と反応させるとビニロンが得られます。生ゴムはイソプレンが重合した構造を持つもので、「ウ:加硫」という操作により、S原子を含む架橋構造で弾性が増します。スチレンとp-ジビニルベンゼンの共重合体に、アルキルアンモニウム基を多数導入した樹脂は「エ:陰」イオン交換樹脂として利用されます。メラミンとホルムアルデヒドを重合させて得られるメラミン樹脂は立体網目構造をしており、熱「オ:硬化」性樹脂の一つです。
問2に関して、思考問題です。まず化合物Aに関して、問題文「6-ナイロンは化合物Aの開環重合により得られる」より、Aは「ε-カプロラクタム」で確定です。
【丸暗記回避テクニック】
- 普通は材料の「ε-カプロラクタム」→ 製品の「6-ナイロン」という順番で憶えますが、反対に「6-ナイロン → ε-カプロラクタム」と導きます
- 「6-ナイロン」という名前は「炭素が6個つながった繊維」という意味(ロンはrun=走る・伝線する)なので、炭素を6つ使ってアミド結合で繋いでください
- 構造式([NH-(CH2)5-CO]n)が自然に出てきます。つまり「名前の通りに書くだけ」です。
- 後は、両端のN-HとC=Oをつないで輪っかの形にすれば、それが「ε-カプロラクタム」です
問2化合物Bに関して、問題文「生ゴムは化合物Bが重合した構造」より、Bは「イソプレン」で確定です。化合物Cに関して、問題文「次の図は、化合物Cとホルムアルデヒドとを重合させて得られる樹脂」と問題文に描いてある図より、化合物Cは「メラミン」で確定です。
問3に関して、知識問題です。
- a:ポリプロピレン
- b:ポリスチレン
- c:ポリ酢酸ビニル
- d:ポリビニルアルコール
上記4つの中で最も水溶性が高いのは「-OH基」を持つ「d:ポリビニルアルコール」が正解です。
問4に関して、思考問題です。ポリエチレンテレフタラートは、エチレングリコールとテレフタル酸をn個ずつ並べ、2n回脱水したものと考える事ができます。ポリエチレンテレフタラートの繰り返し単位の分子量は192nなので、比の式「ポリエチレンテレフタラート:水=192n:18×2n=1.20グラム:xグラム」が立ち、これを解いた「x=2.25×10^-1グラム」が正解となります。
問5に関して、思考問題です。やや複雑な問題なので、ゴールから辿って「何を求めればよいか」を確認しましょう。最終的に欲しいのは「付加する臭素の質量」なので「臭素の質量 → 臭素のモル数 → 二重結合の数 → 共重合体の構造 → ブタジエンとスチレンの比率」と解ります。よって、本問は「共重合体に含まれるブタジエンとスチレンの比率を求める問題」と言い換える事ができるので、繰り返し単位内のブタジエンの個数をx、スチレンの個数をyと置いて考えます。
- 問題文より、C:H=35.2/44 :9.00/18×2=4:5
- よって、重合体の組成式はC₄H₅
- 重合体の構造式[(ブタジエン)x(スチレン)y]nに含まれるCとHの質量より「C:H=4x+8y:6x+8y=4:5」
- これを解いて「x=2y」より、重合体の構造式は[(ブタジエン)2(スチレン)1]n(分子量212n)と決まる
- よって、重合体212グラム毎に2モルの臭素が付加できるので、比の式「重合体:臭素=212:79.9×2×2=5.30グラム:zグラム」が立つ
- これを解いて「z=7.99グラム」が正解
受験生としての解説
問1に関して、樹脂に関する基礎知識で憶えるだけすが、不合格者さんの中には一定数の不正解者が出るレベルです。合格者さんは正解してきます。よって、合否を分ける1問より少し簡単な問題です。
問2に関して、憶えるだけの知識問題ではありますが、不合格者さんの中には一定数の不正解者が出ます。合格者さんは正解してきます。よって、合否を分ける1問より少し簡単な問題です。
問3・問4に関して、本問も基礎レベルではありますが、合格者さんが正解してくるのに対し、不合格者さんの一定数が不正解になります。よって、合否を分ける1問より少し簡単な問題です。
問5に関して、最後に応用問題が来ました。合格者さんでも難しいレベルなので、正解できれば他者に差をつける1問となります。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:問4まで正解したい
大問6B

講師としての解説
「天然繊維」と「発酵」からの出題です。
知識の必要性に関して、普通程度です。ピルビン酸という高校化学の範囲外の物質が扱われていますが、それに対するフォローは少ないです。思考力の必要性に関して、普通程度です。ピルビン酸は「考えて導き出す」という形で問題に使われていますが、取り付きにくいです。他の問題はやや簡単です。
問1に関して、知識問題です。生物系の語句問題を5つ答えます。木綿の主成分「ア:セルロース」を衣類の材料とするために無水酢酸と反応させ「イ:アセチルセルロース」にします。一方、セルロースを溶液に溶かし、再び長繊維として取り出したものを「ウ:再生繊維」といいます。セルロースはグルコースが「エ:縮合」重合した高分子です。酵母菌はピルビン酸1分子を、1分子のエタノールと1分子の「オ:二酸化炭素」に分解します。
問2に関して、思考問題です。材料のセルロースと終点のエタノールの間には以下の関係があります。
- セルロース=nグルコース+nH₂O
- nグルコース=2n(エタノール+CO₂)
よって「セルロース:エタノール=162n:46×2n=80グラム:xグラム」という比の式が立つので、これを解いて「x=4.5×10グラム」が正解となります。
問3に関して、思考問題です。まず(1)ピルビン酸の構造に関して、下線部bの直後に「ピルビン酸は還元のみで乳酸を生じる」と書いてあるので、乳酸からHを2個取り去ったものがピルビン酸です。ピルビン「酸」と書いてあるので-COOHが存在すると推定できます。(2)ピルビン酸からエタノールへ向かう中間体に関して。ピルビン酸からCO₂を抜いたものが中間体となるため、正解は「アセトアルデヒド」となります。
問4に関して、思考問題です。セルロース(分子量162n)の重合度をnとすると、そこから乳酸が2nモル得られます。この内47%が乳酸発酵に使われたので、乳酸のモル数は「80/162n ×2n×47%」となります。一方、そのポリ乳酸(重合度n’とする)は1.0×10^-2モルだったので、合成に使われた乳酸のモル数は「1.0×10^-2×n’」となります。よって「80/162n ×2n×47%=1.0×10^-2×n’」を解いて、「n’≒46」が正解となります。
問5に関して、思考問題です。乳酸2分子を前後逆向きにして並べ、互いに「-COOHと-OH」「-OHと-COOH」でエステル結合を作ってください。環状構造ができ、正解となります。
受験生としての解説
問1に関して、基本知識なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、質量の計算としては簡単な部類なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、合格者さんでも厳しい問題です。まず主役の「ピルビン酸」ですが、高校の指導範囲外なので知らなくて大丈夫です。その上で、ピルビン酸に関する説明無しで「ピルビン酸の構造を答えよ」と来ていますから、合格者さんでも難しい出題でした。
問4に関して、やや複雑な計算問題なので不合格者さんには厳しく、合格者さんは正解してきます。よって、合否を分ける1問です。
問5に関して、下線部dに「環状」と書いてあるので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:問3以外はやや簡単
九州大学の化学2007年・平成19年度
大問1

講師としての解説
「原子」からの出題です。
知識の必要性に関して、簡単です。電子殻、酸化数などの知識を問われています。思考力の必要性に関して、やや簡単です。存在割合から原子量を導く計算があります。
問1に関して、知識問題です。塩素原子は典型元素なので、電子殻の内側から規則的に電子が入ります。よって(ア)は「K²L⁸M⁷」が正解です。最外殻電子の数は「イ:7」個です。
問2に関して、知識問題です。塩素原子には最外殻電子が7個あるので、酸化数の幅は電子を1つ仕入れた「-1」から最外殻電子をすべて失った「+7」まであります。また、Cl原子の酸化数が+3のオキソ酸ナトリウム塩は「NaClO₂」です。
問3に関して、思考問題です。原子量の計算式は「質量数×存在割合」を足したものなので「35.0×75.8/100 + 37.0×24.2/100≒35.5」が(オ)の正解です。そして、塩素は2原子分子なので「(オ)×2=71.0」が(カ)の正解です。
問4に関して、思考問題です。「³⁵Cl:³⁷Cl=3:1」なので、Cl₂の存在比は以下の表となります。
| ³⁵Cl | ³⁷Cl | |
| ³⁵Cl | 9 | 3 |
| ³⁷Cl | 3 | 1 |
よって「質量数70:72:74=9:6:1」が正解です。
受験生としての解説
問1~問4に関して、共通テストと同等なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★(簡単)
- 思考:★★(やや簡単)
- 総合:★(簡単)
- 短評:完答したい1問
大問2

講師としての解説
「電気分解」からの出題です。
知識の必要性に関して、普通程度です。この電気分解では水が電子の授受に関わっており、液性によって反応式が変化します。思考力の必要性に関して、やや簡単です。各電極での反応式がわかれば、計算は難しくありません。
問1に関して、知識問題です。電気分解に関する語句問題を10個答えます。水に溶けるとアルカリ性を示し、ほぼ完全に電離する物質を「ア:強塩基」といいます。図の電気分解において、負極の電極Bでは「イ:水」が電子を受け取って「ウ:水酸化物イオン」を生じ、気体の「エ:水素」が発生しています。一方、正極の電極Aでは気体の「オ:酸素」が発生しています。上記の反応に伴い、水溶液中では「カ:水酸化物」イオンが「キ:②」の向きに移動し、これによってNaOHの濃度が均一に保たれています。しかし、図2の様に陽イオン交換膜で仕切ると「ク:ナトリウム」イオンが「ケ:①」の向きに移動するので、電極「コ:B」が存在する側の溶液中には水酸化ナトリウムが濃縮されます。
問2に関して、知識問題です。水溶液中に重金属イオンは無く、液性は塩基性なので「4OH⁻ → 2H₂O+O₂+4e」が正解の反応です。
問3に関して、思考問題です。陰極は
- 白金電極であり
- 溶液にハロゲンイオンは存在せず
- 液性は塩基性なので
「2H₂O+2e → H₂+2OH⁻」という反応が起きています。よって、電子が1モル流れる度にOH-が1モル生じ、陽極側からNa⁺が来るので、NaOHが1モル生じていることになります。よって、求める式は「(既存のNaOH+電極Bで生じたNaOH)×1000/100=(0.100× 100/1000 + 0.150×2.00×10³/96500)×1000/100≒1.31×10⁻¹モル/リットル」が正解です。
受験生としての解説
問1に関して、電気分解の基礎知識なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、電気分解で水が電子の授受をする場合、不合格者さんには難しいレベルとなります。合格者さんは正解してくるので、合否を分ける1問です。
問3に関して、標準的な問題ですが不合格者さんの一定数が不正解になるレベルです。合格者さんは正解してくるので、合否を分ける1問より少し簡単な問題です。
- 知識:★★★(普通)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:完答したい1問
大問3

講師としての解説
「反応速度」からの出題です。
知識の必要性に関して、普通程度です。濃度計算、反応速度の知識があれば正解できます。思考力の必要性に関して、やや難しいです。加水分解と中和反応が同時に起きている中での濃度計算・速度計算なので、混乱しやすい作りとなっています。
問1に関して、知識問題です。酢酸エチルの加水分解の式(CH₃COOC₂H₅+H₂O → CH₃COOH+C₂H₅OH)を書くと解りますが、塩酸が出てきません。よって、塩酸は「触媒作用」が正解となります。
問2に関して、知識問題です。正解の1つは、固体水酸化ナトリウムの特徴として頻出の潮解性です。「空気中の水蒸気を吸収するから(14文字)」が正解です。もう1つの正解は塩基性で「空気中の二酸化炭素と反応する(14文字)」となります。
問3に関して、思考問題です。二水和物という事で計算が厄介になりそうですが、二水和物を「加えた後の状態」と考えれば、二水和物の水も含めて「溶媒」となります。こうなればただの濃度計算です。
- シュウ酸のモル数:0.10×50/1000・・・①
- シュウ酸のモル数:x/126・・・②
- ①=②より、x=0.10×50/1000×126=6.3×10⁻¹グラム(これが正解です)
問4に関して、思考問題です。問題文「酸の総量」とは「最初に入っていたHClの水素イオン+加水分解によって発生したCH₃COOHの水素イオン」です。
| CH₃COOC₂H₅ | +H₂O | ↔CH₃COOH | +C₂H₅OH | |
| 前 | csV/1000モル | 0 | 0 | |
| 中 | -csV/1000×2/5 | +csV/1000×2/5 | +csV/1000×2/5 | |
| 後 | csV/1000×3/5 | csV/1000×2/5 | csV/1000×2/5 |
よって、水酸化ナトリウムの体積xとして「csV/1000×2/5 + cAV/1000 = cBx/1000」を解いて、「x=V/cB(cA+2cs/5)」が正解です。
問5に関して、思考問題です。この反応における酸と水酸化ナトリウムは1:1で反応するため、中和に要した水酸化ナトリウムのモル数「cBV1/1000」がそのまま「残っていた酸のモル数」となります。この内「cAV/1000」はHCl由来なので、酢酸エチル由来は「cBV1/1000 - cAV/1000」となります。つまり、酢酸エチル由来の濃度は(cBV1/1000 - cAV/1000)×1000/V・・・①です。ここで「反応開始時の酢酸の濃度=0」より「反応速度=(①-0)÷Δt=(cBV1-cAV)/VΔt」が正解となります。
大問6に関して、思考問題です。反応速度の式は速度定数k1として「v=k1[濃度]」と表すことができます。今、反応開始時の速度を「平均反応速度」とみなしてよいとの事なので「問5の正解=k1cs」となります。よって、式変形より「k1=(cBV1-cAV)/VΔtcs」が正解となります。
受験生としての解説
問1に関して、金属ではなく液体の塩酸が触媒という事で、不合格者さんの一定数が不正解になるレベルです。よって、合否を分ける1問より少し簡単な問題です。
問2に関して、水酸化ナトリウムの「潮解性・塩基性」は不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、不合格者は「二水和物」に惑わされて計算が止まるレベルです。合格者さんは正解してくるので、合否を分ける1問です。
問4に関して、計算が複雑になってきましたが「モル数=モル数」で正解を出せるので、不合格者さんでも一定数は正解してきます。よって、合否を分ける1問より少し簡単な問題です。
問5に関して、酢酸の濃度変化が反応速度計算に使えると気づく事が難しいですし、それが解ってもかなりの計算が待ち構えています。よって、合格者さんでも難しい問題なので、正解できれば他者に差をつける1問となります。
問6に関して、本問に参加するためには問5の正解が必要です。問5を正解できた人にとって、問6の正解は難しくないため、問5とセットで、正解できれば他者に差をつける1問となります。
- 知識:★★★(普通)
- 思考:★★★★(やや難しい)
- 総合:★★★★(やや難しい)
- 短評:問3まで正解したい
大問4
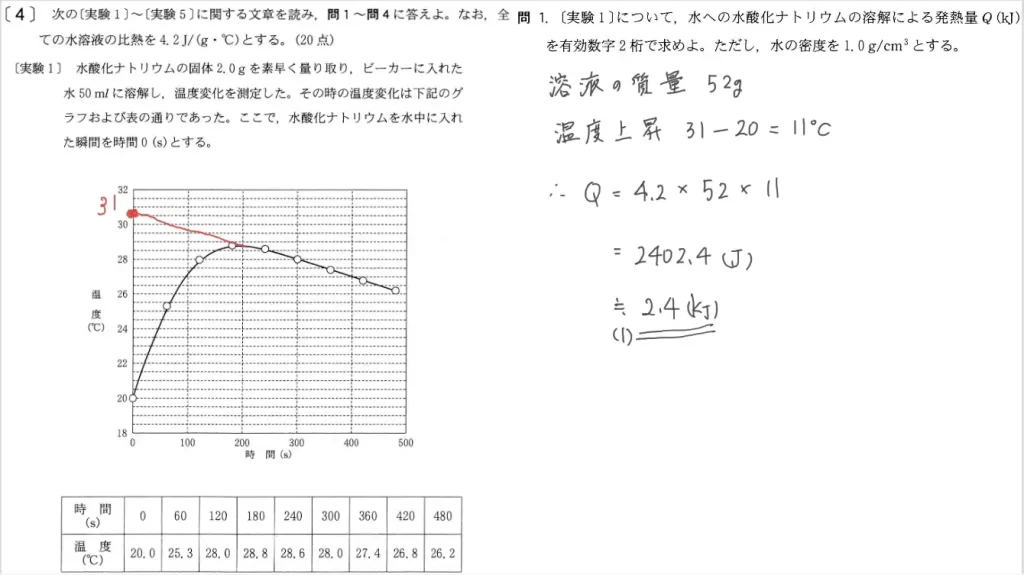
講師としての解説
「溶解熱・中和熱」からの出題です。
知識の必要性に関して、やや簡単です。温度上昇グラフの見方、溶解熱、中和熱などの知識が必要です。思考力の必要性に関して、普通程度です。問1~問4まであまり難しくない計算ですが、それだけに素早い処理が求められます。
問1に関して、思考問題です。水酸化ナトリウムを溶かしたことで、溶液の質量は52g(50+2.0)となっています。また、グラフを真っ直ぐ伸ばしたy切片が31℃なので、温度上昇は11℃(31℃-20℃)となります。よって「発熱量Q=4.2×52×11≒2.4kJ」が正解です。
問2に関して、思考問題です。
- NaOHの物質量:2.0/40=0.050モル
- HClの物質量:1.0×75/1000=0.075モル
- 発熱量:(52+75)×4.2×5.4=2880.36(J)
上記より、中和反応に使われた物質量は0.050モルです。中和熱は1モルあたりの発熱量なので「中和熱=2880.36÷0.050≒58kJ」が正解です。
問3に関して、思考問題です。求めるアンモニアの体積をxリットルとおくと
- 残っている水素イオン:0.075-0.050=0.025モル
- アンモニアの物質量:x/22.4モル
- 溶液の体積:2.0リットル
- 溶液の最終的な水素イオン濃度:1.0×10⁻³モル/リットル
よって、溶液の水素イオン濃度に関して「(0.025-x/22.4)×1/2.0=1.0×10⁻³」という式が成り立ち、これを解いて「x≒5.2×10⁻¹リットル」が正解です。
問4に関して、思考問題です。本問の発熱に関して
- まず、硫酸を水に入れた溶解熱が発生する
- 次に、硫酸と水酸化ナトリウムの中和熱が発生する
という2段階のプロセスで考えます。実験4のデータより「溶解熱=(100×1.0+10×1.8)×4.2×25=12390(J)」と解ります。続いて中和熱に関して
- 投入した硫酸:18×10/1000=0.18モル
- 溶液中の水酸化ナトリウム:1.0×100/1000=0.10モル
- 反応割合「硫酸:水酸化ナトリウム=1:2」
- 中和反応したモル数:0.10モル
よって、問2より「中和熱=57.6×0.10=5.76kJ」となり、正解は「発熱量Q=溶解熱+中和熱=12390(J)+5.76(kJ)≒18kJ」となります。
受験生としての解説
問1に関して、グラフを真っ直ぐ伸ばしたy切片が本当の温度上昇という事は、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、中和熱の計算は難しくないので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、やや難しくなりましたが、それでも不合格者さんが正解してくるレベルです。よって、全ての受験生さんが正解したい問題です。
問4に関して、溶解熱+中和熱という2段構造は見えやすいですが、不合格者さんには少し厳しい計算です。合格者さんは正解してくるので、合否を分ける1問です。
- 知識:★★(やや簡単)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:完答したい1問
大問5
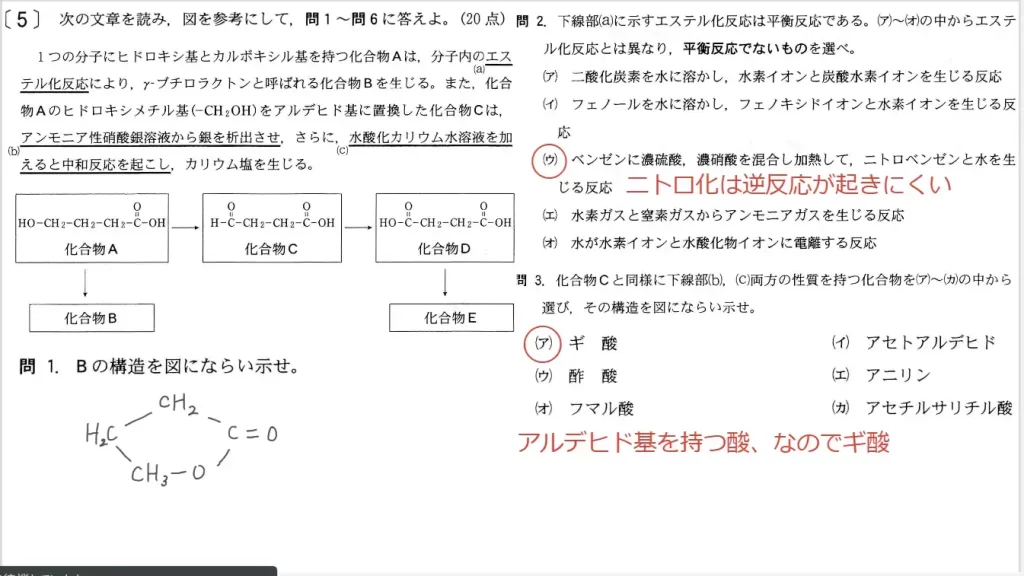
講師としての解説
「構造決定」からの出題です。
知識の必要性に関して、やや簡単です。小問1~6まで共通テストと大差ない基本知識で解けます。思考力の必要性に関して、やや簡単です。問1・3・5・6がパズルの様な問題ですが、いずれも即答できる簡単さです。
問1に関して、思考問題です。問題文「Aを分子内エステル結合でB」という内容より、Aの両端を折り曲げて近づけ、-OHと-COOHから脱水(-H₂O)し、環状構造としたものが正解です。
問2に関して、知識問題です。選択肢ア~オの中で平衡でない(左→右への一方通行)反応は(ウ)のニトロ化です。
問3に関して、知識問題です。
- 下線部bは「還元性」
- 下線部cは「酸性」
を表しているため「還元性を持つ酸」と言えば「ア:ギ酸」となります。残り5つの選択肢でこの条件を満たしているものはありません。
問4に関して、知識問題です。下線部bの反応名は「銀鏡反応」です。
問5に関して、思考問題です。カルボキシル基を2つ持つ分子を加熱すると何かが起きる、という事で有機化学のフタル酸でよく見る「分子内脱水」が起こると解ります。よって、両端のカルボキシ基を真ん中に寄せて脱水(-H₂O)し「-O-」を構造を作ったものが正解です。
問6に関して、思考問題です。化合物Cの左から2番めの炭素原子で「H → COOH」と置き換えると、不斉炭素原子になります。
受験生としての解説
問1に関して、エステル結合を組むだけなので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、事前に準備できる知識ではなく、また考えて正解できるものでもないため、不合格者さん・合格者さんの中に一定数の正解・不正解が出るタイプです。ただ、練習を重ねるほど「ニトロ化の逆反応が起きているのを見たことがない」事が経験的に解ってくるので、合格者さんの方が正解は多くなります。
問3に関して、「還元性を持つ酸=ギ酸」は化学の重要ポイントなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、反応名を答えるだけなので、全ての受験生さんが正解したい問題です。
問5に関して、分子内脱水は合格者さんは正解してくるレベル、不合格者さんの一定数が不正解になるレベルです。よって、合否を分ける1問より少し簡単な問題です。
問6に関して、不斉炭素を見つけるパズル問題なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★★(やや簡単)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:素早く完答したい1問
大問6
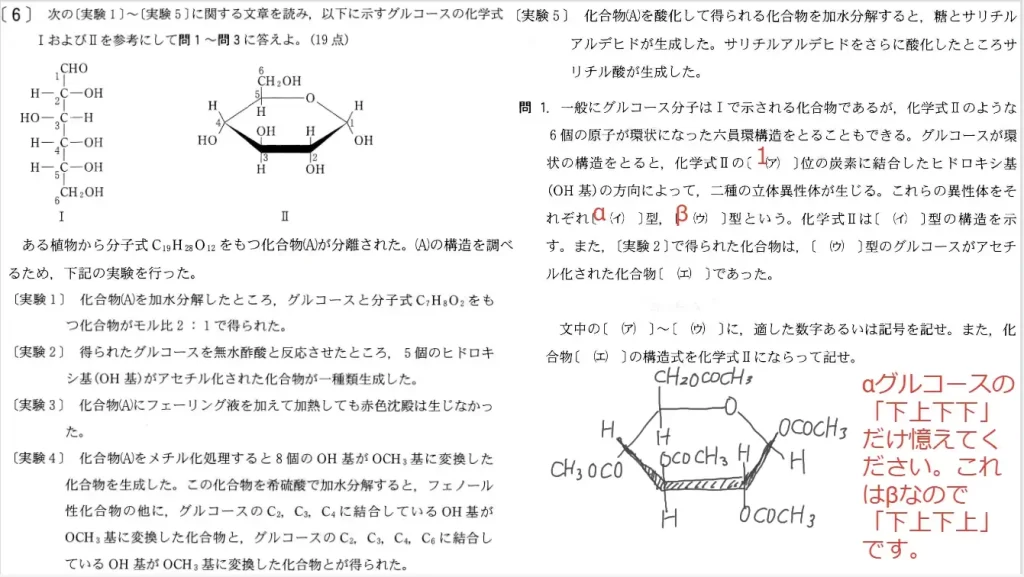
講師としての解説
「二糖類」からの出題です。
知識の必要性に関して、普通程度です。グルコースのヒドロキシ基の「メチル化・アセチル化」は勉強が行き届きにくい部分なので、勉強量を問われています。思考力の必要性に関して、普通程度です。メチル化された部分から「結合部位」を見つける部分で思考力を要します。
問1に関して、思考問題です。本問のベースは「β-グルコース」なので、α-グルコースの1位の炭素の「-Hと-OHの上下」を入れ替えた構造をまず書きます。次に、アセチル化と書いてあるので「-OH」の横に「HOCOCH₃」を並べ脱水縮合(-H₂O)した構造が正解となります。
問2に関して、思考問題です。実験1~実験4で読み取れる事は以下のとおりです。
- α-グルコースが2つ繋がった形
- 一方のグルコースは1位と6位の炭素が結合に使われている
- もう一方のグルコースは1位の炭素が結合に使われている
上記の条件を満たす選択肢、CかDが正解です。
問3に関して、思考問題です。グルコース2個の構造は問2で解っているので、残った部分を考えましょう。「酸化して加水分解したらサリチルアルデヒド(おそらくサリチル酸の-COOHが-CHOになったもの)」と書いてあるので、元の構造は
- フェノールの-OHの隣に1級アルコール(-CH2OH)が付いたもの
- フェノールの-OHを使ってグルコースと結合している
と解ります。この情報だけで正解の構造が判明します。
受験生としての解説
問1に関して、グルコースの構造を描いてアセチル化するだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、不合格者さんには「グルコースのヒドロキシ基のメチル化」は厳しいです。合格者さんは正解してくるので、合否を分ける1問です。ただ、本問は「6択中2つが正解」なので、実験1~実験4から少しでもヒントを拾えれば、後は運で当たってしまう問題でもあります。
問3に関して、合格者さんでも一定数の不正解者が出るレベルです。よって、正解できれば他者に差をつける1問です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:合否を分ける1問
大問7A

講師としての解説
「高分子」からの出題です。
知識の必要性に関して、やや簡単です。問1~問3は尿素と塩化ビニルの構造がややメジャーではないですが、九大受験では普通です。問4のフェノールの正しい構造もややメジャーではないですが、九大受験では普通です。思考力の必要性に関して、簡単です。全て知識問題で考える事は特にありません。
問1に関して、知識問題です。尿素に関する語句問題を5つ答えます。硫酸アンモニウムや塩化アンモニウムと並び「ア:尿素」は重要な窒素肥料です。また、化粧品の保湿成分としても使われますが、その理由は水分子を「イ:水素」結合で保持するからです。高濃度の尿素はタンパク質内部の水素結合を破壊し、立体構造を変化させてタンパク質の正常な機能を奪います。この事をタンパク質の「ウ:変性」といいます。酸性条件下で尿素と「エ:ホルムアルデヒド」を脱水縮合させて得られる樹脂は、加熱しても軟化しません。この性質を持つ樹脂を「オ:熱硬化性」樹脂といいます。
問2に関して、知識問題です。尿素とホルムアルデヒドの構造式を描けば正解です。
問3に関して、知識問題です。「ポリ」はギリシャ語で「たくさん」の意味なので、ポリプロピレンの原料は「プロペン」、ポリ塩化ビニルの原料は「塩化ビニル」となります。正解は以下のとおりです。
- プロペンはプロパンのアルキン:CH₂=CH-CH₃
- 塩化ビニルはビニル基+塩化物イオン:CH₂=CH-Cl
問4に関して、知識問題です。フェノール樹脂は、フェノールをホルムアルデヒドでつないだものなので、選択肢(C)がまず脱落します(Cはメラミン樹脂)そして、フェノール樹脂の正しい構造は選択肢(E)であり、これが正解です。
受験生としての解説
問1に関して、メジャーな語句が主体なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、構造式を描くだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、プロペンと塩化ビニルを描くだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、フェノール樹脂の「正しい」構造を選ぶ問題なので、不合格者さんにはやや難しいです。合格者さんは正解してくるレベルなので、合否を分ける1問です。
- 知識:★★(やや簡単)
- 思考:★(簡単)
- 総合:★(簡単)
- 短評:完答したい1問
大問7B

講師としての解説
「アミノ酸」からの出題です。
知識の必要性に関して、普通程度です。アミノ酸の4大検出(キサントプロテイン・ニンヒドリン・硫黄・ビウレット)を問われています。思考力の必要性に関して、やや簡単です。ポリペプチドの計算問題がありますが、重合同100なので難しくありません。
問1(1)に関して、知識問題です。アミノ酸に関する語句問題を3つ答えます。アミノ酸は水溶液中では「ア:双性イオン」陽イオン、陰イオンの平衡状態で存在しています。また、アミノ酸の正電荷・負電荷が釣り合って分子全体として電化が0になるpHを「イ:等電点」といいます。pH12のグリシン水溶液に電極を入れて電流を流すと、グリシンは「ウ:陽」極側へ移動します。
問1(2)に関して、知識問題です。pH=7の状態においてグルタミン酸のアミノ基・カルボキシ基は全てイオン化した状態で存在するため、選択肢(D)が正解です。pH=12において、溶液はOH⁻があふれ返っているためグルタミン酸の「-NH₃⁺」は「-NH₂」になっています。よって、選択肢(F)が正解です。
問1(3)に関して、知識問題です。まず、リシンのアミノ酸側鎖は「-(CH₂)₄-NH₂」です。pH=1の状態では溶液中にH⁺があふれ返っているため、リシンの「-NH₂」を「-NH₃⁺」に変えれば正解です。
問2に関して、知識問題です。まず、グリシンのアミノ酸側鎖は「-H」である事を確認しておきます。その上で、アミノ酸の検出法4つと検討していきます。
- ア:「濃硝酸を加えて黄色」なのでキサントプロテイン反応です。これは「ベンゼン環のニトロ化」によって起きる反応なので、ポリグリシンは関係ありません
- イ:「水酸化ナトリウム、硫酸銅(Ⅱ)、赤紫色」よりビウレット反応です。これは「2個以上のペプチド結合」によって起きる反応なので、多数のペプチド結合を持つポリグリシンは反応します。
- ウ:「酢酸鉛(Ⅱ)」より硫黄反応です。これは「S原子を含むアミノ酸・タンパク質」によって起きる反応なので、ポリグリシンは無関係です。
- エ:「ニンヒドリン溶液」よりニンヒドリン反応です。これは「アミノ酸・タンパク質」によって起きる反応なので、ポリグリシンは反応します。
以上より、(イ)(エ)が正解です。
問3に関して、思考問題です。重合体100のポリグリシンの作り方は
- グリシンを100個並べる:75×100=7500
- 99回脱水縮合する:-18×99=-1782
よって、「ポリグリシンの分子量=7500-1782=5718」が正解です。
受験生としての解説
問1(1)に関して、簡単な語句問題なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問1(2)に関して、「等電点」は丸暗記で済ませやすいポイントであり、不合格者さんの一定数は「等電点のしくみ」を知りません。本問の正解にはしくみを知っておく必要があるため、不合格者さんの一定数が正解できず、合格者さんは正解してきます。よって、合否を分ける1問より少し簡単な問題です。
問1(3)に関して、まず不合格者さんの一定数が「リシンの構造式」を知りません。そして、同じく不合格者さんの一定数が「等電点のしくみ」を知らないため、合わせ技で不合格者さんには厳しい問題となります。合格者さんは正解してくるので、合否を分ける1問です。
問2に関して、アミノ酸・タンパク質の4大検出を憶えるだけですが、不合格者さんの一定数が不正解となります。合格者さんは正解してくるので、合否を分ける1問より少し簡単な問題です。
問3に関して、グリシンは不合格者さんでも知っているため、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★★★(普通)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:完答したい1問
九州大学の化学2006年・平成18年度
大問1

講師としての解説
「遷移元素」と「窒素」からの出題です。
知識の必要性に関して、普通程度です。錯イオンの反応式、銅と硝酸に関する酸化還元の式、記述解答ではありますが有名な式なので普通レベルです。思考力の必要性に関して、普通程度です。定番の銅と硝酸のモル数計算に蒸気圧で少し変化を加えています。
問1に関して、知識問題です。金属に関する語句問題を5つ答えます。周期表の「ア:11」族に属する遷移元素としては、第4周期のCu、第5周期の「イ:Ag」第6周期の「ウ:Au」があります。銀の単体の電気伝導性と「エ:熱」伝導性は全金属の中で最大です。金の単体は展性・延性に富み、硝酸とは反応しませんが、濃硝酸と「オ:濃塩酸」の体積比1:3の混合液には溶解します。
問2に関して、知識問題です。Zn、Cu、Ag(ゴロ合わせ:安藤銀さん)はNH₃を加えると一旦は水酸化物(Agは酸化物)として沈殿しますが、NH₃を過剰に加えると沈殿が錯イオンとなって再び溶けます。その反応式は「Cu(OH)₂+4NH₃ → [Cu(NH₃)₄]²⁺+2OH⁻」が正解です。イオン反応式は化学反応式の一部なので、式内にイオンが残った状態で提出して大丈夫です。
問3(1)に関して、思考問題です。まず、銅に希硝酸なので発生した気体Xは一酸化窒素です(3Cu+8HNO₃ → 3Cu(NO₃)₂+4H₂O+2NO)その蒸気圧は「101.3-3.56=97.74kPa」よって、状態方程式より「n=PV/RT=97.74×1.00/(8.31×300)モル」であり、求める質量は「n×30.0≒1.18グラム」が正解です。
問3(2)に関して、思考問題です。上記「銅と希硝酸の反応式」より、3モルのCuが消費されると2モルのNOが発生すると解ります。よって、「残った銅の質量=最初の質量-消費された質量=5.00-97.74×1.00/(8.31×300) × 3/2 ×63.5≒1.3グラム」が正解です。
問4(1)に関して、知識問題です。まず、銅に濃硝酸をなので反応式「Cu+4HNO₃ → Cu(NO₃)₂+2H₂O+2NO₂」より、二酸化窒素が発生します。そして、二酸化窒素と水の反応式は「3NO₂+H₂O → 2HNO₃+NO」となり、これが正解です。
問4(2)に関して、知識問題です。二酸化窒素と四酸化二窒素の平衡反応なので「2NO₂ ↔ N₂O₄」が正解となります。
受験生としての解説
問1に関して、共通テストと同等の語句問題なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、ゴロ合わせ「安藤銀さん」の頻出問題なので、反応式を書かせるタイプとはいえ不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3(1)に関して、捕集した気体の圧力経由でモル数を表す部分がややテクニカルです。合格者さんは正解してきますが、不合格者さんの一部は不正解になるレベルです。よって、合否を分ける1問より少し簡単な問題です。
問3(2)に関して、こちらはよくある質量計算なので、不合格者さんでも正解してきます。しかし、本問に参加するためには問3(1)の正解が必要なので、(1)とセットで合否を分ける1問より少し簡単た問題です。
問4(1)に関して、銅と濃硝酸の反応式は酸化還元トップクラスの重要式なので、不合格者さんでも書けます。続いて、二酸化窒素が水に溶ける式ですが、これは硝酸の製法(オストワルト法)の1つでかなり重要な式ですが、不合格者さんには難しいレベルです(特にNOが右辺に残る部分)合格者さんは正解してくるので、合否を分ける1問です。
問4(2)に関して、二酸化窒素と四酸化二窒素の平衡反応は有名かつ簡単な式なので、不合格者さんでも正解してきます。(1)とセットの関係ではありますが、実は(2)単独でも正解できるため、全ての受験生さんが正解したい問題です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:合否を分ける1問
大問2
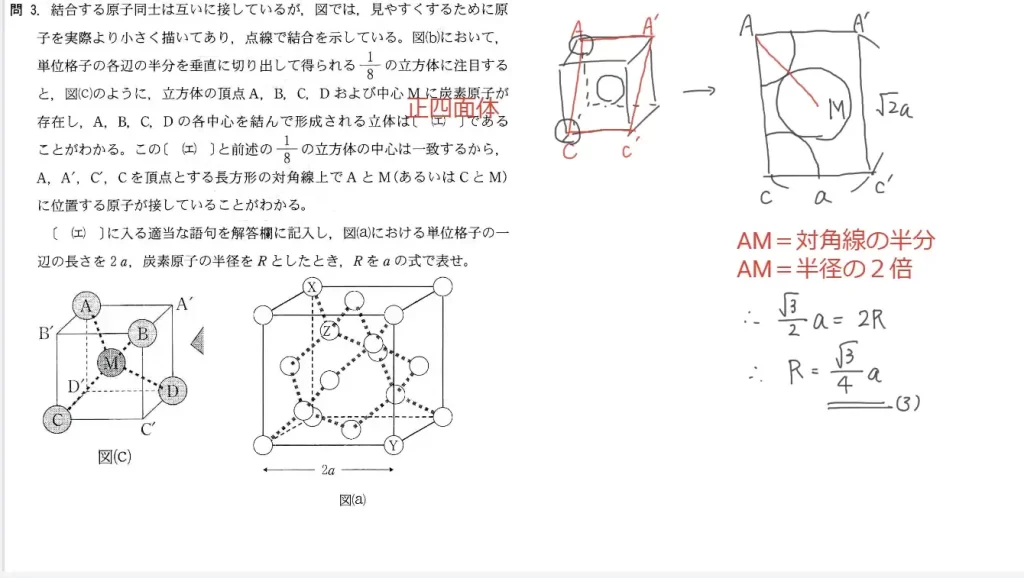
講師としての解説
「結晶構造」からの出題です。
知識の必要性に関して、簡単です。化学に関する知識は少なく、概ね数学の様な問題です。思考力の必要性に関して、普通程度です。立方体に含まれる球の体積割合を計算します。
問1・問2に関して、知識問題です。問題文で指定された通り、頂点の原子に●を、各面の中央の原子に+を記入してください。各原子が単位格子で占める体積は
- 頂点にある原子:1/8
- 面にある原子:1/2
- 格子内部にある原子:1
- Nの値:8
となります。
問3に関して、思考問題です。ポイントは「長方形AA’C’Cで考える事」です。そうすると線分AMに関して「AM=半径の2倍、AM=長方形の対角の半分と解ります。よって「2R=a√3/2」より「R=a√3/4」が正解となります。
問4に関して、思考問題です。「充填率=単位格子内の原子が占める体積÷単位格子の体積」より、各成分を書き出すと以下の様になります。
- 単位格子の体積:(2a)³・・・①
- 原子が占める体積:4πR³/3=4π(a√3/4)³/3・・・②
- 充填率=②÷①=π√3/16=3.14×1.73÷16≒34%(これが正解です)
受験生としての解説
問1に関して、共通テストより簡単なので、全ての受験生さんが正解したい問題です。
問2に関して、共通テストと同等の図形問題なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3・問4に関して、よくあるタイプの問題なので「長方形AA’C’Cで考える」「充填率=球の体積÷立方体の体積」と思い出せれば簡単です。しかし、不合格者さんの一定数はこれに気づけない(あるいは勉強した経験が無い)ため不正解が出るレベルです。合格者さんは正解してくるので、合否を分ける1問より少し簡単な問題です。
- 知識:★(簡単、数学の様な問題)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:完答したい1問
大問3

講師としての解説
「化学平衡」と「反応速度」からの出題です。
知識の必要性に関して、普通程度です。反応速度のしくみ、増減表の理解を問われています。思考力の必要性に関して、普通程度です。問1~問3まで、問題ごとに1つずつ増減表を作ります。問4ではエネルギー図を描きます。量が多いので素早くさばきたい所です、難易度は低めです。
問1に関して、思考問題です。「平衡」という事で増減表を書きましょう。
| A₂ | +B₂ | ↔2AB | |
| 前 | 2.0mol/L | 1.0 | 0 |
| 中 | -0.814 | -0.814 | +0.814×2 |
| 後 | 1.186 | 0.186 | 1.628 |
よって「平衡定数K=[AB]²/[A₂][B₂]=(1.628)²/1.186×0.186≒1.2×10」が正解です。
問2に関して、思考問題です。問題文で与えられた濃度変化の表を埋めていきます。問1で使った増減表の考え方で正解できます。まず(ア)(イ)に関して、「ABの濃度=1.0」に注目してください。ABの濃度が1.0増えたという事は、A₂・B₂の濃度は0.50減ったという事です。よって「ア=1.5、イ=0.50」が正解となります。続いて(オ)(カ)に関して、Bの濃度が0.81減っています(1.0 → 0.19)よって、Aの濃度も0.81減っており、ABの濃度は0.81×2増えているので「オ=1.19≒1.2、カ=1.62≒1.6」が正解です。最後に(ウ)(エ)に関して、(ウ)が2つある事に注意して比の式を立てると「A₂の減少量:ABの増加量=1:2=2.0-ウ:ウ」となります。これを解いて「ウ=1.333≒1.3」そして「エ=1.0-(2.0-ウ)=0.33」が正解です。
問3に関して、思考問題です。反応途中におけるA₂の濃度減少量をxと置くと増減表は以下の様になります。
| A₂ | +B₂ | ↔2AB | |
| 前 | 1.0mol/L | 1.0 | 0 |
| 中 | -x | -x | +2x |
| 後 | 1.0-x | 1.0-x | 2x |
「平衡定数K=(2x)²/(1.0-x)²=12」より「x=0.633≒0.63モル/リットル」となり、よって
- A₂の濃度:1.0-0.63=0.37モル/リットル
- ABの濃度:0.63×2≒1.3モル/リットル
これを満たすグラフは「cとf」が正解です。
問4に関して、思考問題です。色々とエネルギー値を与えられ複雑になっているので「エネルギー図」を描くとよいです。文章では説明しにくいのですが、以下のプロセスで正解が出ます。
- 反応熱=負方向の活性化エネルギー-正方向の活性化エネルギー=185-174=11kJ
- 2ABの結合エネルギー=反応熱+A₂の結合エネルギー+B₂の結合エネルギー=11+436+151=598
- ABの結合エネルギー=598÷2=299kJ/mol(これが正解です)
問5に関して、知識問題です。各選択肢の正誤判定は以下の通りです。
- a:温度を上げると正負両方向の反応速度が上がります。よって、◯が正解です
- b:時間の経過と共に反応物(材料)の濃度が下がるため反応速度は減っていきます。よって、✕が正解です。
- c:平衡状態では正負両方向の反応速度が等しくなり、見た目が止まって見えます。よって、◯が正解です
- d:触媒は活性化エネルギーを下げるので負方向の触媒としても働きます。よって、◯が正解です
- e:触媒は反応速度を上げるため、平衡に達するまでの時間は短くなります。よって、✕が正解です
- f:与式の両辺の物質量が等しいため、圧力を低くしても平衡は移動しません。よって、✕が正解です
受験生としての解説
問1に関して、増減表を書いて平衡定数を計算するだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、(ウ)(エ)が少しトンチが利いてますが、不合格者さんでも乗り越えてくるレベルです。よって、全ての受験生さんが正解したい問題です。
問3に関して、本問単独で出題されれば「合否を分ける1問」でしたが、問2までの流れで解法に乗りやすい状態になっているため、不合格者さんでも一定数が正解してきます。よって、合否を分ける1問より少し簡単な問題です。
問4に関して、不合格者さんには厳しいです。合格者さんでも一定数の不正解が出るレベルなので、正解できれば他者に差をつける1問です。
問5に関して、反応速度の仕組みは不合格者さんでも理解できている場合が多いので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:合否を分ける1問
大問4
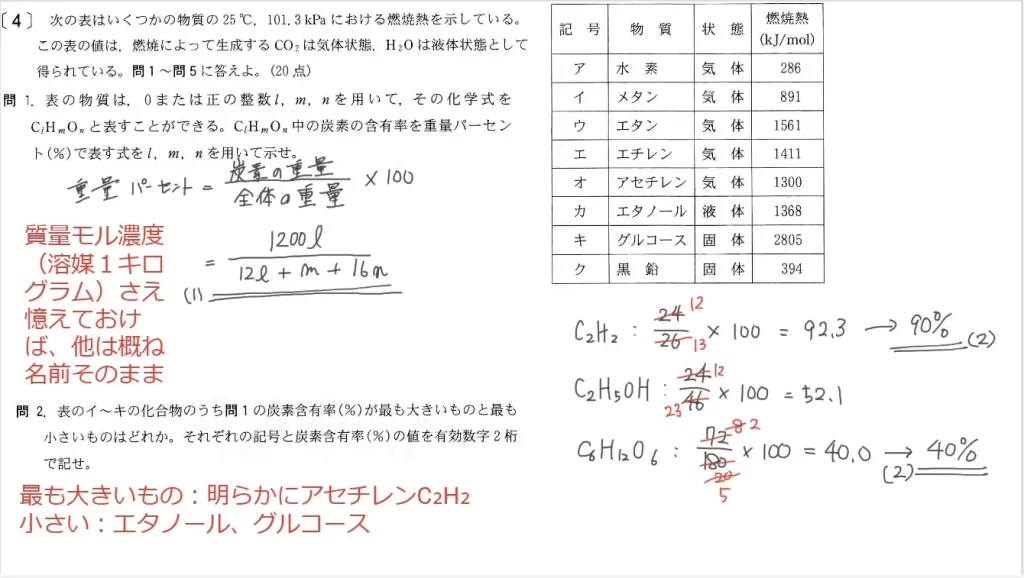
講師としての解説
「熱化学」からの出題です。
知識の必要性に関して、やや簡単です。「反応熱=右辺の生成熱-左辺の生成熱」またはそれに相当する「エネルギー図の利用」ができれば正解できます。思考力の必要性に関して、やや難しいです。本問は「燃焼熱」を前面に出した出題ですが、問題集でガッツリ練習できるタイプではないため、取り付きにくい部分があります。
問1に関して、思考問題です。「重量パーセント=炭素の重量/全体の重量 × 100=1200l/(12l+m+16n)」が正解です。
問2に関して、思考問題です。イ~キまで全ての物資を計算する必要はありません。
- 明らかに炭素含有率が高いもの:アセチレン(24/26=92.3%)
- 炭素含有率が低そうなもの:エタノール(24/46=52.1%)
- 炭素含有率が低そうなもの:グルコース(72/180=40.0%)
よって上記より「オ、90%」「キ、40%」が正解です。
問3に関して、思考問題です。与式の左辺「C原子=l個、H原子=m個」より「b=l、c=m/2」と決まります。よって、右辺の「O原子の数=2l+m/2個」と決まるため「a=(2l+m/2-n)÷2=(4l+m-2n)4」となります。同様に、2番めの与式の右辺から逆算して「d=l、e=m/2、f=n/2」となります。
問4に関して、思考問題です。まず、本問は燃焼熱を使うようなので、メタンの燃焼の式を書いてみましょう。「CH₄(気)+2O₂(気)=CO₂(気)+2H₂O(液)+891kJ」となります。よって、求めるメタンの生成熱をQ(kJ/mol)とおくと「反応熱=右辺の生成熱の和-左辺の生成熱の和」より「891=(286×2+394)-Q」となり、これを解いて「Q=75kJ/mol」が正解です。
問5に関して、思考問題です。まず、水の蒸発熱が与えられているので「H₂O(液)=H₂O(気)-44kJ」という式を準備します。この式を2倍して与式に加えることにより、与式から扱いにくい「H₂O(気)」を消すことができます。「CH₄(気)+2H₂O(液)=4H₂(気)+CO₂(気)+Q-88kJ」となります。
- CO₂(気)の生成熱は「黒鉛の燃焼熱」
- H₂O(液)の生成熱は「水素の燃焼熱」
- 問4よりメタンの生成熱75kJ/mol
よって「Q-88=CO₂(気)の生成熱-メタン(気)の生成熱-H₂O(液)の生成熱×2=394-75-286×2=-253」これを解いて「Q=-165kJ」が正解です。
受験生としての解説
問1・問2に関して、仮に「重量パーセント」を知らなかったとしても、不合格者さんでも正解を導き出してくるレベルです。よって、全ての受験生さんが正解したい問題です。
問3に関して、両辺の原子数のツジツマを合わせるだけなので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4・問5に関して、燃焼を経由するルートは頻出ではないため、合格者さんでも一定数の不正解者が出るレベルです。よって、合否を分ける1問より少し難しい問題です。
- 知識:★★(やや簡単)
- 思考:★★★★(やや難しい)
- 総合:★★★(普通)
- 短評:問3までは正解したい
大問5

講師としての解説
「構造決定」からの出題です。
知識の必要性に関して、やや簡単です。環状構造、二重結合の酸化開裂、エステル化が出てきますが、構造決定問題としては簡単な部類です。思考力の必要性に関して、やや簡単です。ヒネった部分はなく、実験内容に素直に応じていけば正解が出ます。
問1に関して、知識問題です。水素を付加させているので「ニッケル」が正解です。
問2に関して、思考問題です。実験1において、水素を付加して化学式「C₅H₁₀」のBが出ているため(二重結合が無いのにアルケンの式形なので)Bはシクロペンタンと解ります。よって、Aは「シクロペンテン、C₅H₈」となります。
問3に関して、知識問題です。過マンガン酸カリウムによる「酸化作用」が正解です。
問4に関して、知識問題です。実験3において、シクロペンテンの二重結合が酸化で開裂し、分子が直線形になって、両端が-COOHになった事が読み取れます。よって正解は「カルボキシル基、エステル化」です。
問5に関して、知識問題です。問4でカルボキシル基が出てきたので、問題文「強い分子間力」より水素結合とわかります。よって、2つの分子を描いてカルボキシル基を向かい合わせにし、OとHの間に破線を引けば正解となります。
問6に関して、思考問題です。実験2においてAに臭素を付加させて生じた化合物C、この臭素原子が付加した2つの炭素原子が不斉炭素原子になっています。これを◯で囲めば正解です。
受験生としての解説
問1に関して、「水素付加の触媒」は意外に盲点な部分です。合格者さんでも一定の不正解者が出るレベルなので、正解できれば他者に差をつける1問です。
問2に関して、構造決定の中でも簡単な部類なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、過マンガン酸カリウムを用いているので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、酸化による二重結合の開裂は、共通テストでも見かけるレベルです。よって、不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
問5に関して、問4からの流れで水素結合も解りやすくなっています。よって、不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
- 知識:★★(やや簡単)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:完答したい1問
大問6

講師としての解説
「タンパク質」と「油脂」からの出題です。
知識の必要性に関して、やや簡単です。アミノ酸が脱水縮合すること、油脂が「高級脂肪酸とグリセリンのエステル」であることなど知っていれば正解できます。思考力の必要性に関して、やや簡単です。最終問題の問2(2)以外は簡単です。そして、問2(2)はやや難しいです。
問1(1)に関して、思考問題です。分子量25000のカゼインが2.50×10⁻¹グラムあるということで「2.50×10⁻¹÷25000=1.00×10⁻⁵モル」が正解です。
問1(2)に関して、思考問題です。3つのアミノ酸が2回脱水してトリペプチドTVYができているので「119+117+181-18×2=3.81×10²」が正解です。
問1(3)に関して、思考問題です。カゼインとトリペプチドTVYは1:1の関係で生じるため、問1のモル数と問2の分子量をかけて「1.00×10⁻⁵×381=3.81×10⁻³グラム」が正解です。
問2(1)に関して、知識問題です。(ア)はC₁₇に対しH₃₅より飽和脂肪酸なので、二重結合の数は「0個」です。(イ)は(ア)の状態からH原子が6個減っているので、二重結合の数は「3個」です。(ウ)は飽和脂肪酸ならH₄₃になるところがH₃₁でH原子が12個減っているので、二重結合の数は「6個」です。
問2(2)に関して、思考問題です。「パルミチン酸:ステアリン酸:オレイン酸=2:1:3」という事で、もし油脂が2個あれば、グリセリンの6つの手に対し上記の高級脂肪酸が2個・1個・3個付くことになります。この時の分子量を解析してみましょう。
- グリセリン2つ:92×2
- パルミチン酸が2つ:256×2
- ステアリン酸1つ:284
- オレイン酸3つ:282×3
- 脱水6ヶ所:-18×6
- 上記の合計:1718(油脂2個分)
- 平均分子量:1718÷2=859(これが正解)
受験生としての解説
問1(1)~(3)に関して、共通テストより簡単な計算問題なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2(1)に関して、最初にステアリン酸(この分野の基準と言える物質)を与えてくれているので、その流れを使って不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2(2)に関して、油脂を2つ用意して「高級脂肪酸が2個・1個・3個付く」と発想できれば簡単な問題です。しかし、割合で考えてしまうと計算が複雑になるため、合格者さんでも一定数の不正解者が出るレベルです。よって、正解できれば他者に差をつける1問です。
- 知識:★★(やや簡単)
- 思考:★★★(普通)
- 総合:★★(やや簡単)
- 短評:問2(2)以外は簡単
大問7A

講師としての解説
「繊維」からの出題です。
知識の必要性に関して、普通程度です。勉強が行き届きにくい「繊維」「洗剤」の基礎知識を問われています。思考力の必要性に関して、簡単です。ほぼ全て知識問題なので考える事は少ないです。
問1に関して、知識問題です。問題文「合成される」より、天然繊維の「羊毛・木綿」再生繊維の「レーヨン」は候補から脱落します。残り3つの内、ポリエチレンテレフタラートと6,6-ナイロンは縮合重合なので不可。そして、最後の1つ「ポリアクリロニトリルは付加重合」なので、これが正解です。
問2に関して、知識問題です。問題文にエチレングリコールとテレフタル酸が書いてあるので、この2者を縮合重合した「ポリエチレンテレフタラート」が正解です。
問3に関して、知識問題です。選択肢ア・ウは強酸の「スルホ基」と強塩基の「NaOH」からできているため合成洗剤(中性)です。これに対し、イは「高級脂肪酸(弱酸)」と強塩基「NaOH」の塩なので、水溶液は塩基性(アルカリ性)を示します。よって、問題文「羊毛はアルカリに弱い」より不適切となります。イが正解です。
問4に関して、知識問題です。木綿に関する◯✕問題を5つ答えます。
- ア:セルロースをセロビオースに分解する酵素はアミラーゼではなくセルラーゼです、よって✕が正解です
- イ:セルロースは冷水に溶けませんが、温水にも溶けません。よって、✕が正解です
- ウ:人間はセルロースを分解する酵素を持ちません。よって、◯が正解です
- エ:ヨウ素反応はグルコースが螺旋を描き、螺旋にヨウ素が取り込まれ時に色をつける反応です。よって、直鎖状のセルロースではヨウ素反応しないため、✕が正解です
- オ:レーヨンはセルロースを溶かした液を糸状に固めた繊維なので、◯が正解です
受験生としての解説
問1に関して、ポリアクリロニトリルは合格者さんでも一定数が憶えてないレベルの物質です。しかし、不正解の選択肢5つが「不正解である理由」は合格者さんなら解るので、消去法で正解してきます。これに対し、不合格者さんだと消去法が使えないため正解は難しいです。よって、合否を分ける1問です。
問2に関して、PETは不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、「合成洗剤」は合格者さんでも勉強が行き届きにくい部分です。よって、正解できれば他者に差をつける1問です。
問4に関して、セルロースの細かい性質も勉強が行き届きにくい部分です。よって、5問全て正解は合格者さんでもやや難しいので、正解できれば他者に差をつける1問です。
- 知識:★★★(普通)
- 思考:★(簡単)
- 総合:★★★(普通)
- 短評:7Bを選択するよりは本問が良い
大問7B
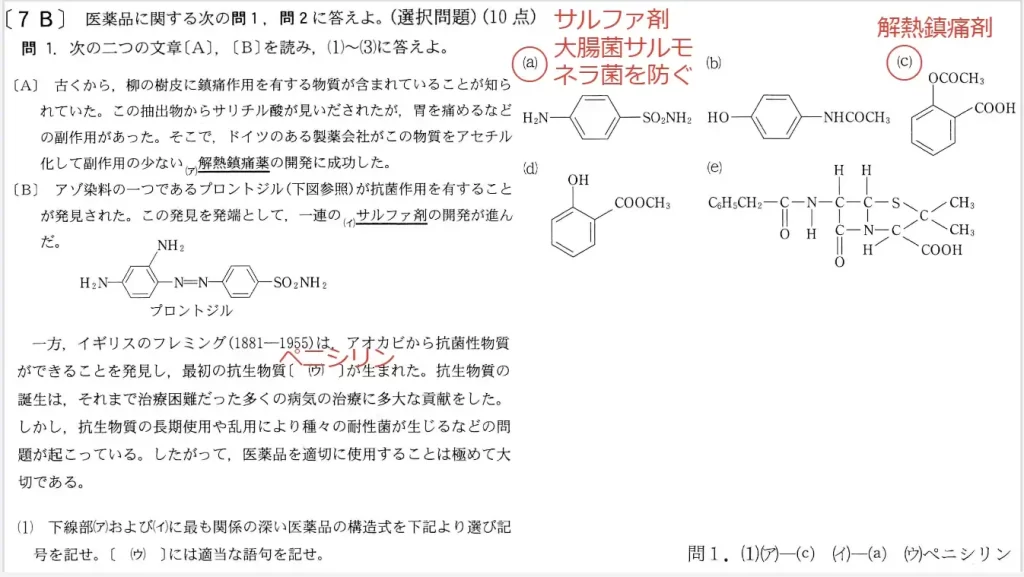
講師としての解説
「生命と物質」からの出題です。
知識の必要性に関して、やや難しいです。化学の知識というより医薬品の知識です。思考力の必要性に関して、やや簡単です。概ね知識問題なので、あまり考える事はありません。
問1(1)に関して、知識問題です。解熱鎮痛薬は(C)のアセチルサリチル酸です。サルファ剤の基本構造は選択肢(a)p-アミノベンゼンスルホンアミドです。
問1(2)に関して、知識問題です。薬剤に関する◯✕問題を3つ答えます。
- a:プロントジルは体内で代謝されて有効成分になるので、◯が正解です
- b:サルファ剤は化学的に合成された化合物なので、✕が正解です
- c:サルファ剤は人間に毒性を示さず最近に対して選択毒性を持つので、◯が正解です
問1(3)に関して、知識問題です。サルファ剤は葉酸を合成する成分の1つであるp-アミノ安息香酸と構造が似ています。よって、選択肢aが正解です。
問2に関して、知識問題です。「NaHCO₃+HCl → NaCl+CO₂+H₂O」と反応することで胃酸(HCl)を中和するはたらきがあります。よって選択肢(3)が正解です。
受験生としての解説
問1・問2に関して、特殊な1問です。化学よりも医薬品に寄った知識問題であり
- 「教科書そのままの出題だった」という人もいれば
- 「全く見たことも聞いた事もない」という人もいました
選択問題なので、本問ではなく大問7Aを選んだ方が良いです。
- 知識:★★★★(やや難しい)
- 思考:★★(やや簡単)
- 総合:★★★★(やや難しい)
- 短評:選択問題は7Aを選んだ方が良い
九州大学の化学2005年・平成17年度
大問1

講師としての解説
「混合気体の燃焼」からの出題です。
知識の必要性に関して、簡単です。燃焼の式が書ければ十分です。思考力の必要性に関して、やや簡単です。不完全燃焼した気体の割合が不明ですが、計算はシンプルです。
問1に関して、知識問題です。メタンの完全燃焼の式は「CH₄+2O₂ → CO₂+2H₂O」が正解です。
問2に関して、思考問題です。反応後の状態は以下のとおりです。
| CH₄ | +2O₂ | → CO₂ | +2H₂O | |
| 後 | 0.4モル | 0.8 | 0.4 | 0.8 |
| 2H₂ | +O₂ | → 2H₂O | ||
| 後 | 0.1モル | 0.05 | 0.1 |
よって、正解は以下の通りです。
- O₂:32×0.15モル=4.8g
- CO₂:44.0×0.4=17.6g
- H₂O:18.0×0.9=16.2g
問3に関して、思考問題です。燃焼後の気体のモル数は0.55モル(0.4+0.1+0.05)なので、状態方程式より「P=nRT/V=0.55×0.0821×273/10≒1.2atm」が正解です。
問4に関して、知識問題です。メタンの不完全燃焼なので、右辺にCOが来ると決まっています。そこからツジツマを合わせると「2CH₄+3O₂ → 2CO+4H₂O」が正解です。
問5に関して、思考問題です。メタンの一部が不完全燃焼となっているため
- 完全燃焼したメタン:xモル
- 不完全燃焼したメタン:yモル
と置いて考えます。
| 2H₂ | +O₂ | → 2H₂O | |
| 後 | 0.2モル | 0.1 | 0.2 |
| CH₄ | +2O₂ | → CO₂ | +2H₂O | |
| 後 | xモル | 2x | x | 2x |
| 2CH₄ | +3O₂ | → 2CO | +4H₂O | |
| 後 | yモル | 1.5y | y | 2y |
上記より
- x+y=0.3
- 2x+1.5y=0.2
- よって「x=0.1、y=0.2」
- CO:28.0×0.2モル=5.6g(これが正解です)
- CO₂:44.0×0.1=4.4g(これが正解です)
- H₂O:18.0×(0.2+0.2+0.4)=14.4g(これが正解です)
受験生としての解説
問1~問4に関して、気体反応の基本的な計算問題で共通テストと同等なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問5に関して、本問も共通テストと大差ありませんが、不合格者さんの一定数が不正解になるレベルです。よって、合否を分ける1問より少し簡単な問題です。
- 知識:★(簡単)
- 思考:★★(やや簡単)
- 総合:★★(やや簡単)
- 短評:完答したい1問
進研模試10点台(偏差値35前後)化学が苦手で苦しんでいた学生さん達が、九大化学を解けるようになっています。「化学がキライ、見るのも嫌」と言ってた学生さん達が、楽しそうに勉強しています。
大問2

講師としての解説
「熱化学」からの出題です。
知識の必要性に関して、普通程度です。燃焼熱の定義、熱化学方程式、それらを部分的に結合エネルギーへ応用する知識などが必要です。思考力の必要性に関して、普通程度です。問4の計算がやや複雑です。ペプチド結合だけに絞って考ます。
問1に関して、思考問題です。問題文で5本の熱化学方程式が与えられています。この5本を上から順に①~⑤としてこの先の話を進めていきます。まず、問題文で要求されている燃焼の式を立てます。
- CO(気)+1/2O₂(気)=CO₂(気)+Q₁kJ
- NO(気)+1/2O₂(気)=NO₂(気)+Q₂kJ
式①~⑤を使って上式を再現すると、CO(気)の式は「③-②より、Q₁=283kJ」これが正解の1つです。さらにNO(気)の式は「⑤-④より、Q₂=56.5kJ」ですが、これはNO1モルあたりの発熱量なので「283kJ/56.5kJ≒5.0モル」となり、これが2つめの正解となります。
問2に関して、知識問題です。問題で要求されている式は「燃焼熱」の式なので、主役になる物質はグリシンです(燃焼熱の定義が、ある物質1モルを燃焼させた時の熱量だから)よって、グリシンを1モルと確定し残りの式を立てていくと「C₂H₅O₂N(固)+9/4O₂(気)=2CO₂(気)+5/2H₂O(液)+1/2N₂(気)+966kJ」が正解です。
問3に関して、思考問題です。グリシンの生成熱(xと置く)を求める問題なので、問2「グリシンの燃焼熱の式」を利用します。「反応熱=右辺の生成熱の和-左辺の生成熱の和」より「966kJ=③×2+①×5/2-x=394×2+286×5/2-x」となり、これを解いて「x=537kJ/mol」が正解です。
問4に関して、思考問題です。まず、ペプチド結合1モルで何kJエネルギーが増えるか求めます。反応式は「COOH+NH₂ = CONH +H₂O+QkJ」と書けるので「反応熱Q=右辺で新しく生じる結合エネルギーの和-左辺で失われる結合エネルギーの和=463×2+292-(391+352+463)=12kJ」となります。よって
- ペプチド結合1モルで12kJ増える
- 問題文より、実際は48kJ増えた
- よってペプチド結合は4モル発生
- よって正解は「5分子」です
受験生としての解説
問1に関して、求める式が与式①~⑤の引き算だけで書けるので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、「燃焼熱の定義」に沿ってグリシンを1モルに固定する事(他の物質の係数が分数になる事)は不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問3に関して、「反応熱=両辺の生成熱の差」である事は不合格者さんには厳しく、合格者さんは正解してきます。よって、合否を分ける1問です。
問4に関して、問3が複雑になった問題なので、合格者さんでも一定の不正解者が出ます。よって、正解できれば他者に差をつける1問です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:問3までは正解したい
大問3

講師としての解説
「電気分解」からの出題です。
知識の必要性に関して、普通程度です。電池が1つ・電解槽が2つで計6つの極板における反応式を使います。難しくはありませんが、幅広い基礎知識を求められています。思考力の必要性に関して、普通程度です。少し量が多く、やや簡単な問題が並んでいます。
問1に関して、知識問題です。鉛蓄電池の正極・負極、電解槽Aの陰極でおこる反応を答えます。
- 正極:PbO₂+4H⁺+SO₄²⁻+2e⁻ → PbSO₄+2H₂O
- 負極:Pb+SO₄²⁻ → PbSO₄+2e⁻
- 電解槽A・陰極:Cu²⁺+2e⁻ → Cu
問2に関して、思考問題です。鉛蓄電池の正極ではPbO₂が消費される度にPbSO₄が生じ、結果としてPbO₂を1モル消費する毎に64.1g増加します。今、実際の増加量は0.320gなので消費されたPbO₂の物質量は「0.320/64.1≒5.0×10⁻³モル」が正解です。
問3に関して、思考問題です。電解槽Aでは陽極で溶け出した銅と同じ物質料の銅が陰極で析出します。よって「0.159/63.6=2.5×10⁻³モル」が正解です。
問4に関して、思考問題です。「回路Bに流れた電気量=全体を流れた電気量-回路Aを流れた電気量=(5.0×10⁻³×2-2.5×10⁻³×2)×96500=482.5≒4.8×10²クーロン」が正解です。
問5に関して、思考問題です。問題文に「電流は0.25A」と書いてあるので、電流を流した時間t秒として「0.25×t=482.5」となります。よって「t=1930≒1.9×10³秒」が正解です。
問6に関して、思考問題です。電解槽Bの陽極では「2H₂O→O₂+4H⁺+4e⁻」の反応が起こるため、電子が1モル流れる度にH⁺が1モル発生します。よって「[H⁺]=5.0×10⁻³×1000/500=1.0×10⁻²」より「pH=-log[H⁺]=2.0」が正解です。
受験生としての解説
問1に関して、鉛蓄電池の反応式なので合格者さんは正解してきます。しかし、不合格者さんの一定数は不正解になるレベルなので、合否を分ける1問より少し簡単な問題です。
問2に関して、不合格者さんでも正解してくるレベルの計算です。しかし、本問に参加するためには問1の正解が必要なので、問1とセットで、合否をわける1問より少し簡単な問題です。
問3に関して、本問は共通テストと同等であり、問1・問2の正解も必要ないため、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、本問自体は不合格者さんでも正解してきますが、全体を流れた電気量を知るためには問1正解が必要です。よって、問1とセットで合否を分ける1問より少し簡単な問題です。
問5に関して、本問も共通テストと同等なので不合格者さんでも正解してきますが、参加するには問1の正解が必要です。よって、問1とセットで、合否を分ける1問より少し簡単な問題となります。
問6に関して、電気分解において電子のやり取りを「水」が行う場合、反応式が複雑になるため不合格者さんには厳しいレベルになります。合格者さんは正解してくるので、合否を分ける1問です。
- 知識:★★★(普通)
- 思考:★★★(普通)
- 総合:★★★(普通)
- 短評:合否を分ける1問
大問4

講師としての解説
「芳香族の分離」からの出題です。
知識の必要性に関して、やや難しいです。基礎知識の集合体ですが、数が多いです。思考力の必要性に関して、普通程度です。やや量が多めの分離操作の後に、簡単ではありますが平衡定数の計算があります。
問1に関して、知識問題です。最初の問題ではありますが、ほぼ全ての物質を明らかにする必要があります。
- 操作(1):「塩化鉄(Ⅲ)で赤紫色」よりAはフェノール類です
- 操作(2):「ナトリウム塩を高温・高圧カで二酸化炭素と反応(その後、希硫酸で酸に戻している)」と言えば「Bはサリチル酸」で確定です。よって、Aのナトリウム塩がナトリウムフェノキシドで確定するため、「Aはフェノール」で確定です
- 操作(3):「ベンゼンを濃硫酸と濃硝酸と反応」より「Cはニトロベンゼン」で確定です
- 操作(4):「酸であるにも関わらず・・・銀鏡を生じた」より、「Dはギ酸」で確定です。
- 操作(5):「エチレンに水蒸気」より「Fはエタノール」で確定です
- 操作(6):「トルエンの酸化反応」より「Gは安息香酸」で確定です
- 化合物E:FエタノールとG安息香酸のエステル「安息香酸エチル」と思われます
これで問1を解く準備ができました。問題文に戻り、分離操作を確認していきます。
- 「A~Eの混合物・・・水とジエチルエーテルを加えて振り」より、エーテル層ⅠへはA・B・C・E(全てベンゼン環を持つ)水層Ⅰへは「ギ酸(極性分子)」が分離します
- 「エーテル層Ⅰに水酸化ナトリウム水溶液」より、水層ⅡへA・Bが進み(酸なので中和反応で塩を生じて溶ける)エーテル層ⅡへC・Eが進みます
- 「水層2に二酸化炭素を通じ」より、弱酸の遊離によって塩状態を解除されたAフェノールがエーテル層3へ、水層3には塩状態のサリチル酸が分離します
- 「残った油状物に水酸化ナトリウム溶液を加えて加熱」より、エステルのけん化をしているため、E安息香酸エチルがエステル状態を解除されてナトリウム塩となり水層へ分離します。よって、エーテル層4はCニトロベンゼンです。
以上で問1の正解となります。
問2に関して、知識問題です。問題文「Eは、FとGのエステル結合」という内容より、Eは「安息香酸エチル」が正解です。
問3に関して、知識問題です。問題文「水酸化ナトリウムおよびヨウ素と温めると黄色沈殿」という内容より、正解は「ヨードホルム」です。
問4に関して、思考問題です。ポイントは問題文の「この反応の平衡定数K」です。つまり、正解を導く式は「K=[A⁻][H₂CO₃]/[HA][HCO₃⁻]」なので、ヒントを頼りにこの形を目指すと正解できます。与えられたヒントは
- K₁=[A⁻][H⁺]/[HA]=1.5×10⁻¹⁰
- K₂=[HCO₃⁻][H⁺]/[H₂CO₃]=4.5×10⁻⁷
なので、「K=K₁/K₂≒3.3×10⁻⁴」が正解です。
問5に関して、知識問題です。最弱レベルの酸であるフェノールに、弱い酸(フェノールよりは強い)である炭酸(二酸化炭素+水)を加えると、フェノールが遊離しているため選択肢(エ)が正解です。思考問題として出題されていますが、「弱酸の遊離」という知識問題として正解した学生さんの方が多いと思われます。
受験生としての解説
問1に関して、不合格者さんには化合物A~Eを「全て」割り出すことが難しいため、その分離操作を見抜くことは厳しいです。合格者さんは乗り越えてくるので、合否を分ける1問です。
問2に関して、不合格者さんでも正解してくるレベルですが、本問に参加するためには問1の正解が必要です。よって、問1とセットで合否を分ける1問です。
問3に関して、本問に参加するためには問1の正解が必要ですが、問題文の「黄色沈殿」という文言だけで「ヨードホルム」と書けば、かなり良い確率で当たります(体感だと80%以上)よって、不合格者さんでも正解してくるので、全ての受験生さんが正解したい問題です。
問4に関して、本問は化合物A(フェノール)の問題ですが、問1を正解せずとも参加できます。よって、問4の難易度だけで考えれば、合否を分ける1問より少し簡単なレベルです。
問5に関して、「弱酸の遊離」は不合格者さんでも正解してきます。問1を正解できずとも、本問単独で正解を見抜けるため、全ての受験生さんが正解したい問題です。
- 知識:★★★★(やや難しい、全て基礎だが多い)
- 思考:★★★(普通)
- 総合:★★★★(やや難しい)
- 短評:問1が不正解でも問3~問5に参加できる
大問5

講師としての解説
「14族元素」からの出題です。
知識の必要性に関して、やや簡単です。問2の「14族元素の縦読み」が少し難しいですが、他は共通テストと同等です。思考力の必要性に関して、簡単です。問3で少し考える問題はありますが、基本的に知識問題ばかりです。
問1に関して、知識問題です。14族元素に関する語句問題を14個答えます。単体の炭素として最も硬く透明な結晶の「ア:ダイヤモンド」は1つの炭素原子が他の「イ:4」個の炭素原子と「ウ:共有」結合を形成しています。このためダイヤモンドの結晶は「エ:1」個の分子と考えることができ、電気伝導度は非常に「オ:小さい」です。一方、黒鉛は炭素原子が他の「カ:3」個の炭素原子と共有結合し、価電子の内「キ:1」個は結合に関連しないため分子内を自由に動けます。このため、黒鉛の電気伝導度は「ク:大きい」です。炭素と水素だけから成る化合物を「ケ:炭化水素」といいます。第3周期14族元素の「コ:ケイ素」の結晶は炭素と類似の構造を持ち、電気伝導性の観点から「サ:半導体」に分類されています。ケイ素の酸化物を「シ:二酸化ケイ素」といいます。第5周期14族元素の「ス:スズ」でメッキした鉄をブリキといいます。これは鉄とスズの「セ:イオン化傾向」の差を利用した物質です。
問2に関して、知識問題です。14族元素のゴロ合わせは「谷繁すんな!(炭素、Si、Ge、スズ、鉛)」であり、問題文で使われていない「鉛」か「ゲルマニウム」を答えると正解です。
問3に関して、思考問題です。C1個から順に考えていけば正解できます。論理的に考えるならば、4つの側鎖が
- CH2=CH
- H
- CH₃
- CH₃-CH₂-
となれば、最小の炭素数で不斉炭素原子が生じると解ります。
問4に関して、知識問題です。鉄とスズのイオン化傾向は「スズ<鉄」となります。
受験生としての解説
問1に関して、語句問題が14個ありますが全て簡単な部類なので、不合格者さんでも1・2問ミスでまとめてきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、周期表を縦に読む事は勉強が行き届きにくい部分です。よって、不合格者さんには厳しく、合格者さんは正解してくるので、合否を分ける1問です。
問3に関して、不斉炭素原子は不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問4に関して、イオン化傾向の大小なので不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
- 知識:★★(やや簡単)
- 思考:★(簡単)
- 総合:★(簡単)
- 短評:完答したい1問
大問6

講師としての解説
「構造決定」と「高分子」からの出題です。
知識の必要性に関して、やや難しいです。構造決定に高分子が絡んでくると、難易度が1段上がります。思考力の必要性に関して、やや難しいです。自分で構造を仮定し、仮定が正しいか確認しながら進めていくタイプなので思考力を要します。
問1に関して、思考問題です。
- ヒント(1):Cはカルボキシル基を持つ
- ヒント(2):Cはトランス異性体である
という情報より「Cは2-ブテン酸(2-ブテンの端っこが-COOHになったもの)」と決まります。続いてA・Bですが、決定的なヒントが無いため
- ヒント(1):A・B・Dはエステル結合
- ヒント(2):A・B・Cは炭素間二重結合を持つ
- ヒント(3):A・Bにはいずれもシスートランス異性体が無い
- 分子式「C₄H₆O₂」
これらの条件を満たす構造を描くと
- プロペン酸メチル(プロペンの端がCOOCH₃になったもの)
- 酢酸ビニル(ビニルアルコールがアセチル化されたもの)
上記2つしかないと解ります。その上で
- ヒント(5):Aの重合体を水酸化ナトリウムで加水分解し中和すると、カルボキシル基を持つ高分子E
- ヒント(6):Bの重合体を水酸化ナトリウムで加水分解し中和すると、ヒドロキシ基を持つ高分子F
というヒントより、加水分解でカルボン酸になるAが「プロペン酸メチル」、ヒドロキシ基になるBが「酢酸ビニル」と確定します。続いてDに関して
- ヒント(2):Dは炭素間二重結合を持たない(環状構造)
- ヒント(4):水酸化ナトリウムで加水分解し酸化すると、4-ヒドロキシ酪酸
より、Dは「CH2-CH2-CH2-COOを環状にしたもの」となります。
問2に関して、知識問題です。語句問題を5つ答えます。A・B・Cはいずれも炭素間に二重結合を持っており「ア:付加」重合することで高分子を得られます。Aの重合体を水酸化ナトリウムで加水分解し中和すると、カルボキシ基を持つ高分子Eと「イ:メタノール」を得られます。Bの重合体を水酸化ナトリウムで加水分解し中和すると、ヒドロキシ基を持つ高分子Fと「ウ:酢酸」が得られます。Bは「エ:アセチレン」に酢酸を作用することで合成されます。高分子Fの水溶液をホルムアルデヒド水溶液で処理すると、合成繊維である「オ:ビニロン」が得られます。
問3に関して、思考問題です。問1・問2を解く過程で
- Eは「ポリアクリル酸(ビニル基のRがCOOHになったもの)」
- Fは「ポリビニルアルコール」
と判明しています。
問4に関して、思考問題です。得られたビニロンに関して
- アセタールかされてない部分:8000×60%×44(繰り返し単位の式量)=211200
- アセタール化された部分:8000×40%×1/2(アセタール化により2個1単位)×100(繰り返し単位の式量)=160000
- 分子量=211200+160000=371200=3.71×10⁵(これが正解です)
問5に関して、思考問題です。問題文の指示そのままで正解が出ます。化合物Cの二重結合をはずし、Clを2つ付けたものが正解です。不斉炭素の数は2個です。
受験生としての解説
問1に関して、合格者さんは正解してくるが、不合格者さんには厳しい1問です。よって、合否を分ける1問です。
問2に関して、本問単独で見ても不合格者さんにはやや厳しい語句問題であり、本問に酸化するためには問1の正解も必要です。よって、問1とセットで合否を分ける1問です。
問3に関して、合格者さんでも一定数が不正解になるレベルです。よって、正解できれば他者に差をつける1問です。
問4に関して、高分子の割合計算は不合格者さんには厳しく、合格者さんは正解してきます。よって、合否を分ける1問です。
問5に関して、本問単体なら不合格者さんでも正解してきますが、参加するためには問1の正解が必要です。よって、問1とセットで合否を分ける1問です。
- 知識:★★★★(やや難しい)
- 思考:★★★★(やや難しい)
- 総合:★★★★(やや難しい)
- 短評:問1を突破したい(残りの問題の参加権利)
九州大学の化学2004年・平成16年度
大問1

講師としての解説
「化学反応」からの出題です。
知識の必要性に関して、簡単です。語句問題が5つありますが初歩的なものです。思考力の必要性に関して、普通程度です。難しくはないのですが、やや煩わしい計算が2題あります。
問1(a)~(e)に関して、知識問題です。化学反応に関する語句問題を5つ答えます。水分子は酸素原子の水素原子が2個「a:共有」結合したものです。水分子における酸素原子の電子配置は「b:ネオン」原子と類似しています。これに対し、塩化カリウムに存在する化学結合を「c:イオン結合」といいます。共有結合の反応において、水と一酸化炭素が1モルずつ反応すると「d:1」モルのの二酸化炭素と「e:1」モルの水素が発生します。
問1(f)~(i)に関して、思考問題です。
| CH₄ | +H₂O | → CO | +3H₂ | |
| 前 | 20/16 =1.25モル | 20/18 =1.111 | 0 | 0 |
| 中 | -13.5/18 | -13.5/18 | +13.5/18 | +13.5×3/18 |
| 後 | 0.5 | 0.36111 | 0.75 | 2.25 |
上記の表より「f:21.0」グラムの二酸化炭素と「g:4.5」グラムの水素が生成し、「h:8.0」グラムのメタンが残ります。温度・圧力一定の条件で反応前後の体積を比較すると「反応後÷反応前=(0.5+0.36111+0.75+2.25)÷(1.25+1.111)≒1.6倍」が(i)の正解です。
問2に関して、思考問題です。銀と酸素の反応式は「2Ag+O₂ → Ag₂O」であり、この反応によって質量は「215.8 → 231.8」となっています。今、問題文で「体積が1.56倍になった」ことが判っているので、密度は「(231.8÷215.8)/1.56≒0.6885倍」になった事が解ります。よって「銀の密度×0.6885=酸化銀の密度=7.229…≒7.23g/cm³」が正解です。
受験生としての解説
問1に関して、計算がやや煩わしいですが語句・計算ともに共通テストと同等なので、不合格者さんでも正解してきます。よって、全ての受験生さんが正解したい問題です。
問2に関して、「密度の倍率=質量の倍率/体積の倍率」と気づくことは、不合格者さんの中に一定数の不正解者が出るレベルです。合格者さんは乗り越えてくるので、合否を分ける1問より少し簡単な問題です。
- 知識:★(簡単)
- 思考:★★★(普通)
- 総合:★★(やや簡単)
- 短評:完答したい1問
おわりに
上記の考え方で取り組んでいけば、高校偏差値60の高校で落ちこぼれて
- 1番簡単な国立大学を目指せない
- 九州工業大学・熊本大学など想像できない
という学生さんでも、トップ高校との「才能の差」を補って九大合格できます。
「九大化学の攻略法」は現在執筆中です。
考え方は「数学・英語」と同じなので、よかったら以下を御覧ください。